
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。它与二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
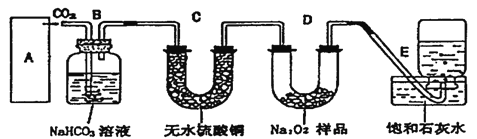
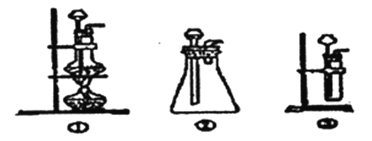
(l)A中制取CO2的装置,应从下列图①、②、③中选哪个图:_____。
B装置的作用是________, C装置内可能出现的现象是________。为了检验E中收集到的气体,在取出集气瓶后,用________的木条伸入集气瓶内,木条会出现________。
(2)若E中的石灰水出现轻微白色浑浊,请说明原因:________。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?________。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(答大或小),相差约________mL(取整数值,所用数据均在标准状况下测定),这是由于________。
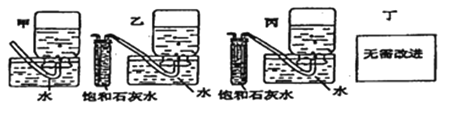
(5)你认为上述A~E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项:________。(用甲、乙、丙、丁回答)
【答案】 图2 吸收A装置中产生的酸雾 变蓝 带火星的木条 复燃 D中有部分CO2未参加反应流入E中生成沉淀 E中石灰水的白色浑浊明显增加,瓶内液面的下降接近停止 小 30 因样品中含有不与CO2反应生成气体的杂质 乙
【解析】(1)该反应的药品是固体和液体,且不需加热,所以所需装置为固液混合不加热型,所以排除①;③中只能制取少量二氧化碳而不能制取大量二氧化碳,所以排除③,故选②.
大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体、水蒸气,吸收A装置中产生的酸雾,氯化氢和碳酸氢钠能反应生成二氧化碳,二氧化碳和碳酸氢钠不反应,水蒸气能使无水硫酸铜由白色变蓝色,所以C装置内可能出现的现象是白色固体变蓝色;过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃.
(2)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致.
(3)过氧化钠样品接近反应完毕时,二氧化碳含量增加,E中石灰水的白色浑浊明显增加,瓶内液面的下降接近停止。
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2 --- -O2;
2mol 22.4L
1.95g/78g/mol v
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.280mL-250mL=30mL;原因是Na2O2可能含有其它杂质;D装置可能有氧气未被排出.
(5)E装置容易产生倒吸现象,所以不安全、不合理,所以需要改进;饱和石灰水能和二氧化碳反应,所以饱和石灰水的作用是吸收二氧化碳,收集较纯净的氧气,乙试管中进气管较长,二氧化碳能充分和饱和石灰水反应,丙试管中进气管较短,导致二氧化碳和饱和石灰水反应不充分,且随着气体的进入,试管中的液体被排到水槽中,故选乙.


科目:高中化学 来源: 题型:
【题目】元素性质随原子序数的递增呈周期性变化的实质是( )
A. 元素的相对原子质量增大,量变引起质变
B. 原子的电子层数增多
C. 原子核外电子排布呈周期性变化
D. 原子半径呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )。
A. 所用NaOH已吸潮 B. 向容量瓶加水时眼睛一直仰视液面
C. 有少量NaOH溶液残留在烧杯内 D. 向容量瓶加水时眼睛一直俯视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B. AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C. 三氯化铁溶液中加入铁粉: ![]()
D. FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三个容器中最初存在的物质的量如图所示,三个容器最初的容积相等、温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的是( ) 
A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B.平衡时N2O4的百分含量:乙>甲=丙
C.平衡时甲中NO2 与丙中N2O4 的转化率不可能相同
D.平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素D,E,F,X,Y,Z的原子序数依次增大,D,E两元素最高正价与最低负价之和均为0,E元素的一种同位素常用于考古断代,D和X同主族,F和Y同主族,F的多种化合物可用作化肥,豆科植物的根瘤菌可将其单质转化为化合物,X和Z形成的二元化合物是厨房常用的调味品.回答下列问题:
①E元素在元素周期表中的位置是 .
②由D和F,Y,Z所形成的最简单常见共价型化合物中,还原性最强的是(用化学式表示).
③F,X,Z形成的简单离子半径从大到小顺序为(用离子符号表示).
④X与Z能形成一种离子化合物,用电子式表示其形成过程: .
⑤2012年,罗马大学科学家制造出F4分子,则F4和F2两种单质的关系是 .
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写错误的是( )
A. CaCl2= Ca2++2Cl- B. Na2SO4=2Na++SO42-
C. HNO3=H++NO3- D. KClO3 =K++Cl-+3O2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com