
【题目】下列粒子中与NH4+具有不同质子数但具有相同电子数的粒子是
A. Na+B. Cl-C. OH-D. -CH3
科目:高中化学 来源: 题型:
【题目】短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等:
(1)下列能说明碳、硫两种元素非金属性相对强弱的是(填序号)、
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为﹣2价
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似.羰基硫(COS)的电子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。它与二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
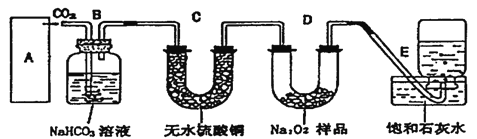
(l)A中制取CO2的装置,应从下列图①、②、③中选哪个图:_____。
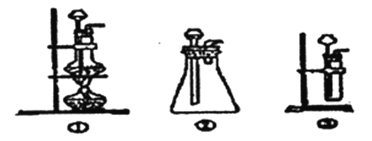
B装置的作用是________, C装置内可能出现的现象是________。为了检验E中收集到的气体,在取出集气瓶后,用________的木条伸入集气瓶内,木条会出现________。
(2)若E中的石灰水出现轻微白色浑浊,请说明原因:________。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?________。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(答大或小),相差约________mL(取整数值,所用数据均在标准状况下测定),这是由于________。
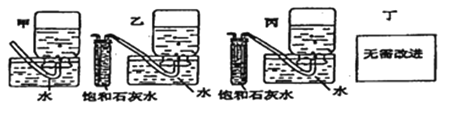
(5)你认为上述A~E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项:________。(用甲、乙、丙、丁回答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( ) 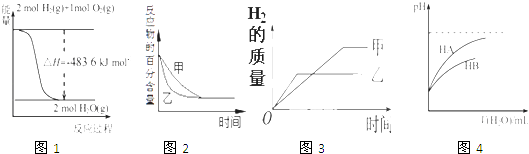
A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJmol﹣1
B.图2表示压强对可逆反应2A(g)+2 B(g)3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是一个一次性加热杯的示意图.当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升.制造此加热杯可选用的固体碎块是( ) 
A.硝酸铵
B.生石灰
C.氯化镁
D.食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3﹣对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下: ![]() +CO
+CO ![]()

![]() B
B ![]()

![]() E
E
已知:HCHO+CH3CHO ![]() CH2═CHCHO+H2O
CH2═CHCHO+H2O
(1)A中官能团的名称为 , A分子中核磁共振氢谱各峰值比为
(2)物质B的结构简式为 , 生成E的反应类型为
(3)试剂C可选用下列中的 . a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(4)![]() 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为 .
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为 .
(5)遇FeCl3溶液呈紫色,且苯环上有两个取代基的A的同分异构体有种,E在一定条件下可以生成高聚物F,F的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl26H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3 , 还含少量Fe2O3、Al2O3、MnO等)制取CoCl26H2O的工艺流程如图1: 
已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCI26H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式: .
(2)写出NaClO3发生反应的主要离子方程式:;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式: .
(3)惰性电极电解CoCl2溶液的阳极电极反应式为 . (注:横坐标依次为1﹣6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是、和过滤.制得的CoCl26H2O在烘干时需减压烘干的原因是 .
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是 , 其使用的最佳pH范围是 A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl26H2O的质量分数大于100%,其原因可能是 . (答一条即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面均是正丁烷与氧气反应的热化学方程式(25℃、101kPa):
①C4H10(g)+ ![]() O2(g)═4CO2(g)+5H2O(l);△H=﹣2 878kJmol﹣1
O2(g)═4CO2(g)+5H2O(l);△H=﹣2 878kJmol﹣1
②C4H10(g)+ ![]() O2(g)═4CO2(g)+5H2O(g);△H=﹣2 658kJmol﹣1
O2(g)═4CO2(g)+5H2O(g);△H=﹣2 658kJmol﹣1
③C4H10(g)+ ![]() O2(g)═4CO(g)+5H2O(l);△H=﹣1 746kJmol﹣1
O2(g)═4CO(g)+5H2O(l);△H=﹣1 746kJmol﹣1
④C4H10(g)+ ![]() O2(g)═4CO(g)+5H2O(g);△H=﹣1 526kJmol﹣1
O2(g)═4CO(g)+5H2O(g);△H=﹣1 526kJmol﹣1
由此判断,正丁烷的燃烧热为( )
A.﹣2878 kJ/mol
B.﹣2 658kJ/mol
C.﹣1746 kJ/mol
D.﹣1526 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com