
【题目】元素性质随原子序数的递增呈周期性变化的实质是( )
A. 元素的相对原子质量增大,量变引起质变
B. 原子的电子层数增多
C. 原子核外电子排布呈周期性变化
D. 原子半径呈周期性变化
科目:高中化学 来源: 题型:
【题目】《天工开物》中对“海水盐”有如下描述:“凡煎盐锅古谓之牢盆……其下列灶燃薪,多者十二三眼,少者七八眼,共煎此盘……火燃釜底,滚沸延及成盐。”文中涉及的操作是( )
A.萃取B.结晶
C.蒸馏D.过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体体积的大小与许多因素有关.当温度和压强相同时,气体体积主要取决于
A.气体的物质的量 B.气体分子之间的平均距离
C.气体分子本身的大小 D.气体的种类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示: 
(1)该图中有两处仪器未画出,它们是、 .
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式为(中和热数值为57.3kJ/mol) .
(3)取55mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表.
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm2 , 中和后生成溶液的比热容c=4.08J/(g℃).则中和热△H=(取小数点后一位).
(4)有关中和热测定实验,下列说法错误的是 a.用温度计测定NaOH溶液起始温度后马上直接测定H2SO4溶液的温度会导致中和热数值比57.3低
b.温度计的冲洗液应倒入小烧杯参与反应
c.混合硫酸和氢氧化钠溶液时应分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.若装置完全相同,操作均没失误,取110mLNaOH溶液和50mL硫酸溶液进行实验,误差比55mLNaOH溶液和25mL硫酸溶液进行实验误差小.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或叙述正确的是( )
A.1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ?mol﹣1
B.12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=﹣110.5 kJ?mol﹣1
C.已知:H2(g)+ ![]() O2(g)═H2O(l)△H=﹣286 kJ?mol﹣1 , 则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ?mol﹣1
O2(g)═H2O(l)△H=﹣286 kJ?mol﹣1 , 则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ?mol﹣1
D.已知N2(g)+3H2(g)?2NH3(g)△H=﹣92.4 kJ?mol﹣1 , 则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。它与二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
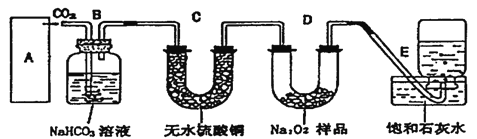
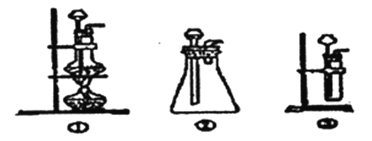
(l)A中制取CO2的装置,应从下列图①、②、③中选哪个图:_____。
B装置的作用是________, C装置内可能出现的现象是________。为了检验E中收集到的气体,在取出集气瓶后,用________的木条伸入集气瓶内,木条会出现________。
(2)若E中的石灰水出现轻微白色浑浊,请说明原因:________。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?________。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(答大或小),相差约________mL(取整数值,所用数据均在标准状况下测定),这是由于________。
(5)你认为上述A~E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项:________。(用甲、乙、丙、丁回答)
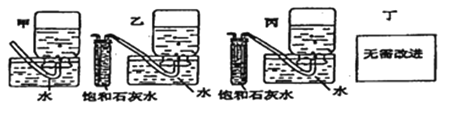
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com