
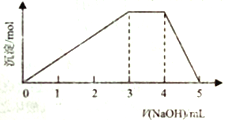
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,它们占据三个周期。Y原子最外层电子数是电子层数的3倍。同由W、X、Z和SO42-组成一种离子化合物的水溶液中滴加稀氢氧化钠溶液,产生沉淀与加入的氢氧化钠溶液的体积关系如图所示。下列说法正确的是
A. X、Y两种元素的非金属性强,其单质化学性质也很活泼
B. Z与X、Y形成的常见盐的水溶液会使蓝色石蕊试纸变红
C. Z的最高价氧化物对应的水化物可溶于X的最简单氢化物的水溶液中
D. 由W、X、Y三种元素只能组成一种盐
【答案】B
【解析】短周期主族元素W、X、Y、Z的原子序数依次增大,它们占据三个周期,则W应为H元素;Y原子最外层电子数是电子层数的3倍,则Y原子核外应有两个电子层,最外层电子数为6,所以Y为O元素;X为第二周期元素、Z为第三周期元素;又根据由W、X、Z和SO42-组成一种离子化合物的水溶液中滴加稀氢氧化钠溶液,产生沉淀与加入的氢氧化钠溶液的体积关系图可得,Z为Al元素、X为N元素,由W、X、Z和SO42-组成离子化合物为:NH4Al(SO4)2。
A项,X(N)、Y(O)两种元素的非金属性强,但其单质化学性质:O2和O3性质活泼、N2性质稳定,故A错误;B项,Z(Al)与X(N)、Y(O)形成的常见盐为Al(NO3)3,属于强酸弱碱盐,其水溶液显酸性,会使蓝色石蕊试纸变红,故B正确;C项,Z(Al)的最高价氧化物对应的水化物为Al(OH)3,X(N)的最简单氢化物为NH3,溶于水得到NH3H2O,是弱碱,与Al(OH)3不反应,故C错误;D项,由W(H)、X(N)、Y(O)三种元素可组成的盐不只一种,如NH4NO3、NH4NO2等,故D错误。


科目:高中化学 来源: 题型:
【题目】如图为配制480 mL 0.2 mol·L-1 NaCl溶液的示意图。

回答下列问题:
(1)在容量瓶的使用方法中,下列操作不正确的是________(填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用胶头滴管滴加蒸馏水到刻度线
D.溶解过程中,要等烧杯中溶液冷却到室温再转入容量瓶
(2)①中应称NaCl________ g;②选择容量瓶的规格____________。
(3)玻璃棒在②、③两步中的作用分别是____________________________、____________________________。
(4)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.某同学在第①步称量时物品和砝码放反了 ________。
B.某同学在第⑧步观察液面时仰视________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.含离子键的化合物是离子化合物,含共价键的化合物是共价化合物
B.离子键的形成过程中一定有电子得失
C.第ⅠA、ⅡA族元素与第ⅥA、ⅦA族元素一定形成离子键
D.离子键与共价键的本质都是静电作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙酸是弱酸的实验事实是
A. CH3COOH溶液与Zn反应放出H2
B. 0.1 mol·L-1 CH3COONa溶液的pH大于7
C. CH3COOH溶液与Na2CO3反应生成CO2
D. 0.1 mol·L-1 CH3COOH溶液可使紫色石蕊变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某离子晶体晶胞如图所示,其摩尔质量为M,阿伏加德罗常数为NA,晶体的密度为d g/cm3。下列说法中正确的是( )

A. 晶体晶胞中阴、阳离子的个数都为1
B. 其中阴、阳离子的配位数都是4
C. 该晶胞可能是NaCl的晶胞
D. 该晶体中两个距离最近的阳离子的核间距为![]() cm
cm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3p轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D的电负性由小到大的顺序为________________。
(2)C的最高价氧化物分子是________(填“极性”或“非极性”)分子。
(3)与B同主族元素X,其气态氢化物是同主族元素的氢化物中沸点最高的,解释X的气态氢化物极易溶于水的原因:①_______________②_______________
(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断E(CO)5的晶体类型为____;E(CO)5在一定条件下发生分解反应:E(CO)5===E(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是________________。
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞如图所示。
体心立方晶胞和面心立方晶胞中E原子的配位数之比为________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运动员无论是在比赛或者是训练时都是需要大量的体力消耗,需比较快地补充能量,可以饮用葡萄糖水。则葡萄糖在人体内发生的主要反应是( )
A.酯化反应B.氧化反应C.还原反应D.水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com