
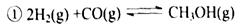


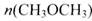 =_________mol。
=_________mol。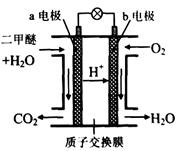
 CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol
CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol。
CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol。 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)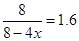


科目:高中化学 来源:不详 题型:单选题
| A.钢铁发生电化学腐蚀的正极反应式为:Fe-2e-=Fe2+ |
| B.氢氧燃料电池的负极反应式为:O2+2H2O+4e-=4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2PbSO4+2H2O
2PbSO4+2H2O| A.充电时阴极反应为:Pb + SO42- -2e- =PbSO4 |
| B.放电时,当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为1mol |
| C.放电时溶液中H+向负极移动 |
| D.充电时阳极附近溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
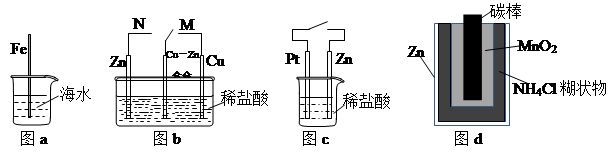
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由连接M改为连接N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Pt上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化性引起的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
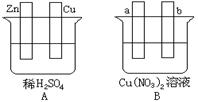
| A.铜片作原电池的负极,碳棒作原电池的正极,氯化锌作电解质溶液 |
| B.铜锌合金在潮湿空气中发生电化学腐蚀 |
| C.用锌片作阴、阳电极,电解硫酸铜溶液 |
| D.用铜片作阴、阳电极,电解硫酸锌溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com