
��16�֣�ZnO�ǵ�ơ�Ϳ�ϡ��л��ϳɵȻ�ѧ��ҵ����Ҫԭ�ϡ�ij����������ɺ�п��ҵ���ϣ���Fe��Cu��Mn�����ʣ�����ZnO�Ĺ����������£�

��֪������������pHΪ1.5���¶�Ϊ90��ʱ��ȫ�����������ڹ��ˡ�
2Cu +O2 +2H2SO4 == 2CuSO4+2H2O
��1������ٵĽ�ȡҺ�������Zn2+��Mn2+���⣬�����еĽ��������� �� �������Լ�XΪNa2SO4��_________�Ļ��Һ��
��2������ڿɽ�һ��������������������ȥ��Mn2+����д����Ӧ�ij�ȥMn2+�����ӷ���ʽ_________________________������ۼ�����Լ���_______���������������п���ѭ��ʹ�õ��Լ���_____________��
��3��������м�������Ƿ�ϴ�Ӹɾ��IJ���������____________________________��
��4�������̼��ʵ�ʵõ�����һ�ּ�ʽ̼��п[ZnCO3��xZn(OH)2��yH2O]��ȡ����Ʒ7.18 g��������պ��ò���������Ϊ4.86 g������������ͨ����������ʯ��ˮ�У��õ�2.00 g��������˼�ʽ̼��п�Ļ�ѧʽ��________________��
��16�֣�
��1��Fe3+��Cu2+��2�֣�, H2SO4��2�֣�
��2��Mn2++H2O2+H2O==MnO(OH)2��+2H+��3�֣�, Zn��2�֣���Na2SO4��2�֣�
��3��ȡ���һ��ϴ����Һ1~2mL���Թ��У������еμ�BaCl2��Һ�����ް�ɫ�������ɣ��������ϴ�Ӹɾ����𰸺������ɣ���2�֣�
��4��ZnCO3��2Zn(OH)2��2H2O��Zn3(OH)4CO3��2H2O��3�֣�
��������
����������������̷������Լ�X�к������ᣬFe�����ᷴӦ������������������������Ϊ�����ӣ��������������Ʒ�Ӧ���ɻ���������������ȥ��Cu�����ᡢ������Ӧ��������ͭ��Mn�����ᷴӦ���������̣����������������������Һ��pH��ʹMnԪ��ת��ΪMnO(OH)2��ʣ�������ӻ���ת��Ϊ���������������ټ������Zn�ۣ�����ͭ���ӷ����û���Ӧ���ɵ���Cu���Ӷ���ȥͭ���ӣ�������̼���ƺ�õ�̼��п���������պ�õ�ZnO��
��1���������Ϸ���������ٵĽ�ȡҺ�������Zn2+��Mn2+���⣬�����еĽ���������Fe3+��Cu2+�������Լ�XΪNa2SO4��H2SO4�Ļ��Һ��
��2����������������ⷴӦ����MnO(OH)2���������ӣ����ӷ���ʽMn2++H2O2+H2O==MnO(OH)2��+2H+������ۼ�����Լ���Zn���ʣ���ͭ���ӷ����û���Ӧ������п��Һ�м���̼���ƺ�����̼��п�������ƣ������̿�ʼʱ�����������ƣ������������������п���ѭ��ʹ�õ��Լ���Na2SO4��
��3�����ɵ�̼��п�����п��ܺ�����������ӣ����Լ�������Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ����Һ1~2mL���Թ��У������еμ�BaCl2��Һ�����ް�ɫ�������ɣ��������ϴ�Ӹɾ���
��4���������⣬���յõ���ZnO�����ʵ�����4.86g/81g/mol=0.06mol��2.00g����Ϊ̼��ƣ��������ɶ�����̼�����ʵ�����2.00g/100g/mol=0.02mol��ZnCO3��xZn(OH)2��yH2O ��x+1��ZnO+CO2��+(x+y)H2O��������ˮ�����ʵ����ǣ�7.18g-4.86g-0.02mol��44g/mol��/18g/mol=0.08mol������ZnO��CO2��H2O�����ʵ�������0.06:0.02:0.08=3:1:4=��x+1��:1����x+y�������x=2,y-2����˼�ʽ̼��п�Ļ�ѧʽ��ZnCO3��2Zn(OH)2��2H2O��Zn3(OH)4CO3��2H2O��
��x+1��ZnO+CO2��+(x+y)H2O��������ˮ�����ʵ����ǣ�7.18g-4.86g-0.02mol��44g/mol��/18g/mol=0.08mol������ZnO��CO2��H2O�����ʵ�������0.06:0.02:0.08=3:1:4=��x+1��:1����x+y�������x=2,y-2����˼�ʽ̼��п�Ļ�ѧʽ��ZnCO3��2Zn(OH)2��2H2O��Zn3(OH)4CO3��2H2O��
���㣺���鹤�����̵ķ��������ʻ�ѧʽ�ļ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��������ε��п��Ի�ѧ�Ծ��������棩 ���ͣ������
(14��)ij��ѧС��ͨ���������ϣ����������ͼ��ʾ�ķ����Ժ����ϴ���Ϊԭ�����Ʊ�NiSO4����֪ij�������ĺ����ϴ�����Ҫ����Ni��������Al(31��)��Fe(1��3��)�ĵ��ʼ������������������(3.3��)��

����������������������ʽ����ʱ��pH���£�

��1��������������з�����Ӧ�����ӷ���ʽ��
��2���������ʱ����������� (�ѧʽ)��
��3������H2O2ʱ������Ӧ�����ӷ���ʽΪ
��4������bΪ������Һ��pH������ΪpH�ĵ��ط�Χ��
��5����Ʒ��������ʱ����������̷�(FeS04��7H20)����ԭ������� (д��һ�㼴��)��
��6��NiS04��7H20�������Ʊ�������(NiMH)��������Ŀǰ�Ѿ���Ϊ��϶���������һ����Ҫ������͡�NiMH�е�M��ʾ���������Ͻ𡣸õ���ڳ��������ܷ�Ӧ�Ļ�ѧ����ʽ��Ni(OH)2+M=NiOOH+MH����NiMH��طŵ�����У������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�������Һ�еķ�Ӧ�����ܷ�Ӧ�����Ķ��٣���ֻ����ͬһ�����ӷ���ʽ����ʾ����
A��NaHCO3��Ca (OH)2 B��Ba(OH)2��H2SO4
C��HCl��NaAlO2 D��AlCl3��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ�Ϫ�ظ����ڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ӷ���ʽ��д��ȷ����
A��Fe(NO3)3��Һ�м���������HI��Һ��2Fe3��+2I����2Fe2��+I2
B����Mg(HCO3)2��Һ�м������NaOH��Һ��Mg2++2HCO3��+4OH����Mg(OH)2��+2CO32��+2H2O
C���ö��Ե缫��ⱥ��ʳ��ˮ��2Cl��+2H+ H2��+Cl2��
H2��+Cl2��
D��������Һ��ͨ��������CO2��2C6H5O��-+CO2 +H2O��2C6H5OH+CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ�Ϫ�ظ����ڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ʵ��װ��ͼ���е���Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���

A����ͼ1װ������һ�����ʵ���Ũ�ȵ�ϡ����
B����ͼ2װ�ÿ�̽������������ʴ
C����ͼ3װ�ÿ���ȡ����������
D����ͼ4װ�ÿ�˵��Ũ���������ˮ�ԡ�ǿ�����ԣ�SO2����Ư���ԡ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ������У���˸�����ѧ��3���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ������ǻ�ѧʵ�����Ҫ����֮һ��������װ�ã��г�װ��ʡ�ԣ�������ʵ�飬�������ѡ����

A��ͼ����KMnO4��Һ�Ϻ�ɫ��ȥ��˵��SO2����Ư����
B��ͼ���ܹ���ͭпԭ���
C��ͼ�������ſ������ռ�������̼
D��ͼ�ܼ��װ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ������ѧ�ڳ������ۻ�ѧ�Ծ��������棩 ���ͣ������
���ᣨH2C2O4����Һ������KMnO4��Һ��Ӧʱ����Һ��ɫ����������죬ijѧϰС��̽����Ӧ������ʹ��ɫ�ӿ����Ҫԭ��������:
���������ϡ�KMnO4��Һ����H2C2O4�ķ�Ӧ����Ϊ��
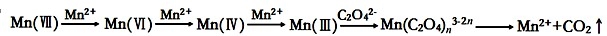
��������衿����1:�÷�ӦΪ���ȷ�Ӧ
����2:��Ӧ���ɵ�Mn2���Ը÷�Ӧ�д�����
����3:K+�Ը÷�Ӧ�д�����
��С��ͬѧδ���Ũ��ʹ��Ӧ���ʼӿ�ļ��裬ԭ���� ��
����ơ����ʵ�顿
��1����ȡ g���ᾧ�壨H2C2O4��2H2O��������500mL 0.10mol/L H2C2O4��Һ��
�������������б����õ���2�ֶ���������������ƽ�� ��
�����в�����ʹ������ҺŨ��ƫ�͵��� (������ѡ�����ĸ��ţ���
A����ȡ���ᾧ��ʱ�������ᾧ�����������ƽ����
B������ʱ���ӿ̶���
C�����ձ�����Һת�Ƶ�����ƿ֮ǰ������ƿ������������ˮ
D��ҡ�Ⱥ�����ҺҺ����ڿ̶��ߣ������ý�ͷ�ιܼ�ˮ�ٶ���
��2�����̽������¼����
ʵ�� ��� | �ձ��������Լ���������mL�� | �������� | ��Һ��ɫʱ�� (s) | |||
0.10mol/L H2C2O4��Һ | ��Ũ�� KMnO4��Һ | H2O | 0.50mol/L ϡ���� | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | ˮԡ�����¶�65�� | 15 |
3 | 30 | 20 | 30 | 20 | ��������MnSO4���� | 3.6 |
4 | 30 | 20 | x | 20 | ����5mL 0.10mol/L K2SO4��Һ | 18 |
��x = ������2������
��3������KMnO4������ˮ���л�������أ�Ϊ���ƺ��ȶ���KMnO4��Һ����Ũ����궨��ȡ10.00 mL 0.10mol/L H2C2O4��Һ����ƿ�У�����10mL 0.50mol/L ϡ���ᣬ�ã�2����KMnO4��Һ�ζ�����ƿ��ǡ�ó�dz��ɫ���Ұ���Ӳ���ɫ����¼���ݣ�ƽ������ʵ�飬ƽ������KMnO4��Һ4
ϡ���ᣬ�ã�2����KMnO4��Һ�ζ�����ƿ��ǡ�ó�dz��ɫ���Ұ���Ӳ���ɫ����¼���ݣ�ƽ������ʵ�飬ƽ������KMnO4��Һ4 0.00 mL���������Һ������KMnO4��Һ��Ӧ�����ӷ���
0.00 mL���������Һ������KMnO4��Һ��Ӧ�����ӷ��� ʽΪ�� ������ʵ����KMnO4��Һ�����ʵ���Ũ��Ϊ ��
ʽΪ�� ������ʵ����KMnO4��Һ�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���йظ�������ĸ���������ȷ����
�����������ﲻһ���Ƿǽ���������
�ڷǽ���������϶�������������
�ۼ���������϶��ǽ���������
�ܽ���������϶��Ǻ���������
�����������������ˮ��Ӧ������Ӧ����
����ˮ��Ӧ������������ﲻһ���������������ˮ��Ӧ���ɼ�������ﲻһ���Ǽ�ס������
�߲��ܸ��ᷴӦ��������һ���ܸ��Ӧ
A���٢ۢ� B���٢ڢݢ� C���ۢܢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ұһ�е���У����Ԫ�µ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A�������£���pH=3�Ĵ�����Һϡ�͵�ԭ�����10����ϡ�ͺ���Һ��pH=4
B��25��ʱKsp(AgCl)=1.8��10��10����AgCl�������ܽ�ƽ����ϵ�м���NaCl���壬AgCl���ܽ�ȿ�������
C��Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ��pH�ɴ�С������˳��Ϊ��NaOH>Na2CO3>(NH4)2SO4>NaHSO4
D��Ϊȷ��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH >7����H2A�������pH<7����H2A��ǿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com