
(1) 已知在一定条件下的反应4HCl+O2=2Cl2 +2H2O中, 有4mol HCl被氧化时,放出120kJ的热量,且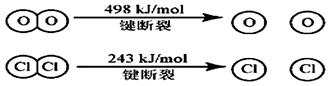
则断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差为__________KJ。
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
(1)33
(2)MgO> CaO> NaCl > KCl (3) B、D、E(漏一个扣1分,错选0分)
(4)SP3 K2CuCl3
解析试题分析:(1)△H=断裂化学键吸收的能量-形成化学键放出的能量=4×x kJ/mol+498k
J/mol-2×243kJ/mol-2×2×y kJ/mol=-120kJ/mol,解得y-x=33kJ/mol。
(2)离子半径Mg2+<Na+<O2-<Ca2+<Cl-;离子电荷数Na+=Cl-<O2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl。
(3)已知AlCl3熔点190℃,沸点183℃,这说明氯化铝的熔沸点很低,所以形成的晶体类型是分子晶体,根据结构可知,分子中含有的作用力有共价键、配位健和分子间作用力,答案选BDE。
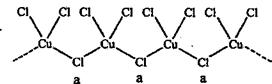
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,所以杂化轨道类型为sp3。一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,CuCl3原子团的化合价为-2,其化学式为:K2CuCl3。
考点:考查反应热、晶格能、微粒间作用力以及杂化轨道类型的有关判断和计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。


科目:高中化学 来源: 题型:阅读理解
 Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)| 浓H2SO4 |
| △ |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出有机物在有氧气条件下转化为无机物的化学方程式_________________________。
(2)这条河水的生化需氧量为_______________________________________。
(3)这条河中的鱼类____________(填“能”或“不能”)维持生命。
查看答案和解析>>
科目:高中化学 来源:2014届江西省景德镇市高三一检化学试卷(解析版) 题型:填空题
Ⅰ.恒温,容积为1
L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示(已知:2SO2(g)+O2(g) 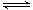 2SO3(g)
ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g)
ΔH=-196.6 kJ·mol-1),请回答下列问题:
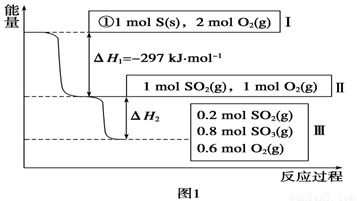
(1)写出能表示硫的燃烧热的热化学方程式:______________________。
(2)ΔH2=__________kJ·mol-1。
Ⅱ.工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:
CH3COOH(l)+C2H5OH(l)
 CH3COOC2H5(l)+H2O(l) ΔH=-8.62 kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-8.62 kJ·mol-1
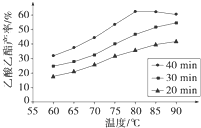
已知CH3COOH、C2H5OH和CH3COOC2H5的沸点依次为118 ℃、78 ℃和77 ℃。在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示。
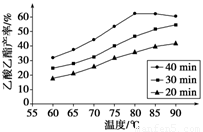
(1)该研究小组的实验目的是___________________________________。
(2)60 ℃下反应40 min与70 ℃下反应20 min相比,前者的平均反应速率________后者(填“小于”、“等于”或“大于”)。
(3)如图所示,反应时间为40 min、温度超过80 ℃时,乙酸乙酯产率下降的原因可能是_________________________________(写出两条)。
Ⅲ.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) 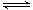 H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
800 |
|
平衡常数K |
9.94 |
9 |
1 |
试回答下列问题:
(1)在800 ℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有________(选填“A、B、C、D、E”)。
n(CO) n(H2O) n(H2) n(CO2)
A 1 5 2 3
B 2 2 1 1
C 3 3 0 0
D 0.5 2 1 1
E 3 1 2 1
(2)已知在一定温度下,C(s)+CO2(g) 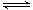 2CO(g)平衡常数为K;
2CO(g)平衡常数为K;
①C(s)+H2O(g) 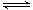 CO(g)+H2(g) 平衡常数为K1;
CO(g)+H2(g) 平衡常数为K1;
②CO(g)+H2O(g) 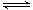 H2(g)+CO2(g) 平衡常数为K2;
H2(g)+CO2(g) 平衡常数为K2;
则K、K1、K2之间的关系是______________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省清远市高三上学期期末检测理综化学试卷(解析版) 题型:计算题
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g)
2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l) H2O(g)
△H=+ 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
(2)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。

①在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂。
②能判断该反应在“图2”所在条件下是否已达化学平衡状态的依据是 。(双选)
A.容器中压强不变 B.体系的密度不随时间改变
C.v正(H2)=2v逆(CH3OH) D.CO与H2的物质的量的比不随时间改变
③计算该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数K=
。
CH3OH(g)的化学平衡常数K=
。
④请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(3)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6。现将c mol·L-1 CaCl2溶液与2.00×10-2 mol·L-1 Na2SO4溶液等体积混合生成沉淀,则c的最小值是 (结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源:江西省2010届高三适应考试2理综化学 题型:实验题
(16分)、据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中间产物,其合成路线为:

 已知: 一定条件(Ⅰ)RNH2+
已知: 一定条件(Ⅰ)RNH2+ CH2Cl →
RNHCH2
CH2Cl →
RNHCH2 +HCl(R和
+HCl(R和 代表烃基);
代表烃基);
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ) (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)
(Ⅳ)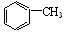 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
回答下列问题:
(1)C的结构简式是 。
(2)请写出D+E→F的化学方程式: 。
(3)E在一定条件下,可聚合成很好的功能高分子材料,写出合成此高聚物的化学方程式 。
(4)反应①~⑤中,属于取代反应的是(填反应序号)
(5)符合下列条件的E的同分异构体的数目是( )。
①与FeCl3溶液有显色反应 ②能发生银镜反应 ③苯环上的一溴取代物只有3种。
A、3种 B、8种 C、10种 D、12种
(6) 已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45~50%),反应方程式如下:
C6H5CHO + (CH3CO)2O → C6H5CH=CHCOOH +CH3COOH
苯甲醛 肉桂酸
若苯甲醛的苯环上有取代基,也能发生Perkin反应,相应产物的产率如下:
|
反应物
|
|
|
|
|
|
产率(%) |
15 |
23 |
33 |
0 |
|
反应物
|
|
|
|
|
|
产率(%) |
71 |
63 |
52 |
82 |
请根据上表回答:取代基对Perkin反应的影响有(写出3条即可):
①
②
③ [来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com