
����Ŀ�������ε�ϡ��Һ��amol��L-1NaX��Һ��bmol��L-1NaY��Һ������˵������ȷ���ǣ� ��
A.��a=b����pH(NaX)>pH(NaY)��������HX<HY
B.��a>b����c(X-)=c(Y-)������Һ��c(HX)>c(HY)
C.��a=b����c(X-)=c(Y-)+c(HY)����HXΪǿ��
D.������Һ�������Ϻ�c(X-)+c(HX)=c(Y-)+c(HY)=0.1mol��L-1����a=b=0.1mol��L-1
���𰸡�D
��������
![]() ������ҺŨ����ͬ��
������ҺŨ����ͬ��![]() ��˵��NaX�ļ��Ը�ǿ����Ӧ��
��˵��NaX�ļ��Ը�ǿ����Ӧ��![]() ��ˮ��̶ȸ�ǿ���������
��ˮ��̶ȸ�ǿ���������![]() ����A��ȷ��
����A��ȷ��
B.![]() ����
����![]() �����������غ�
�����������غ�![]() ��
��![]() ��������Һ��
��������Һ��![]() ����B��ȷ��
����B��ȷ��
C.![]() ��
��![]() ����˿��Կ���
����˿��Կ���![]() û��ˮ�⣬���HXΪǿ�ᣬ��C��ȷ��
û��ˮ�⣬���HXΪǿ�ᣬ��C��ȷ��
D.������Һ�����ǰ�����������غ�![]() ��
��![]() �����������ϣ����Ϻ������ǻ��ǰ����������ʱc��X-��+c��HX��=
�����������ϣ����Ϻ������ǻ��ǰ����������ʱc��X-��+c��HX��=![]() ��c��Y-��+c��HY��=
��c��Y-��+c��HY��=![]() ������Ϊc��X-��+c��HX��=c��Y-��+c��HY��=0.1mol/L����a=b=0.2����D����
������Ϊc��X-��+c��HX��=c��Y-��+c��HY��=0.1mol/L����a=b=0.2����D����
��ѡ��D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G�Ǻϳ�ij�����Ⱦۺ���ĵ��壬��ϳɷ������£�
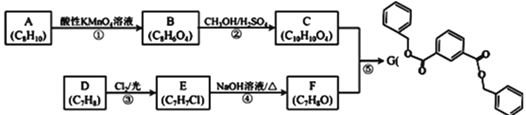
��֪��R1COOR2+R3OH![]() R1COOR3+R2OH
R1COOR3+R2OH
![]() �к��������ŵ������� ______ ��F�������� ______ ��
�к��������ŵ������� ______ ��F�������� ______ ��
![]() ���������е�ȡ����Ӧ��
���������е�ȡ����Ӧ��![]() ��
��![]() ��� ______
��� ______ ![]() �����
�����![]() ��������E�ĺ˴Ź�������ͼ�й��� ______ �����շ壬�������Ϊ ______ ��
��������E�ĺ˴Ź�������ͼ�й��� ______ �����շ壬�������Ϊ ______ ��
![]() �����кϳ�·�߿ɵõ�F��ͬ���칹��H����ɼ���H��F���Լ��� ______ ��
�����кϳ�·�߿ɵõ�F��ͬ���칹��H����ɼ���H��F���Լ��� ______ ��
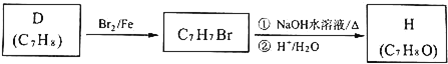
![]() ��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ______ ��
��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ______ ��
![]() ��ͬ���칹��K�����������ʣ�
��ͬ���칹��K�����������ʣ�![]() ����NaOH��Һ��Ӧ����1molK��ȫ��Ӧ����4molNaOH
����NaOH��Һ��Ӧ����1molK��ȫ��Ӧ����4molNaOH![]() �ܷ���������Ӧ����1molK��������������Һ��Ӧ����4molAg
�ܷ���������Ӧ����1molK��������������Һ��Ӧ����4molAg![]() �����б����ϵ�һ��ȡ����ֻ��һ�֡���K�Ľṹ��ʽΪ ______ ��
�����б����ϵ�һ��ȡ����ֻ��һ�֡���K�Ľṹ��ʽΪ ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
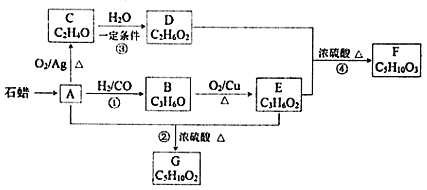
����Ŀ����֪A��![]() ��CO�γ�B��B�ܷ���������Ӧ��C������ֻ��һ���⣬�������ת����ϵ����
��CO�γ�B��B�ܷ���������Ӧ��C������ֻ��һ���⣬�������ת����ϵ����![]() ������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ����
������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ����![]() ��
��
��ش�
![]() �л���C�Ľṹ��ʽ��______����Ӧ�ڵķ�Ӧ������______��
�л���C�Ľṹ��ʽ��______����Ӧ�ڵķ�Ӧ������______��
![]() д��һ�������·�����Ӧ�ٵĻ�ѧ����ʽ______��
д��һ�������·�����Ӧ�ٵĻ�ѧ����ʽ______��
![]() ����˵������ȷ����______
����˵������ȷ����______![]() ����ĸ
����ĸ![]() ��
��
A.������A������
B.������D�������ֹ�����
C.�ý�������������F��G
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɵ����������ϳɰ����ķ��������1918��ŵ������ѧ����
N2+3H2![]() 2NH3
2NH3
����һ�ܱ������г���1 mol N2��3 mol H2����һ��������ʹ�÷�Ӧ�����������й�˵����ȷ���ǣ� ��
A.�ﵽ��ѧƽ��ʱ��N2����ȫת��ΪNH3
B.�ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ��һ�����
C.�ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯
D.�ﵽ��ѧƽ��ʱ������Ӧ���淴Ӧ�����ʶ�Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ�������й���C2H2(g)��![]() O2(g)=2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵����ȷ����(����)
O2(g)=2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵����ȷ����(����)
A.��10NA������ת��ʱ������1300 kJ����
B.��8NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ����
C.��NA��ˮ����������ΪҺ��ʱ������1300 kJ����
D.��2NA��̼��˫������ʱ���ų�1300 kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵؿ��еĺ����ϸߡ��輰�仯����Ŀ��������Ѿã����ִ��������й㷺Ӧ�á��ش��������⣺
��1��1810����仯ѧ�ұ�������˹�ڼ���ʯӢɰ��ľ̿����ʱ���õ�һ������������������������������_______��
��2���մɡ�ˮ��Ͳ����dz��õĹ����β��ϡ����У�������ͨ��������Ҫԭ����_______��
��3���ߴ������ִ���Ϣ���뵼��������Ȳ�ҵ����Ҫ�Ļ������ϡ���ҵ���ᴿ���ж���·�ߣ�����һ�ֹ�������ʾ��ͼ����Ҫ��Ӧ���£�
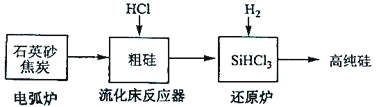
��������Ҫ��Ӧ | |
�绡¯ | SiO2+2C |
��������Ӧ�� | Si+3HCl |
��ԭ¯ | SiHCl3+H2 |
����ʯӢɰ�ͽ�̿�ڵ绡¯�и��¼���Ҳ��������̼���裬�÷�Ӧ�Ļ�ѧ����ʽΪ_______��̼�����ֳ�_______���侧��ṹ��_______���ơ�
������������Ӧ�IJ����У�SiHCl3��Լռ85%������SiCl4��SiH2Cl2��SiH3Cl�ȣ��й����ʵķе��������±����ᴿSiHCl3����Ҫ���ղ��������dz�����������_______��
���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
�е�/�� | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
��SiHCl3����ˮ�⣬����ȫˮ��IJ���Ϊ_______��
��4���ȼҵ��Ϊ�������������ṩ����ԭ�ϣ���Щԭ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����(H2C2O4)��һ�ֶ�Ԫ���ᣬ���ἰ���ι㷺����ҽҩ��ӡȾ�����ϵȹ�ҵ��
��1����֪25��ʱ�����ֳ��������Ka���±���ʾ��
����� | H2C2O4 | CH3COOH | HCN | H2CO3 |
���볣��(mol��L-1) | K1=5.6��10-2 K2=5.4��10-3 | K1=1.7��10-5 | K2=6.2��10-10 | K1=4.2��10-7 K2=5.6��10-11 |
��25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L-1��Na2C2O4��CH3COONa��NaCN��Na2CO3��pH�ɴ�С��˳����___���к͵��������pH��HCOOH��HCN����NaOH����___(����ǰ�ߴ��������ߴ������������)��
�����й���0.1mol��L-1NaHC2O4��Һ��˵����ȷ����___��
a.HC2O4-�ĵ���̶ȴ���ˮ��̶ȣ���Һ������
b.HC2O4-��ˮ��̶ȴ��ڵ���̶ȳ̶ȣ���Һ�Լ���
c.��Һ��c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.��Һ��c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
��2����t��ʱ��MgC2O4��ˮ�еij����ܽ�ƽ��������ͼ1��ʾ����֪t��ʱMg(OH)2��Ksp=5.6��10-12������˵������ȷ����____
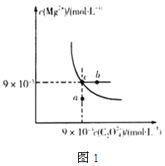
A.��t��ʱ��MgC2O4��Ksp=8.1��10-5mol2��L-2
B.��MgC2O4������Һ�м���Na2CO3���壬��ʹ��Һ��c�㵽b��
C.ͼ��a���Ӧ����MgC2O4�IJ�������Һ
D.��t��ʱ��MgC2O4(s)+2OH-(aq)Mg(OH)2(s)+C2O42-(aq)ƽ�ⳣ��K=![]()
��3��������������(FeC2O4��2H2O)��һ��dz��ɫ���壬������ˮ�������ֽ⡣ij��ѧ��ȤС�����ʵ����֤�������������ȷֽ�IJ��̽��������ͼ2��
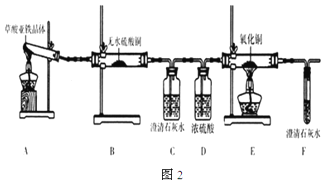
�ٴӻ����Ƕȿ��ǣ�����ʵ��װ�õ�����ȱ����___��
�ڸ���ȤС���������ʵ��ʱ����ʵ�鰲ȫ�Ƕȿ��ǣ�Ӧ�ȵ�ȼ___(����A������E��)���ľƾ��ơ�
����ʵ������й۲쵽B�а�ɫ��ˮCuSO4�����ɫ��___(����ʵ������)�����֤���������������ȷֽ�����������H2O��CO��
��Ϊ̽��������������ֽ�Ĺ�������ȤС��ͬѧȷ��ȡ3.60g������������(FeC2O4��2H2O)����Է���������180)����ּ��ȣ�ʹ����ȫ�ֽ⣬��ȴ��Ƶ�ʣ����������Ϊ1.60g����ʣ�����ֻ��һ�����������ͨ������ȷ����������Ļ�ѧʽΪ___��������������ֽ�Ļ�ѧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������װ���Ʊ�Cl2�����������ʣ�����˵����ȷ���ǣ� ��
A.Iͼ�У����MnO2������Ũ����Ϳ�ȫ��������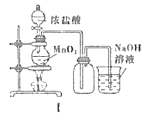
B.IIͼ�У����ű���ʳ��ˮ�ռ�һ�Թ���������ֹ��պ�ˮ������Һ������ǿ����Ͳ��Һ������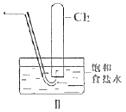
C.IIIͼ�У�������ɫ���̣�������ƿ�м�������ˮ��������Һ�ʻ�ɫ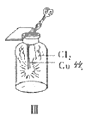
D.IVͼ�У��������ɫ��������ɫ��ʪ�����ɫ��������ɫ��˵��Cl2��Ư����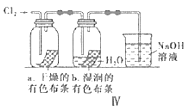
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���Ա���Ϊ��Ҫԭ����ȡ�����ͺͰ�˾ƥ�ֵĹ��̣�
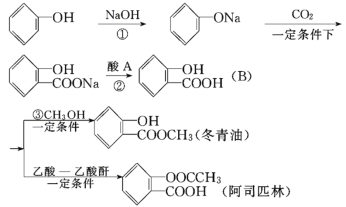
(1) �����ͺ��еĹ���������Ϊ________________
(2)B���ڶ�������ʹ��Ʒ�������������������Լ����ٷ�Һ���ɳ�ȥ_____
(A) NaOH ��Һ (B) Na2CO3��Һ (C) NaHCO3��Һ (D) Na
(3)д����������Ӧ�Ļ�ѧ����ʽ_________________________________.
(4)д����Ӧ�۵Ļ�ѧ����ʽ_____________________________________
(5)1 mol ��˾ƥ��������________ mol �������Ʒ�����Ӧ��
(6)������M�Ƕ����͵�ͬ���칹�壬�붬���;�����ͬ�Ĺ����ţ������Ȼ���������ɫ��Ӧ����������������λ��ȡ������д������M���ܵĽṹ��ʽ____________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com