
【题目】硅在地壳中的含量较高。硅及其化合物的开发由来已久,在现代生活中有广泛应用。回答下列问题:
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”。这种“金属”可能是_______。
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料。其中,生产普通玻璃的主要原料有_______。
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
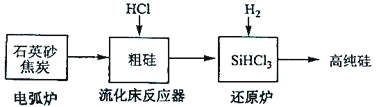
发生的主要反应 | |
电弧炉 | SiO2+2C |
流化床反应器 | Si+3HCl |
还原炉 | SiHCl3+H2 |
①用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为_______;碳化硅又称_______,其晶体结构与_______相似。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和_______。
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
③SiHCl3极易水解,其完全水解的产物为_______。
(4)氯碱工业可为上述工艺生产提供部分原料,这些原料是_______。
【答案】含有硅、碳的铁合金(或硅铁) 石英砂、纯碱和石灰石 SiO2+3C![]() SiC+2CO↑ 金刚砂 金刚石(或单晶硅) 精馏(或蒸馏) H4SiO4(或H2SiO3)、H2、HCl H2、HCl
SiC+2CO↑ 金刚砂 金刚石(或单晶硅) 精馏(或蒸馏) H4SiO4(或H2SiO3)、H2、HCl H2、HCl
【解析】
(1)石英砂是SiO2,在高温下和木炭发生反应:2C+SiO2![]() 2CO↑+Si,然后硅和铁形成合金,或者是硅、铁、过量的碳形成合金;
2CO↑+Si,然后硅和铁形成合金,或者是硅、铁、过量的碳形成合金;
(2)制造普通玻璃的原料:石英砂、石灰石、纯碱,高温下SiO2+CaCO3![]() CaSiO3+CO2,SiO2+Na2CO3
CaSiO3+CO2,SiO2+Na2CO3![]() Na2SiO3+CO2;
Na2SiO3+CO2;
(3)①根据信息,在高温下,C和二氧化硅反应生成硅单质,硅单质再和C反应生成碳化硅,故:3C+SiO2![]() SiC+2CO,碳化硅俗名金刚砂,属于原子晶体,碳和硅属于同一主族,晶体结构与金刚石或晶体硅相似;
SiC+2CO,碳化硅俗名金刚砂,属于原子晶体,碳和硅属于同一主族,晶体结构与金刚石或晶体硅相似;
②沉降、冷凝后成分是:SiHCl3、SiCl4、SiH2Cl2,都是液体,因此采用蒸馏的方法提纯,水解的反应方程式:SiHCl3+H2O=H2SiO3↓+HCl+H2↑,故H2SiO3、H2、HCl;
(4)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,根据发生的主要反应,可以提供H2、HCl。
2NaOH+H2↑+Cl2↑,根据发生的主要反应,可以提供H2、HCl。


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】有机合成是制药工业中的重要手段。G是某抗炎症药物的中间体,其合成路线如图:
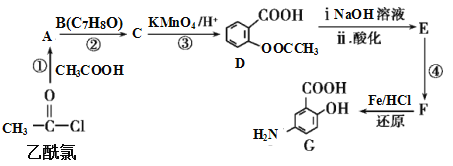
已知:
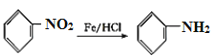
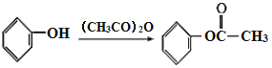 ,
,
(1)B的结构简式为_____。
(2)反应④的条件为____;①的反应类型为___;反应②的作用是____。
(3)下列对有机物G的性质推测正确的是____(填选项字母)。
A.具有两性,既能与酸反应也能与碱反应
B.能发生消去反应、取代反应和氧化反应
C.能聚合成高分子化合物
D.1mol G与足量NaHCO3溶液反应放出2mol CO2
(4)D与足量的NaOH溶液反应的化学方程式为_____。
(5)符合下列条件的C的同分异构体有___种。
A.属于芳香族化合物,且含有两个甲基 B.能发生银镜反应 C.与FeCl3溶液发生显色反应
其中核磁共振氢谱有4组峰,且峰面积之比为6∶2∶1∶1的是___(写出其中一种的结构简式)。
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的取代基连在苯环的间位。根据题中的信息,写出以甲苯为原料合成有机物![]() 的流程图(无机试剂任选)。_______
的流程图(无机试剂任选)。_______
合成路线流程图示例如图:X![]() Y
Y![]() Z…目标产物
Z…目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一容积为2 L的密闭容器中加入0.6molH2O(g)和0.4molCO,在一定条件下发生如下反应:CO(g) + H2O(g )![]() CO2(g) + H2(g)
CO2(g) + H2(g)
(1)若反应2min后,容器中CO仅剩0.2mol,则0~2min间CO的平均反应速率为___。
(2)该反应为放热反应,若升高温度,化学反应速率___;CO的转化率___。(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式C(s)+H2O(g) ![]() CO(g)+H2(g);△H =+131.3kJ/mol表示( )
CO(g)+H2(g);△H =+131.3kJ/mol表示( )
A. 碳和水反应吸收131.3kJ能量
B. 1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气完全反应生成一氧化碳气体和氢气,并吸热131.3kJ热量
D. 1个固态碳原子和1分子水蒸气反应吸热131.1kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种盐的稀溶液:amol·L-1NaX溶液和bmol·L-1NaY溶液。下列说法不正确的是( )
A.若a=b,且pH(NaX)>pH(NaY),则酸性HX<HY
B.若a>b,且c(X-)=c(Y-),则溶液中c(HX)>c(HY)
C.若a=b,且c(X-)=c(Y-)+c(HY),则HX为强酸
D.若两溶液等体积混合后c(X-)+c(HX)=c(Y-)+c(HY)=0.1mol·L-1,则a=b=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() (环戊二烯)容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )
(环戊二烯)容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )
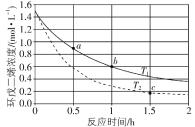
A.T1小于T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol·L-1NaOH溶液滴定10mL0.100mol·L-1H3PO4溶液,曲线如图所示。下列说法正确的是
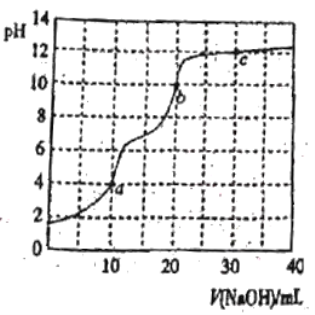
A.滴定终点a可选择酚酞作指示剂
B.c点溶液中c(Na+)>3c(![]() )+2c(
)+2c(![]() )+c(
)+c(![]() )
)
C.b点溶液中c(![]() )>c(
)>c(![]() )>c(
)>c(![]() )
)
D.a、b、c三点中水的电离程度最小的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应aA(g)+bB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是________热反应,且a+b________p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同),正反应速率________。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比c(B)/c(C) 将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
(6)若B是有色物质, A、C均为无色物质,则加入C(体积不变)时混合物的颜色________,而维持容器内气体的压强不变,充入氖气时,混合物的颜色________。(填“变浅”“变深”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:草酸是一种弱酸,草酸晶体(H2C2O4·2H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O。
I.某小组同学配置0.1mol·L-1的草酸溶液480ml并验证草酸的性质
(1)配置该溶液需要草酸晶体___g。(已知H2C2O4·2H2O的相对分子质量为126)
(2)下列操作会使配置溶液的物质的量浓度偏低的是(________)
A.定容时俯视容量瓶刻度线
B.加水时超过刻度线,用胶头滴管吸出
C.转移过程中有少量的溶液溅出
D.称量固体时,砝码放在左盘
E.容量瓶用蒸馏水洗涤干净后没有干燥就移入所配置溶液
F.配置过程中,未用蒸馏水洗涤烧杯和玻璃棒
(3)取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液褪色(MnO4-被还原为Mn2+),反应的离子方程式为___;该反应的反应速率先慢后快的主要原因可能是___。
II.根据草酸晶体的组成,猜想其受热分解产物为CO、CO2和H2O。通过如图装置验证草酸晶体的部分分解产物。
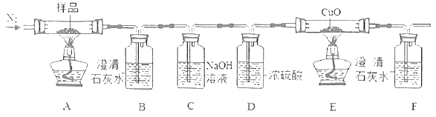
(4)反应开始前通入氮气的目的是___。
(5)B中澄清石灰水变浑浊,并不能证明产物中一定有CO2,理由是___。
(6)E中固体变成红色,F中澄清石灰水变浑浊,说明产物中含有气体___ (填化学式)。
(7)最后可用装置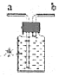 收集多余的CO,气体应从___端进入(选填“a”或“b”)。
收集多余的CO,气体应从___端进入(选填“a”或“b”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com