
【题目】已知草酸(H2C2O4)是一种二元弱酸,草酸及其盐广泛用于医药、印染、塑料等工业。
(1)已知25℃时,几种常见弱酸的Ka如下表所示:
电解质 | H2C2O4 | CH3COOH | HCN | H2CO3 |
电离常数(mol·L-1) | K1=5.6×10-2 K2=5.4×10-3 | K1=1.7×10-5 | K2=6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
①25℃时,浓度均为0.1mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3的pH由大到小的顺序是___。中和等体积、等pH的HCOOH和HCN消耗NaOH的量___(填“前者大”“后者大”或“相等”)。
②下列关于0.1mol·L-1NaHC2O4溶液的说法正确的是___。
a.HC2O4-的电离程度大于水解程度,溶液显酸性
b.HC2O4-的水解程度大于电离程度程度,溶液显碱性
c.溶液中c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.溶液中c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
(2)在t℃时,MgC2O4在水中的沉淀溶解平衡曲线如图1所示。又知t℃时Mg(OH)2的Ksp=5.6×10-12,下列说法不正确的是____
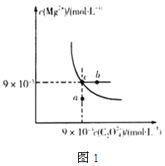
A.在t℃时,MgC2O4的Ksp=8.1×10-5mol2·L-2
B.在MgC2O4饱和溶液中加入Na2CO3固体,可使溶液由c点到b点
C.图中a点对应的是MgC2O4的不饱和溶液
D.在t℃时,MgC2O4(s)+2OH-(aq)Mg(OH)2(s)+C2O42-(aq)平衡常数K=![]()
(3)草酸亚铁晶体(FeC2O4·2H2O)是一种浅黄色固体,难溶于水,受热易分解。某化学兴趣小组设计实验验证草酸亚铁晶体热分解的产物,探究过程如图2:
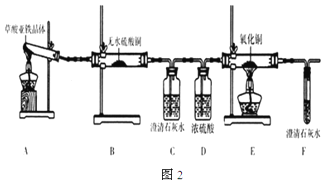
①从环保角度考虑,该套实验装置的明显缺陷是___。
②该兴趣小组进行上述实验时,从实验安全角度考虑,应先点燃___(填“A”或“E”)处的酒精灯。
③若实验过程中观察到B中白色无水CuSO4变成蓝色,___(补充实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O、CO和
④为探究草酸亚铁晶体分解的固体产物,兴趣小组同学准确称取3.60g草酸亚铁晶体(FeC2O4·2H2O),相对分子质量是180),充分加热,使其完全分解,冷却后称得剩余固体的质量为1.60g。若剩余固体只有一种铁的氧化物,通过计算确定该氧化物的化学式为___。草酸亚铁晶体分解的化学方程式为___。
【答案】Na2CO3>NaCN>CH3COONa>Na2C2O4 后者大 ad BD 缺少尾气处理装置 A C中澄清石灰水变浑浊,E中黑色粉末变红色 Fe2O3 FeC2O4·2H2O![]() Fe2O3+3CO↑+CO2↑+2H2O
Fe2O3+3CO↑+CO2↑+2H2O
【解析】
(1)①电离常数越大,酸的酸性越强,其盐溶液的水解程度越小,盐溶液的pH越小,则浓度均为![]() 的
的![]() 、
、![]() 、NaCN、
、NaCN、![]() 的pH由大到小的顺序是
的pH由大到小的顺序是![]() ;pH相同时,酸性越强,其酸的浓度越小,已知甲酸的酸性大于HCN,则pH相同时HCN的浓度大,所以中和等体积、等pH的HCOOH和HCN消耗NaOH的量,HCN消耗的氢氧化钠多;
;pH相同时,酸性越强,其酸的浓度越小,已知甲酸的酸性大于HCN,则pH相同时HCN的浓度大,所以中和等体积、等pH的HCOOH和HCN消耗NaOH的量,HCN消耗的氢氧化钠多;
故答案为:![]() ;后者大;
;后者大;
②![]() 已知
已知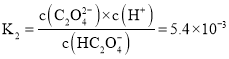 ,HC2O4-的水解平衡常数Kh=
,HC2O4-的水解平衡常数Kh=![]() =
=![]() =
=![]() =1.79×10-13<5.4×10-3,则
=1.79×10-13<5.4×10-3,则![]() 的电离程度大于水解程度,溶液显酸性,故a正确;
的电离程度大于水解程度,溶液显酸性,故a正确;
b.根据a的分析,HC2O4-的电离程度大于水解程度,溶液显酸性,故b错误;
![]() 溶液存在电荷守恒,则溶液中
溶液存在电荷守恒,则溶液中![]() ,故c错误;
,故c错误;
![]() 溶液存在电荷守恒为
溶液存在电荷守恒为![]() ,物料守恒为,
,物料守恒为,![]() ,联立两个式子可得:
,联立两个式子可得:![]() ,故d正确;
,故d正确;
故答案为:ad;
(2)![]() 的Ksp=c/span>(Mg2+)·c(C2O42-)=9×10-3mol/L×9×10-3mol/L =8.1×10-5mol2·L-2,故A正确;
的Ksp=c/span>(Mg2+)·c(C2O42-)=9×10-3mol/L×9×10-3mol/L =8.1×10-5mol2·L-2,故A正确;
B.在![]() 饱和溶液中加入
饱和溶液中加入![]() 固体,会生成碳酸镁沉淀,则镁离子浓度减小,图中由c点到b点时镁离子浓度不变,故B错误;
固体,会生成碳酸镁沉淀,则镁离子浓度减小,图中由c点到b点时镁离子浓度不变,故B错误;
C.沉淀溶解平衡曲线下面的点代表不饱和溶液,则a点对应的是![]() 的不饱和溶液,故C正确;
的不饱和溶液,故C正确;
D.![]() 平衡常数K=
平衡常数K=![]() =
=![]() ,故D错误;
,故D错误;
故答案为:BD;
(3)①根据装置,草酸亚铁晶体受热分解生成CO,![]() 属于有毒气体,要进行尾气处理,所以从环保角度考虑,该套实验装置的明显缺陷是缺少尾气处理装置;
属于有毒气体,要进行尾气处理,所以从环保角度考虑,该套实验装置的明显缺陷是缺少尾气处理装置;
故答案为:缺少尾气处理装置;
②可燃性气体与氧气混合达到一定程度时,遇明火会发生爆炸,所以先点燃分解反应处的酒精灯,排尽装置中的空气,即先点燃A处的酒精灯;
故答案为:A;
③实验过程中观察到B中白色无水![]() 变成蓝色,C中澄清石灰水变浑浊,E中黑色固体变红色,则可证明草酸亚铁晶体热分解的气体产物是
变成蓝色,C中澄清石灰水变浑浊,E中黑色固体变红色,则可证明草酸亚铁晶体热分解的气体产物是![]() ,CO,
,CO,![]() ;
;
故答案为:C中澄清石灰水变浑浊,E中黑色粉末变红色;
④草酸亚铁晶体中的铁元素质量为:![]() ,草酸亚铁晶体中的铁元素完全转化到氧化物中,氧化物中氧元素的质量为:
,草酸亚铁晶体中的铁元素完全转化到氧化物中,氧化物中氧元素的质量为:![]() ,铁元素和氧元素的质量比为:
,铁元素和氧元素的质量比为:![]() :
:![]() :3,设铁的氧化物的化学式为
:3,设铁的氧化物的化学式为![]() ,则有:56x:
,则有:56x:![]() :3,解得x:
:3,解得x:![]() :3,所以铁的氧化物的化学式为
:3,所以铁的氧化物的化学式为![]() ;则草酸亚铁晶体分解生成的产物为
;则草酸亚铁晶体分解生成的产物为![]() 、
、![]() 、CO、
、CO、![]() ,其反应方程式为:FeC2O4·2H2O
,其反应方程式为:FeC2O4·2H2O![]() Fe2O3+3CO↑+CO2↑+2H2O;
Fe2O3+3CO↑+CO2↑+2H2O;
故答案为:![]() ;FeC2O4·2H2O
;FeC2O4·2H2O![]() Fe2O3+3CO↑+CO2↑+2H2O。
Fe2O3+3CO↑+CO2↑+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,一定不能自发进行的是( )
A. 2KClO3(s)===2KCl(s)+3O2(g) ΔH=-78.03kJ/mol ΔS=1110 J/(mol·K)
B. CO(g)===C(s,石墨)+![]() O2(g) ΔH=110.5kJ/mol ΔS=-89.36 J/(mol·K)
O2(g) ΔH=110.5kJ/mol ΔS=-89.36 J/(mol·K)
C. 4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH=-444.3kJ/mol ΔS=-280.1 J/(mol·K)
D. NH4HCO3(s)+CH3COOH(aq)===CO2(g)+CH3COONH4(aq)+H2O(l) ΔH=37.301kJ/mol ΔS=184.05 J/(mol·K)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2+3H2![]() 2NH3合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。
2NH3合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。
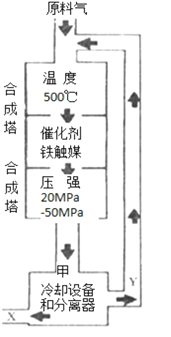
①X的化学式为___;
②图中条件选定的主要原因是(选填字母序号)___;
A.温度、压强对化学平衡影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。如图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是(选填字母代号)___,当横坐标为温度时,变化趋势正确的是(选填字母序号)___。
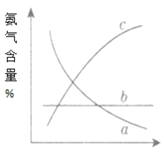
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种盐的稀溶液:amol·L-1NaX溶液和bmol·L-1NaY溶液。下列说法不正确的是( )
A.若a=b,且pH(NaX)>pH(NaY),则酸性HX<HY
B.若a>b,且c(X-)=c(Y-),则溶液中c(HX)>c(HY)
C.若a=b,且c(X-)=c(Y-)+c(HY),则HX为强酸
D.若两溶液等体积混合后c(X-)+c(HX)=c(Y-)+c(HY)=0.1mol·L-1,则a=b=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50molL﹣1盐酸与50mL0.55molL﹣1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
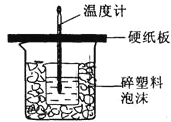
(1)从实验装置上看,图中尚缺少的一种玻璃仪器的名称是_________________。
(2)烧杯间填满碎纸条的作用是___________________________________________________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值_______(填“偏大、偏小、无影响”)。
(4)如果用60mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等、不相等”),所求中和热_______(填“相等、不相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol·L-1NaOH溶液滴定10mL0.100mol·L-1H3PO4溶液,曲线如图所示。下列说法正确的是
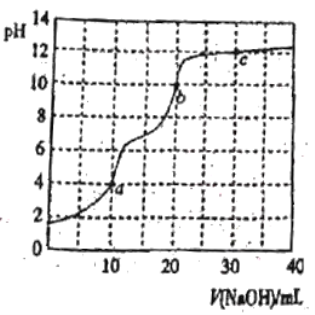
A.滴定终点a可选择酚酞作指示剂
B.c点溶液中c(Na+)>3c(![]() )+2c(
)+2c(![]() )+c(
)+c(![]() )
)
C.b点溶液中c(![]() )>c(
)>c(![]() )>c(
)>c(![]() )
)
D.a、b、c三点中水的电离程度最小的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒温恒容的密闭容器内发生反应:2A(g)+B(g)![]() C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
A. 再充入2mol A,平衡正移,A的转化率增大
B. 如果升高温度,C的体积分数增大
C. 如果增大压强,化学平衡一定向正反应方向移动,B的体积分数减小
D. 再充入1mol C,C的物质的量浓度将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的密闭容器中,可逆反应N2 + 3H2![]() 2NH3 达到平衡状态的标志是
2NH3 达到平衡状态的标志是
A. N2、H2、NH3在容器中共存
B. 混合气体的总物质的量不再发生变化
C. 单位时间内生成n mol N2,同时生成3n mol H2
D. 单位时间内消耗n mol N2,同时消耗n mol NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是(NA表示阿伏加德罗常数)( )
A.常温c(OH-)/c(H+)=10-13的溶液中可能含有K+、Fe2+、NO3-、Cl-四种离子
B.1 L 0.1molL-1的CH3COONa溶液中CH3COO-和OH-的总数大于0.1NA
C.电子工业上用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3+ +Cu = Fe2++Cu2+
D.H2的燃烧热为a kJ·mol-1,H2燃烧热的热化学方程式为:O2(g) +2H2(g) = 2H2O(l) ΔH = -2a kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com