
����Ŀ��N2��3H2![]() 2NH3�ϳɰ���ҵ�Ի�ѧ��ҵ������ҵ������Ҫ���塣��ҵ�ϳɰ�����ʾ��ͼ��ͼ��ʾ��
2NH3�ϳɰ���ҵ�Ի�ѧ��ҵ������ҵ������Ҫ���塣��ҵ�ϳɰ�����ʾ��ͼ��ͼ��ʾ��
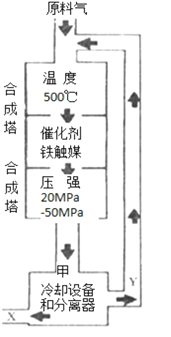
��X�Ļ�ѧʽΪ___��
��ͼ������ѡ������Ҫԭ���ǣ�ѡ����ĸ��ţ�___��
A���¶ȡ�ѹǿ�Ի�ѧƽ��Ӱ��
B������ý�ڸ��¶�ʱ���Դ�
C����ҵ�����ܶ��������ϡ��豸������������
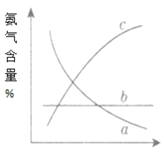
�۸ı䷴Ӧ��������ʹƽ�ⷢ���ƶ�����ͼ��ʾ�������ı䣬�����İٷֺ����ı仯���ơ���������Ϊѹǿʱ���仯������ȷ���ǣ�ѡ����ĸ���ţ�___����������Ϊ�¶�ʱ���仯������ȷ���ǣ�ѡ����ĸ��ţ�___��
���𰸡�NH3 BC C a
��������
�������й�ҵ�ϳɰ�����ʾ��ͼ��֪�����⿼��ϳɰ�ԭ����Ӱ��ϳɰ������أ����û�ѧƽ���ƶ�ԭ��������
���ɺϳɰ�����ʾ��ͼ��֪��ԭ�ϵ����������������ĺϳɡ����ķ��룬����ȴ�豸�ͷ������еõ����ղ������XΪ��������ѧʽΪNH3��
�ʴ�Ϊ��NH3��
��A.�ϳɰ��Ƿ��ȷ�Ӧ�����»�ʹƽ�����淴Ӧ�����ƶ��������ںϳɰ������ѡ��500�����¶ȱȽϺ��ʣ�����ѹǿ���ܼӿ췴Ӧ���ʣ�Ҳ��ʹ��Ӧ�����ƶ������ǹ��ߵ�ѹǿ����߷�Ӧ�ɱ������ѡ��20MPa~50MPa��ѹǿ��A�����
B��ʵ�������в���400��~500��ĸ��£���������ý����ߣ�B����ȷ��
C����ҵ�������������ΪĿ�ģ����Թ�ҵ�������ܶ��������ϡ��豸�����������ƣ�C����ȷ��
�ʴ�Ϊ��BC��
�ۺϳɰ���ҵ��ԭ���ǣ�N2��3H2![]() 2NH3��H<0������H<0���ӻ�ѧƽ��ĽǶȿ���
2NH3��H<0������H<0���ӻ�ѧƽ��ĽǶȿ���
����ӦΪ���ȷ�Ӧ���¶�Խ�ͣ�Խ�����ںϳɰ��������¶ȣ�ƽ�����淴Ӧ�����ƶ��������İٷֺ������٣�����ӦΪ�����С�ķ�Ӧ������ѹǿԽ��Խ�����ںϳɰ�������ѹǿʱƽ�����ҽ��У������İٷֺ��������ͼ�����֪��c����Ҫ������Ϊ�ϳɰ���Ӧ��һ�����ȷ�Ӧ�����Եó������¶ȵ����ߣ�ƽ���������ٵķ����ƶ������ͼ�����֪��a����Ҫ��
�ʴ�Ϊ��C �� a ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ��50 mL 0.50 mol��L��1������50 mL 0.55 mol��L��1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
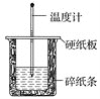
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ���������________��
��2�������60 mL 0.50 mol��L��1������50 mL 0.55 mol��L��1NaOH��Һ���з�Ӧ��������ʵ����ȣ������к���________(��������������������)��
��3��ʵ��ʱ�������ἰNaOH��Һ�������Ϊ50 mL������Һ�ܶȾ�Ϊ1 g��mL��1��������Һ�ı�����c��4.18 J��g��1������1��ʵ����ʼ�¶�Ϊt1������ֹ�¶�Ϊt2�������ƶ��к��ȵļ���ʽ��H��________��
��4������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��________(����ƫ��������ƫС��������Ӱ����)��
II.ij�о���ѧϰС������H2C2O4��Һ������KMnO4��Һ�ķ�Ӧ̽������������ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ����������������ʵ�飺
ʵ����� | ʵ���¶�/K | �й����� | ��Һ��ɫ������ɫ����ʱ��/s | ||||
����KMnO4��Һ | H2C2O4��Һ | H2O | |||||
V/mL | c/ mol��L��1 | VmL | c/ mol��L��1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
��1��ͨ��ʵ��A��B����̽����________(���ⲿ����)�ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V1��________��T1��________��ͨ��ʵ��________(��ʵ�����)��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V2��________��
��2����t1��8�����ɴ�ʵ����Եó��Ľ�����________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��Ϊ�˴�������Cr2O![]() ���Թ�ҵ��ˮ����������Ĵ�������������ҵ��ˮ�м���������NaCl����FeΪ�缫���е�⣬����һ��ʱ�䣬��Fe(OH)3��Cr(OH)3�������ɣ���������Ĺ�ҵ��ˮ�и�(Cr)�ĺ����ѵ����ŷű�����ش��������⣺
���Թ�ҵ��ˮ����������Ĵ�������������ҵ��ˮ�м���������NaCl����FeΪ�缫���е�⣬����һ��ʱ�䣬��Fe(OH)3��Cr(OH)3�������ɣ���������Ĺ�ҵ��ˮ�и�(Cr)�ĺ����ѵ����ŷű�����ش��������⣺
(1)�缫��Ӧʽ������___������___��
(2)д��Cr2O![]() ��ΪCr3+�����ӷ���ʽ___��
��ΪCr3+�����ӷ���ʽ___��
(3)��ҵ��ˮpH���ߵ�ԭ��___��
(4)��װ���в��ܸ���ʯī�缫��ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��![]() ��CO�γ�B��B�ܷ���������Ӧ��C������ֻ��һ���⣬�������ת����ϵ����
��CO�γ�B��B�ܷ���������Ӧ��C������ֻ��һ���⣬�������ת����ϵ����![]() ������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ����
������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ����![]() ��
��
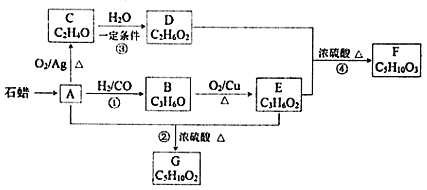
��ش�
![]() �л���C�Ľṹ��ʽ��______����Ӧ�ڵķ�Ӧ������______��
�л���C�Ľṹ��ʽ��______����Ӧ�ڵķ�Ӧ������______��
![]() д��һ�������·�����Ӧ�ٵĻ�ѧ����ʽ______��
д��һ�������·�����Ӧ�ٵĻ�ѧ����ʽ______��
![]() ����˵������ȷ����______
����˵������ȷ����______![]() ����ĸ
����ĸ![]() ��
��
A.������A������
B.������D�������ֹ�����
C.�ý�������������F��G
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Se�����仯�����ڹ�ũҵ��������������;����ͭ�����ࣨ��Ҫ�ɷ�ΪAg2Se��Cu2Se�������𡢲��ȣ�Ϊԭ���Ʊ������Ĺ���������ͼ��ʾ��

�ش��������⣺
��1����������ʱ������Ũ�����Ϊ_____�����ţ���
A��Ũ���� B�� 20������ C��50������ D�� 80%����
��2����������������Cu2Se���뷴Ӧʱ���÷�Ӧ������������_______��
��3����ˮ��������������Ӧ�Ļ�ѧ����ʽΪ____________��
��4�������������ô����ɲ����������ķ��������ᴿ����ô������������Ļӷ��������������¶ȵĹ�ϵ��ͼ��ʾ��

��������п��Ƶ�����¶���_____�����ţ���
A��455�� B��462�� C��475�� D��515��
��5����ˮ�������е�¯������飬�Ҽ�����ˮ���н��ݣ�Ŀ����____________________�����������к��еĽ���������___________��
��6����������Һ���У�c(Ag+)=3.0��10-2 mol/L������Һ��c(SO42-)���Ϊ___________________����֪��Ksp(Ag2SO4)=1.4��10-5������������2λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɵ����������ϳɰ����ķ��������1918��ŵ������ѧ����
N2+3H2![]() 2NH3
2NH3
����һ�ܱ������г���1 mol N2��3 mol H2����һ��������ʹ�÷�Ӧ�����������й�˵����ȷ���ǣ� ��
A.�ﵽ��ѧƽ��ʱ��N2����ȫת��ΪNH3
B.�ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ��һ�����
C.�ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯
D.�ﵽ��ѧƽ��ʱ������Ӧ���淴Ӧ�����ʶ�Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ�������й���C2H2(g)��![]() O2(g)=2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵����ȷ����(����)
O2(g)=2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵����ȷ����(����)
A.��10NA������ת��ʱ������1300 kJ����
B.��8NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ����
C.��NA��ˮ����������ΪҺ��ʱ������1300 kJ����
D.��2NA��̼��˫������ʱ���ų�1300 kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����(H2C2O4)��һ�ֶ�Ԫ���ᣬ���ἰ���ι㷺����ҽҩ��ӡȾ�����ϵȹ�ҵ��
��1����֪25��ʱ�����ֳ��������Ka���±���ʾ��
����� | H2C2O4 | CH3COOH | HCN | H2CO3 |
���볣��(mol��L-1) | K1=5.6��10-2 K2=5.4��10-3 | K1=1.7��10-5 | K2=6.2��10-10 | K1=4.2��10-7 K2=5.6��10-11 |
��25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L-1��Na2C2O4��CH3COONa��NaCN��Na2CO3��pH�ɴ�С��˳����___���к͵��������pH��HCOOH��HCN����NaOH����___(����ǰ�ߴ��������ߴ������������)��
�����й���0.1mol��L-1NaHC2O4��Һ��˵����ȷ����___��
a.HC2O4-�ĵ���̶ȴ���ˮ��̶ȣ���Һ������
b.HC2O4-��ˮ��̶ȴ��ڵ���̶ȳ̶ȣ���Һ�Լ���
c.��Һ��c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.��Һ��c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
��2����t��ʱ��MgC2O4��ˮ�еij����ܽ�ƽ��������ͼ1��ʾ����֪t��ʱMg(OH)2��Ksp=5.6��10-12������˵������ȷ����____
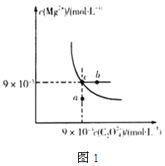
A.��t��ʱ��MgC2O4��Ksp=8.1��10-5mol2��L-2
B.��MgC2O4������Һ�м���Na2CO3���壬��ʹ��Һ��c�㵽b��
C.ͼ��a���Ӧ����MgC2O4�IJ�������Һ
D.��t��ʱ��MgC2O4(s)+2OH-(aq)Mg(OH)2(s)+C2O42-(aq)ƽ�ⳣ��K=![]()
��3��������������(FeC2O4��2H2O)��һ��dz��ɫ���壬������ˮ�������ֽ⡣ij��ѧ��ȤС�����ʵ����֤�������������ȷֽ�IJ��̽��������ͼ2��
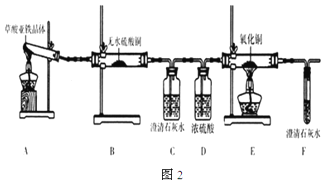
�ٴӻ����Ƕȿ��ǣ�����ʵ��װ�õ�����ȱ����___��
�ڸ���ȤС���������ʵ��ʱ����ʵ�鰲ȫ�Ƕȿ��ǣ�Ӧ�ȵ�ȼ___(����A������E��)���ľƾ��ơ�
����ʵ������й۲쵽B�а�ɫ��ˮCuSO4�����ɫ��___(����ʵ������)�����֤���������������ȷֽ�����������H2O��CO��
��Ϊ̽��������������ֽ�Ĺ�������ȤС��ͬѧȷ��ȡ3.60g������������(FeC2O4��2H2O)����Է���������180)����ּ��ȣ�ʹ����ȫ�ֽ⣬��ȴ��Ƶ�ʣ����������Ϊ1.60g����ʣ�����ֻ��һ�����������ͨ������ȷ����������Ļ�ѧʽΪ___��������������ֽ�Ļ�ѧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������Ⱦ��Ĵ������Ի��������������Ⱦ������������������ĵ�����ʮ����Ҫ�����塣
(1)��֪��C(s)+O2(g)�TCO2(g)��H����393.5/kJmol
N2(g)+O2(g)�T2NO(g)��H��+180kJ/mol
��C(s)+2NO(g)�TCO2(g)+N2(g) ����H��_____kJ/mol��
(2)��һ���¶��£���2L�ĺ����ܱ������г���4.0 mol NO2��4.0 mol CO���ڴ��������·�����Ӧ4CO(g)+2NO2(g)4CO2(g)+N2(g)�����������������ʾ��
t/min | 0 | 5 | 10 | 15 | 20 |
n(NO2)/mol | 4.0 | 3.4 | 3.12 | 3.0 | 3.0 |
n(N2)/mol | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
����0��5 min�ڣ���CO2��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ_____��
�ڴ��¶��µĻ�ѧƽ�ⳣ��K�ı���ʽΪ_____��
(3)�û���̿��ԭ��������������йط�ӦΪC(s)+2NO(g)![]() CO2(g)+N2(g)��ij�о�С����2L�ܱ������м��������Ļ���̿��һ������NO�������¶Ⱥ�������䣬����������Ӧ��
CO2(g)+N2(g)��ij�о�С����2L�ܱ������м��������Ļ���̿��һ������NO�������¶Ⱥ�������䣬����������Ӧ��
������������˵��������Ӧ�Ѵ�ƽ�����_____(����)��
A.����̿���������ٱ仯
B.������������ܶȱ��ֲ���
C.2v(NO)�� ��v(N2)��
D. ���ֲ���
���ֲ���
��ѹǿΪpʱ�������Ĵ�Ч�ʡ������������������¶ȵĹ�ϵ��ͼ��ʾ��������������������Ҫȡ�����¶�ʱ����Ӧ���¶ȷ�Χ��_____��
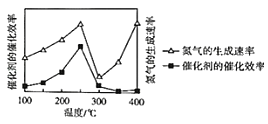
(4)��(N2H4)����ɫҺ�壬����ǿ��ԭ�ԡ�
���µ�ˮ��Һ�������ԣ�����������NH3H2O���ƣ����һ�����뷽��ʽΪ_____��
������N2H4ȼ�ϵ�ز���Ի���û����Ⱦ���õ���Թ���������Ϊ�����(�ܴ���O2��)��д�������ĵ缫��Ӧʽ_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com