
下列有关叙述正确的是( )
A. O和
O和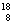 O中子数相同,质子数不同,互为同位素
O中子数相同,质子数不同,互为同位素
B.H2O比H2S稳定,H—S键比H—O键更难断裂
C.Na2O晶体中存在离子键,是离子化合物
D.Na2O2晶体中阳离子与阴离子个数比为1:1
科目:高中化学 来源: 题型:
化学是以实验为基础的学科。利用已学知识对下列实验进行分析并填空:
Ⅰ.(8分) 某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置完成
同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置实验来验证卤族元素性质的递变规律(夹持装置已略去)。A、B、C三个胶头滴管分别是氯酸钾溶液、NaBr溶液、淀粉KI溶液。已知常温下浓盐酸与氯酸钾溶液能反应生成氯气。
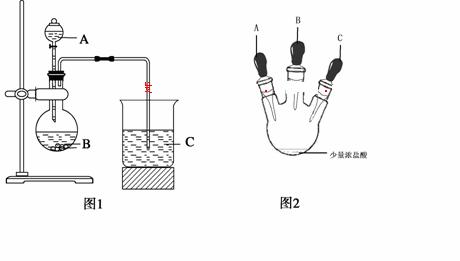
(1)甲同学设计实验所涉及的离子方程式为 、
;
(2)乙同学具体操作如下:
①先挤压胶体滴管A,使少量溶液滴入烧瓶内;
②挤压体滴管B,使稍过量溶液滴入烧瓶内,充分反应。写出该操作中主要离子方程式为 。
③再挤压体滴管C,使少量溶液滴入烧瓶内,可观察到 ;
(3)根据甲乙同学的实验可得到的结论是: 。
II.(6分)
| 实验目的 |
| ||
| 实验 |
|
|
|
| 实验结论 | 结论: FeCl3在实验中的作用为: | ||
| 反应方程式 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A是农药生产中的一种中间体,其结构简式如下,下列叙述正确的是( )
A.有机物A属于芳香烃
B.有机物A和浓硫酸混合加热,可以发生消去反应
C.有机物A的核磁共振氢谱有7个峰
D.1molA和足量的NaOH溶液反应,最多可以消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是( )
A.苯酚具有弱酸性,但不能使紫色石蕊变红
B.能因发生化学反应而使溴水褪色的物质一定是和溴水发生加成反应
C.用核磁共振氢谱鉴别1溴丙烷和2溴丙烷
D.含醛基的有机物都能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得。A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应:
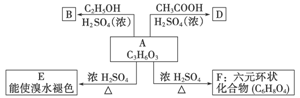
试写出:
化合物的结构简式:
A______________________________,(3分)
B__________________________________________________________________,(3分)
D_____________________________________。(3分)
化学方程式:A→E:
____________________________________________________________________(4分),
A→F: ________________________________________________________________________。(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1kJ·mol-1;
HCl(aq)与NaOH(aq)反应的ΔH=-55.6kJ·mol-1。
则HCN在水溶液中电离的ΔH等于( )
A.+43.5kJ·mol-1 B.-43.5kJ·mol-1 C.+67.7kJ·mol-1 D.-67.7kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与金属腐蚀有关的说法正确的是( )

A.图a中,插入海水中的铁棒越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验
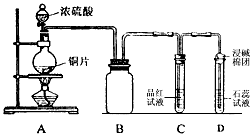
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请在答题卷上把导管补充
完整 ▲ 。
(2)请写出铜跟浓硫酸反应的化学方程式 ▲ 。
(3)实验中D中的现象 ▲ 。
(4)实验中,该同学取6.4g铜片和12mL 18mol·L-1H2SO4溶液放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余;该同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是 ▲ 填字母编号)。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.Na2CO3粉末
(5)若将16g铜与50mLH2SO4物质的量浓度为一定值的浓硫酸反应,铜完全溶解。请回答:
①反应中产生的气体在标准状况下的体积为 ▲ L。
②该反应中被还原的H2SO4的物质的量为 ▲ mol。
③待产生的气体全部释放后,向溶液中滴加VmL a mol·L-1NaOH溶液,恰好使溶液中
的Cu2+全部转化为沉淀,则原浓硫酸中H2SO4的物质的量浓度= ▲ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com