
下列与金属腐蚀有关的说法正确的是( )

A.图a中,插入海水中的铁棒越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
【知识点】本题考查金属的电化学腐蚀与防护相关知识
【答案解析】B解析:A图a中,铁棒中含有铁和碳,在海水与空气交接处铁、碳和海水因发生吸氧腐蚀构成了原电池,铁作负极失电子而容易被腐蚀;插入海水中的铁棒,海水中氧的含量较少,所以插入海水中的铁棒腐蚀速率较越靠近海水与空气交接处腐蚀越慢,所以插入海水中的铁棒越靠近海水与空气交接处腐蚀越严重故不正确.B图b中,开关由M改置于N时,合金作正极,锌作负极,所以Cu-Zn合金的腐蚀速率减慢,故正确.C图c中,接通开关时Zn腐蚀速率增大,但氢离子在铂丝上放电生成氢气,故错误.D图d中,该原电池中锌作负极,二氧化锰作正极,正极上得电子发生还原反应,所以Zn-MnO2干电池自放电腐蚀主要是由MnO2的还原作用引起的,故错误.
【思路点拨】本题以金属的腐蚀为载体考查了原电池原理,难度不大,原电池中负极上金属容易被腐蚀,正极上金属被保护


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
A. O和
O和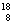 O中子数相同,质子数不同,互为同位素
O中子数相同,质子数不同,互为同位素
B.H2O比H2S稳定,H—S键比H—O键更难断裂
C.Na2O晶体中存在离子键,是离子化合物
D.Na2O2晶体中阳离子与阴离子个数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中的信息判断下列说法正确的是( )。
| 物质 | 金刚石 | 石墨 |
| 外观 | 无色,透明固体 | 灰黑,不透明固体 |
| 熔点 | ? | ? |
| 燃烧热/(kJ·mol-1) | 395.4 | 393.5 |
A.表示石墨燃烧热的热化学方程式为C(石墨,s)+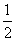 O2(g)=CO(g) ΔH=-393.5kJ·mol-1
O2(g)=CO(g) ΔH=-393.5kJ·mol-1
B.由表中信息知C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1
C.由表中信息可得如图所示的图像
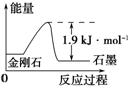
D.由表中信息可推知相同条件下金刚石的熔点高于石墨的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是____________________________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式:__________________________;
负极的电极反应式:__________________________。
(3)下图是一个电解过程示意图。
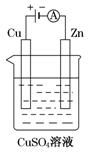
①锌片上发生的电极反应式是:_____________________________。
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)新制备的氯水显__________色,说明氯水中有__________(填分子式)分子存在。
(2)向氯水中滴加几滴AgNO3溶液,立即有__________生成,说明氯水中有__________(填离子符号)存在,反应的化学方程式为_____________ _____________
(3)氯水光照后颜色变浅,并放出___ _____气体。
(4) 相同物质的量 的SO2气体和SO3气体,其分子数之比为________,相同质量的SO2气体和SO3气体,其分子数之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NM—3是处于临床试验阶段的小分子抗癌药物,分子结构如图5,下列说法正确的是 ( )
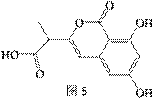
A.该有机物的化学式为C12H12O6
B.1mol该有机物最多可以和3molNaOH反应
C.该有机物容易发生加成、取代、消去等反应
D.该有机物分子与三氯化铁溶液反应显色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com