
| A、pH值变大 |
| B、n (OH-)减少 |
| C、C (Ca2+)增大 |
| D、pH值减小 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、CH4+Cl2→CH3Cl+HCl 取代反应 | ||
B、CH2=CH2+HCl
| ||
C、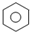 +Br2 +Br2
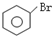 +HBr 取代反应 +HBr 取代反应 | ||
D、2CH3CH2OH+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ni的还原性比铁稍弱,可采用金属铝作还原剂的热还原法 |
| B、在新制的氯水中加入NaOH溶液至中性时,满足C(Na+)═C(ClO-)+C(HClO) |
| C、在某溶液中加入K3Fe(CN)6若产生蓝色沉淀即可证明Fe3+ 的存 |
| D、在相同温度下,向1mL 0.2mol?L-1 NaOH溶液中滴入2滴0.1 mol?L-1 MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol?L-1 FeCl3溶液,又生成红褐色沉淀,可证明Fe(OH)3的溶解度小于Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
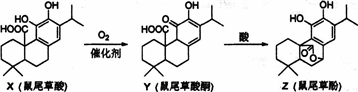
| A、X、Y、Z互为同系物 |
| B、X、Y、Z均能与FeCl3溶液发生显色反应 |
| C、1molZ与NaOH溶液反应最多消耗3molNaOH |
| D、1molY与浓溴水反应最多消耗3molBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Y | Z | W | ||
| X | Q |
| A、元素Y、Z、W、Q均可与氢元素形成一种或多种氢化物,其中YH4中 H的质量分数最大 |
| B、由元素X与元素W组成的物质既能溶于足量的稀盐酸,又能溶于足量的氨水 |
| C、元素Y、Z、W的单质晶体一定是同种类型的晶体 |
| D、为了增强Q单质水溶液的漂白性,可将与W同主族且相邻的元素的低价氧化物通入其中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中加入固体氢氧化钠后,溶液中有c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | ||
B、加水稀释0.2 mol?L-1的醋酸溶液后,溶液中
| ||
| C、pH=3的弱酸HR溶液与pH=13的NaOH溶液等体积混合后,恰好完全反应,反应后的溶液中一定有:c(R-)+c(HR)=0.05mol?L-1 | ||
| D、0.2 mol?L-1的CH3COOH溶液与0.1 mol?L-1NaOH溶液等体积混合后溶液呈酸性,则c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氧化 |
| 雨水 |
| 雨水 |
| 氧化 |
| A、若猜想一或猜想三正确,则该雨水加入盐酸后,再加入BaCl2溶液,有白色沉淀生成 |
| B、若存在猜想二的过程,则该雨水可能使品红褪色 |
| C、若只存在猜想一的过程,则该雨水的pH随时间延长而增大 |
| D、上述任意一个猜想正确,该地区雨水的pH均小于5.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com