
【题目】下列实验中的颜色变化,与氧化还原反应无关的是( )
A. NaOH溶液滴入FeSO4溶液中,产生白色沉淀,随后变为红褐色
B. 石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
C. Na2S溶液滴入AgCl浊液中,沉淀由白色逐渐变为黑色
D. 热铜丝插入稀硝酸中,产生无色气体,随后变为红棕色
【答案】C
【解析】
A、发生的离子反应是Fe2++2OH-=Fe(OH)2↓,然后再发生4Fe(OH)2+O2+2H2O=4Fe(OH)3,该反应为氧化还原反应,故A不符合题意;
B、氯水中存在Cl2+H2O![]() HCl+HClO,石蕊遇酸变红,HClO具有强氧化性,能将有色物质漂白,HClO漂白有色物质属于氧化还原反应,故B不符合题意;
HCl+HClO,石蕊遇酸变红,HClO具有强氧化性,能将有色物质漂白,HClO漂白有色物质属于氧化还原反应,故B不符合题意;
C、白色沉淀转变为黑色沉淀,发生2AgCl+Na2S=Ag2S+2NaCl,该反应没有化合价的变化,不属于氧化还原反应,故C符合题意;
D、铜丝与稀硝酸发生3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,该反应为氧化还原反应,故D不符合题意;
答案为C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B. 一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C. 某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4;若体积减小,则y>4;否则y<4
D. 相同质量的烃,完全燃烧,消耗O2越多,烃中含H量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A.64g二氧化硫中的氧原子数和标准状况下22.4L二氧化碳中的氧原子数
B.200mL1mol/L氯化钙溶液中c(Cl-)和100mL1mol/L氯化钾溶液中c(Cl-)
C.2mol水的摩尔质量和1mol水的摩尔质量
D.20%氢氧化钠溶液中氢氧化钠物质的量浓度和10%氢氧化钠溶液中氢氧化钠物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体NH4Br置于密闭容器中,在某温度下,发生反应:NH4Br(s)![]() NH3(g)+HBr(g),2HBr(g)
NH3(g)+HBr(g),2HBr(g)![]() Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
A. 0.5 mol·L-1·min-1B. 2.5 mol·L-1·min-1
C. 2 mol·L-1·min-1D. 1.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaC1的流程如下:
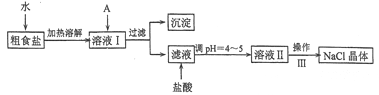
(1)加入A试剂,是为了除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子。A代表的是多种试剂,按滴加顺序依次为:iNaOH,ⅱ__________,ⅲ_________(填化学式)。
(2)请写出下列试剂加入试剂i时发生主要反应的离子反应方程式:_________
(3)右下图是某学生的过滤操作示意图,其操作不规范的是________(填标号)。
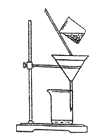
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)操作III的名称是__________
(5)mg粗盐提纯后得到ng纯净的NaCl固体,则m与n的大小关系为_________.
A.m>n B. m=n C. m<n D. 无法确定.
(6)实验室需配制480 mL0.400mol/L盐酸,现用如图所示浓盐酸配制,回答下列问题:
盐酸
分子式: HCl
相对分子质量: 36.5
密度: 1.2g/cm3
HCl的质量分数为: 36.5%
①配制需要的玻璃仪器有玻璃棒、量简、烧杯、________(填仪器名称)
②需量取浓盐酸的体积为:__________mL。(结果保留1位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有四种物质:①氧化铁 ②硫酸 ③碳酸氢钠 ④氢氧化钠
①属于盐的是________(填序号),写出这种物质在水溶液中的电离方程式__________。
②上述物质中有一种与其他三种物质均能反应,此物质是__________(填序号)。
(2)酸性条件下,次磷酸(H3PO2)可发生下列反应而用于化学镀银。
口Ag++口H3PO2+口 =口Ag+口H3PO4+口
试回答下列问题
①该反应的氧化产物是_________。
②请将反应物和生成物补充完整并配平,并用双线桥法标出电子转移的数目。______
③若反应中生成10.8gAg,则转移电子的数目约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是__________。
A 溶液中导电粒子的数目减少 B 醋酸的电离程度增大,c(H+)亦增大
C 溶液中c(CH3COO-)/[c(CH3COOH)c(OH-)]不变 D 溶液中c(CH3COO-)/c(H+)减小
(2)①常温下将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2=_____________(溶液体积变化忽略不计)。
(3)常温下,浓度均为0.lmol/L的下列五种溶液的pH值如表所示:
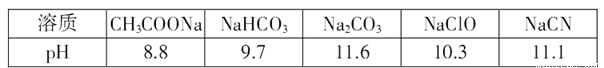
①根据表中数据,将浓度均为0.01 mol/L的下列四种酸的溶液分别稀释100倍,pH变化最小的是_____
A HCN B HClO C H2CO3 D CH3COOH
②根据以上数据,判断下列反应可以成立的是________。
A CH3COOH+Na2CO3=NaHCO3+CH3COONa B CH3COOH+NaCN=HCN+CH3COONa
C CO2 +H2O+ 2NaClO=Na2CO3+2HClO D NaHCO3+HCN=NaCN+CO2 +H2O
(4)几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度离子Cu2+、Fe2+、Mg2+的溶液中滴加NaOH溶液时,_________(填离子符号)先沉淀。
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
(1)已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25 ℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是__________;
②体积相同、c(H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月9日中国科学院正式向社会发布113号、115号、117号和118号元素的中文名称。已知117号元素有多种原子,如![]() 、
、![]() 等。下列说法正确的是
等。下列说法正确的是
A. ![]() 和
和![]() 的化学性质完全不同
的化学性质完全不同
B. 元素Ts的相对原子质量为![]()
C. 基态![]() 原子核外电子共占据7个能级
原子核外电子共占据7个能级
D. Ts位于周期表的第七周期ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况时,8.96L的容器里所含CO的质量为11.2g,则一氧化碳的摩尔质量为____________ g/mol ;
(2)3.01×1023个OH-的物质的量是 __________ mol,质量为_____g,其质子数为________(用NA表示),电子数为 ___________(用NA表示);
(3)同温同压下同体积的H2和A气体的质量分别是0.2 g和1.6 g,则气体A的相对分子质量为________,含有A的分子个数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com