
【题目】按要求填空:
(1)有四种物质:①氧化铁 ②硫酸 ③碳酸氢钠 ④氢氧化钠
①属于盐的是________(填序号),写出这种物质在水溶液中的电离方程式__________。
②上述物质中有一种与其他三种物质均能反应,此物质是__________(填序号)。
(2)酸性条件下,次磷酸(H3PO2)可发生下列反应而用于化学镀银。
口Ag++口H3PO2+口 =口Ag+口H3PO4+口
试回答下列问题
①该反应的氧化产物是_________。
②请将反应物和生成物补充完整并配平,并用双线桥法标出电子转移的数目。______
③若反应中生成10.8gAg,则转移电子的数目约为________。
【答案】③ NaHCO3=Na++HCO3- ② H3PO4 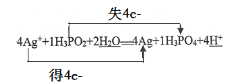 0.1NA
0.1NA
【解析】
(1)①金属阳离子和酸根阴离子构成的化合物为盐;
②硫酸和金属氧化物、碱、碳酸盐反应;
(2)反应中Ag+→Ag,化合价降1,反应中H3PO2→H3PO4,+1价的P化合价升高为磷酸分子中+5价,化合价升高4,依据得失电子守恒,原子个数守恒配平方程式。
(1)①:①氧化铁是氧化物,②硫酸是酸,③碳酸氢钠为盐,④氢氧化钠为碱,碳酸氢钠是强电解质水溶液中完全电离,电离方程式:NaHCO3=Na++HCO3-;
②上述物质中有一种与其他三种物质均能反应的物质是硫酸,和氧化铁反应生成硫酸铁和水,和碳酸氢钠反应生成硫酸钠、二氧化碳和水,和氢氧化钠反应生成硫酸钠和水;故答案为:②;
(2)①该反应的氧化产物是H3PO4;
②反应中Ag+→Ag,化合价降1,反应中H3PO2→H3PO4,+1价的P化合价升高为磷酸分子中+5价,化合价升高4,要使氧化剂得到电子总数等于还原剂失去电子总数,则Ag+系数为4,H3PO2系数为1,依据原子个数守恒,反应方程式:4Ag++H3PO2+2H2O═4Ag+H3PO4+4H+,用双线桥法标出电子转移的数目: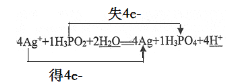 ;
;
③由反应可知生成4mol银转移4mol电子,若反应中生成10.8gAg,物质的量为0.1mol,则转移电子的数目约为0.1NA。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度改变为1.5 mol·L-1
B. 把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1
C. 把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%
D. 把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) ![]() CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )

A. 该反应的ΔH>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 在T2时,若反应体系处于状态D,则此时一定有v正<v逆
D. 在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯能在多种条件下发生水解反应:CH3COOC2H5+H2OCH3COOH+C2H5OH.已知该反应的速率随c(H+)的增大而加快。如图为CH3COOC2H5的水解速率随时间的变化图。下列说法正确的是( )
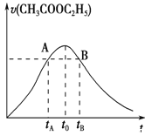
A. 反应初期水解速率增大可能是溶液中c(H+)逐渐增大所致
B. A、B两点表示的c(CH3COOC2H5)相等
C. 图中t0时反应达到平衡状态
D. tB时CH3COOC2H5的转化率低于tA时CH3COOC2H5的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是( )
A. NaOH溶液滴入FeSO4溶液中,产生白色沉淀,随后变为红褐色
B. 石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
C. Na2S溶液滴入AgCl浊液中,沉淀由白色逐渐变为黑色
D. 热铜丝插入稀硝酸中,产生无色气体,随后变为红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如下表所示:
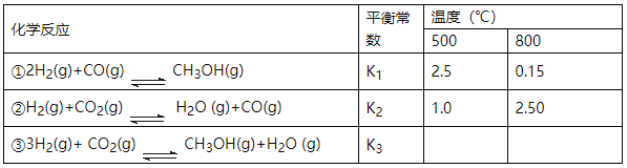
请回答下列问题:
(1)反应②是__________(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示);根据反应③判断△S__________0(填“>”、“=”或“<”),在____________(填“较高”或“较低”)温度下有利于该反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有______________(填写字母序号)。
a.缩小反应容器的容积
b.扩大反应容器的容积
c.升高温度
d.使用合适的催化剂
e.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol·L-1、0.8mol·L-1、0.3mol·L-1、0.15mol·L-1,则此时v正__________v逆(填“>”、“=”或“<”)。
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件随时间的变化曲线,开始时升温,t1时平衡,t2时降压,t3时增加CO浓度,t4时又达到平衡.请画出t2至t4的曲线______。
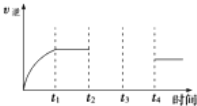
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是

A. 气态氢化物的稳定性:R>W
B. X与Y可以形成原子个数比为1:1和1:2的两种离子化合物
C. 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2-
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2﹣N2+HCl
①该反应中被氧化的元素是_____(填元素名称),氧化剂是_____(填化学式)。
②配平该方程式:_____NH3+_____Cl2=_____N2+_____HCl
(3)“地康法”制氯气的反应原理图示如下:
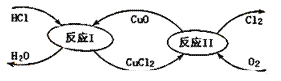
①反应I的化学方程式为_____。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。
(1)该反应中还原剂的化学式是__________;被还原元素的元素符号是_________;
(2)试比较KClO3和CO2的氧化性强弱____________________________________;
(3)消毒时,ClO2还可以将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物,此过程说明ClO2具有___________ (填“氧化”或“还原”)性;
(4)当转移0.2mol电子时,生成的ClO2在标准状况下的体积为_________________________ ;
(5)有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,将这6种物质分别填入下面对应的横线上,并将该化学方程式配平。
________+________Na2SO3+________→________ +________ +________+_____H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com