
����Ŀ����ͼ��ʾ����ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1 mol��ˮ������Ϊ100 g������˵����ȷ����(����)
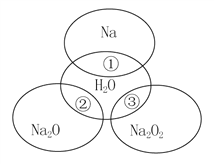
A. Na2O2������������Ŀ֮��Ϊ1��1
B. ��Ӧ�ٵ����ӷ���ʽΪNa��2H2O===Na����2OH����H2��
C. ���������۳�ַ�Ӧ��������Һ�����ʵ�������������>��>��
D. ��Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.1mol
���𰸡�C
��������
����A.������������������O22-����������������Ŀ֮��Ϊ1��2������B����Ӧ�������ӷ���ʽΪ��2Na+2H2O=2Na++2OH-+H2��������C����Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2��ת�Ƶ���2e-����0.1mol�������Ʒ�Ӧ�����ת��0.1 mol���ӣ���ȷ��D���ơ������ơ��������ƺ�ˮ��Ӧ�ķ���ʽ�ֱ����£�
Na+1/2H2O=NaOH+1/2H2������Һ���ӵ�����=m��Na��-m��H2��=2.3g-0.1g=2.2g��Na2O+H2O=2NaOH����Һ���ӵ�����=m��Na2O��=0.1mol��62g/mol=6.2g��Na2O2+H2O=2NaOH+1/2O2������Һ���ӵ�����=m��Na2O2��-m��O2��=m��Na2O��=6.2g,������Һ���ӵ�������С˳��Ϊ���ƣ�������=�������ƣ�������ԭ���غ�֪��0.1mol���ơ������ơ��������ơ�����ˮ�����������Ƶ����ʵ����ֱ�Ϊ��0.1mol��0.2mol��0.2mol��ͨ�����Ϸ�����֪��0.1mol���ơ������ơ��������ơ��ֱ�����ˮ������Һ�����������ֱ�Ϊ��4/(100+2.2)��100%��8/(100+6.2)��100%��8/(100+6.2)��100%������������������ַ�Ӧ��������Һ�����������Ӵ�С��������=��������,ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʻ���(COS)��������ʳѬ��������ȡ��ӦΪ CO(g)+H2S(g) ![]() COS(g)+H2(g)����H=-30kJ��mol-1���ں��ݵ��ܱ������в�ͬ�����·�����Ӧ���ﵽƽ�⣬�������±���
COS(g)+H2(g)����H=-30kJ��mol-1���ں��ݵ��ܱ������в�ͬ�����·�����Ӧ���ﵽƽ�⣬�������±���
ʵ�� | �¶�/�� | n��ʼ/mol | ƽ��ʱ | ����ʱ�� | |||
CO | H2S | COS | H2 | n(CO)/mol | min | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 | e |
2 | 150 | 7.0 | 7.0 | 3.0 | 3.0 | a | f |
3 | 200 | 20.0 | 20.0 | 0 | 0 | 16.0 | g |
����˵���������
A. ʵ��1 ��Ӧ��ʼ��ƽ�����������зų�������Ϊ 90kJ
B. ʵ��2 ��ƽ��ʱ��a>7.0
C. ʵ��3 ʱ�䣺g��e
D. ʵ��3 CO �ﵽƽ��ʱ��ת���ʱ�ʵ��1 С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������岻������ˮ���ռ���Ҫ�������ſ������ռ�����( )
A.NO2
B.O2
C.NH3
D.NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2ͨ�����й������̿��Ʊ�����ԭ��H2SO4�������ԴH2
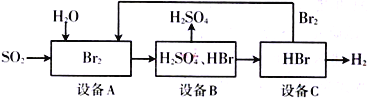
����˵���в���ȷ����
A. �豸A�е���ˮ��ɫ��������SO2�Ļ�ԭ��
B. ���������յ��ŵ㣺Br2����ѭ�����ã�����������ԴH2
C. �ù������̵��ܷ�Ӧ����ʽΪ��SO2+Br2+2H2O=H2SO4+2HBr
D. �豸C���Ƿ����H2SO4������C����Ʒ��Һ�м���BaCl2��Һ���۲��Ƿ��г���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ���ܴ������棬������Ũ��������һ�������ǣ� ����
A.SO2��HI��N2B.O2��CO2��NO
C.NH3��N2��H2D.O2��H2��SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������վ�����ⶨˮ���ܽ������������Ҫ��������ȡ100mLˮ����Ѹ�ټ���̶���MnSO4�ͼ���KI����KOH����Һ����ȫ��Ӧ���������ʹ֮����I2������0.0040mol/L��Na2S2O3��Һ��֮��Ӧ���йط�Ӧ�Ļ�ѧ����ʽΪ��
��2MnSO4+O2+4KOH=2MnO(OH)2+2K2SO4���÷�Ӧ���죩
��MnO(OH)2+2KI+2H2SO4=MnSO4+I2+K2SO4+3H2O
��I2+2Na2S2O3=2NaI+Na2S4O6
��1������ˮ������20.00mLNa2S2O3��Һ������Na2S2O3�����ʵ���Ϊ________mol��
��2���Լ����ˮ���е��ܽ���_____��g/L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������þ��(��Ҫ�ɷ�MgCO3��CaCO3��FeCO3��SiO2)�Ʊ��ߴ�������þ�Ĺ�������:
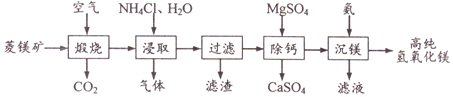
��1����������ʱFeCO3������Ӧ�ķ���ʽΪ_____��
��2������ȡ���¶�100�����ң��ò��躬þ��������뷴Ӧ�Ļ�ѧ����ʽΪ______��
��3������ȡ��ʱNH4Cl������Mg2+�����ʵ�Ӱ����������ͼ��ʾ�������й�˵����ȷ��____(�����)��
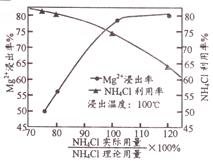
A.����ȡ��ʱ�ʵ����转��
B.�ó���������20%��NH4Cl���н�ȡ
C.����NH4Cl�Խ�ȡ����������ж��ν�ȡ�������ν�ȡҺ�ϲ�
D.�����¶Ȳ���100���ɴٽ�NH4Cl��ˮ���NH3���ݳ�
��4�������������п�ѭ�����õ�������______��
��5����Ҫ�õ��ߴ�Mg(OH)2���������þ���������õĹ������ϴ�ӣ����������ϴ���ķ�����_______��
��6��25��ʱ��Ksp(CaSO4)=7.2��10-5��ʵ������������ǰ����Һ��c(Ca2+)�ֱ�Ϊ2.8g/L��0.8g/L,��1L��Һ���������MgSO4���������Ϊ____g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. ���淴Ӧ���淴Ӧ�Ļ�ܼ�ȥ����Ӧ�Ļ�ܾ��Ǵ˷�Ӧ����H
B. ��Ӧ�����������ȥ����������������Ǵ˷�Ӧ����H
C. ��Ӧ����ܼ��ܼ�ȥ��������ܼ��ܾ��Ǵ˷�Ӧ����H
D. �����£�H2+Cl2![]() 2HCl K=5.3��1033��H2+Br2
2HCl K=5.3��1033��H2+Br2 ![]() 2HBr K=2.2��1018�����жϷǽ����ԣ�Br>Cl
2HBr K=2.2��1018�����жϷǽ����ԣ�Br>Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��ʾ�ķ�Ӧ��ϵ�У����ֲ��ﱻ��ȥ����֪2 mol��ɫ�����ĩX���ȷֽ⣬�ָ����������ɰ�ɫ����A����ɫҺ��B����ɫ����C��1 mol��X��E��G����ɫ��Ӧ��Ϊ��ɫ��

�ش��������⣺
(1)д���������ʵĻ�ѧʽ��G________��D________��
(2)д��G��C��Ӧ����D�Ļ�ѧ��Ӧ����ʽ��____________________________��
(3)д��X��E��A�����ӷ���ʽ��______________________________________��
(4)д��C��Na2O2��Ӧ�Ļ�ѧ����ʽ��_____________________________������0.2 mol Na2O2�μӷ�Ӧ����ת�Ƶĵ�����ĿΪ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com