
(12分)在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650 mg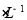 。现用氯氧化法处理,发生如下反应(其中N均为一3价、O均为-2价):
。现用氯氧化法处理,发生如下反应(其中N均为一3价、O均为-2价):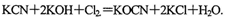 该反应中,被氧化的元素是___________.
该反应中,被氧化的元素是___________.
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气。请用单线桥法标出电子转移方向和数目: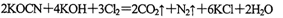
(3)若处理上述废水20.0 L,使KCN完全转化为无毒物质,至少需液氯___________g.
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是___________.
a.NH3 b.HI c.SO2 d.CO2
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中—种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:________.(已知:氯元素最高化合价为+7价)
(1)C 
(3)35.5 (4)b (5) 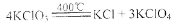
【解析】
试题分析:(1)在KCN+2KOH+Cl2 KOCN+2KCl+H2O反应中,氯元素价态降低,H、N、O、K四种元素的价态没变,只有碳元素的价态升高,被氧化的为碳元素;
KOCN+2KCl+H2O反应中,氯元素价态降低,H、N、O、K四种元素的价态没变,只有碳元素的价态升高,被氧化的为碳元素;
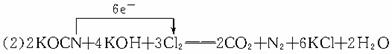
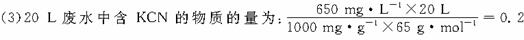 mol,由两步反应的化学方程式得出关系式:2KCN~5Cl2,所以需氯气:0.2 mol×5/2=0.5 mol,即35.5 g
mol,由两步反应的化学方程式得出关系式:2KCN~5Cl2,所以需氯气:0.2 mol×5/2=0.5 mol,即35.5 g
(4)P2O5和浓硫酸都是酸性干燥剂,可以干燥中性气体(如CH4、O2)和酸性气体(如HCl),不能干燥碱性气体(如H2S)。 浓硫酸具有强氧化性,因此还不能干燥还原性气体(如H2S、HI),选b;
(5)一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,根据氧化还原反应原理,这两种盐为KCl、KClO4,配平可得化学方程式, 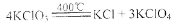 .
.
考点:考查废水的综合治理,干燥剂,化学方程式的书写。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年安徽省江淮十校高三8月联考化学试卷(解析版) 题型:选择题
某稀溶液中含有等物质的量的ZnSO4, Fe2(SO4)3, H2 SO4, CuSO4,向其中逐渐加入铁粉,溶液中Fe2+的物质的量(纵坐标/mol)和加入铁粉的物质的量(横坐标/mol)之间的关系为( )
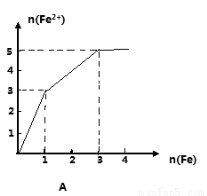
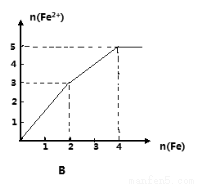
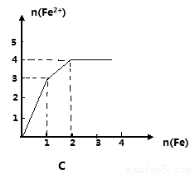
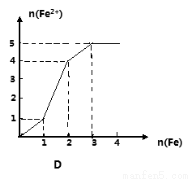
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于阿伏加德罗常数的说法不正确的是( )
A、阿伏加德罗常数是一个纯数,没有单位
B、常用NA表示阿伏加德罗常数
C、阿伏加德罗常数是一个实验值
D、阿伏加德罗常数常用:6.02×1023mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高二上学期期中考试化学试卷(解析版) 题型:选择题
一定条件下,在体积为10L的密闭容器中,1molX和1 molY进行反应:
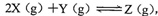 ,经60 s达到平衡,生成0.3 molZ,下列说法正确的是
,经60 s达到平衡,生成0.3 molZ,下列说法正确的是
A.以X浓度变化表示的反应速率为0.001 mol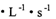
B.将容器体积变为20L,z的平衡浓度变为原来的1/2
C.若升高温度Y的转化率减小,则正反应为吸热反应
D.达到平衡时,X与Y的浓度相等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高二上学期期中考试化学试卷(解析版) 题型:选择题
1 molC与1mol水蒸气反应生成l mol CO和1 mol H2,需要吸收131.5 kJ的热量,则该反应的反应热是

查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高一上学期期中化学试卷(解析版) 题型:选择题
设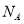 为阿伏伽德罗常数的值。下列说正确的是
为阿伏伽德罗常数的值。下列说正确的是
A.高温下,0.2molFe与足量稀硫酸反应反应,生成的H2分子数目为0.3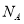
B.2 L0.5 mol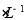 硫酸钾溶液中阴离子所带电荷数为
硫酸钾溶液中阴离子所带电荷数为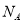
C.C2H4和N2组成的42g混合气体中原子的个数为3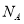
D.  反应中,生成28gN2 时,转移的电子数目为3.75
反应中,生成28gN2 时,转移的电子数目为3.75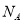
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高一上学期期中化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式书写不正确的是
A.碳酸钙与盐酸的反应: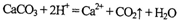
B.等物质的量的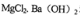 和HCl溶液混合:
和HCl溶液混合: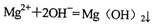
C.氧化铜与稀H2SO4反应:
D.金属钠跟水反应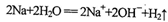
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川邛崃市高二上学期第一次月考化学试卷(解析版) 题型:填空题
下列表格是周期表的一部分,其中的序号对应的是元素,请回答下列问题:
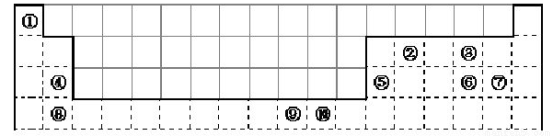
按原子轨道的重叠方式看,元素①和②形成的相对分子质量最小的分子中,含_______键;元素①和③形成化合物有漂白作用的电子式_______。
(2)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的气态化合物分子的空间构型为:_______。
(3)比⑨号元素原子序数少2的元素通常情况下能形成两种离子,其离子符号分别是_______、_______,其中较稳定的是_______,其原因是____________________________。
(4)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是_______(填元素符号)。
(5)元素⑩在周期表中的位置为_______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:选择题
下面的排序不正确的是
A.熔点由低到高:CH4<SiH4<GeH4<SnH4
B.熔点由高到低:Rb>K>Na
C.硬度由大到小:金刚石>碳化硅>晶体硅
D.晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com