
| A、碱式滴定管没有润洗会使测定含量偏低 |
| B、用移液管移取一定体积食醋时,应将移液管垂直放入稍倾斜的容器中,并将尖嘴贴紧容器 |
| C、该实验应用甲基橙作指示剂 |
| D、如果氢氧化钠溶液滴加过量,只能重新实验 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
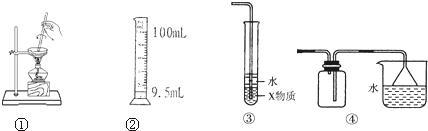
| A、装置①是把饱和食盐水中的食盐提取出来 |
| B、装置②用100mL量筒量取9.5mL液体 |
| C、装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D、装置④可用于收集NH3,并吸收多余的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
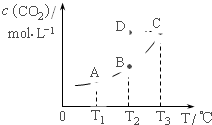 在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图.下列说法错误的是( )
在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图.下列说法错误的是( )| A、平衡状态A与C相比,平衡状态A的c(CO)小 |
| B、在T2时,若反应处于状态D,则一定有V正<V逆 |
| C、反应CO(g)+H2O(g)?CO2(g)+H2(g) 的△H>0 |
| D、若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
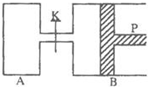 图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.
图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、用已知浓度的盐酸滴定未知浓度的NaOH溶液时,酸式滴定管未用同浓度盐酸润洗,将导致测定结果偏高 |
| D、检验某溶液是否含有SO42-时,应取少量该溶液,加入盐酸酸化的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 50 g | 20 g | 20 g | 10 g | 5 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com