
【题目】一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
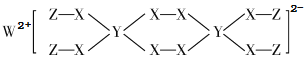
A.工业上通过电解熔融的WX来制得W
B.Z、X两元素形成的某种化合物可做消毒剂
C.Y的最高价氧化物对应水化物为强酸
D.该漂白剂中各元素均满足8电子稳定结构
【答案】B
【解析】
W、Y、Z为不同周期不同主族的短周期元素,说明有一种元素为H,根据图示结构可知,W形成+2价阳离子,X形成2个共价键,Y可以形成4个单键,Z形成1个共价键,则Z为H元素,W位于ⅡA族,X位于ⅥA族;W、X对应的简单离子核外电子排布相同,则W为Mg,X为O元素;W、Y、Z的最外层电子数之和等于X的最外层电子数,Y的最外层电子数为6-2-1=3,Y与H、Mg不同周期,则Y为B元素,Y位于ⅢA族,据此分析解答。
根据上述分析可知,W为Mg,X为O,Y为B,Z为H元素
A.MgO熔点较高,工业上通过电解熔融氯化镁获得镁,A选项错误;
B.H和O元素形成的化合物H2O2俗称双氧水,具有强氧化性,常用作医疗上的消毒剂,B选项正确;
C.Y为B,B的最高价氧化物对应水化物H3BO3为弱酸,C选项错误;
D.该漂白剂中H元素不满足8电子稳定结构,D选项错误;
答案选B。


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】(1)25℃时,相同物质的量浓度的下列溶液中:①NaCl②NaOH③H2SO4④(NH4)2SO4,其中水的电离程度由大到小顺序___(填序号)。
(2)25℃时,体积相同,浓度均为0.2mol·L-1的氨水和NaOH溶液,分别加水稀释10倍,溶液的pH分别变成m和n,则m与n的关系为___;常温下,pH=12的NaOH溶液与pH=2的硫酸,若等体积混合后,溶液的pH为___;
(3)用离子方程式解释碳酸钠溶液呈碱性的原因:___。
(4)能证明CH3COOH是弱酸的事实是___。
A.CH3COOH易挥发
B.常温下,0.1mol·L-1CH3COONa溶液的pH大于7
C.醋酸不易腐蚀衣服
D.pH=3的CH3COOH溶液稀释10倍,溶液pH<4
E.等体积等浓度的CH3COOH溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
F.将一定量的CH3COOH溶液加入Na2CO3溶液中,有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为( )

A. 3∶3∶2B. 3∶2∶1
C. 1∶1∶1D. 3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是天然气的主要成分,以A为原料可以得到B、C、D、E、F其转化关系如下图所示,已知烃B是相同状态下氢气密度的13倍,C是有刺激性气味的液体,F具有芳香气味,B、C、D、E具有相同的碳原子数。
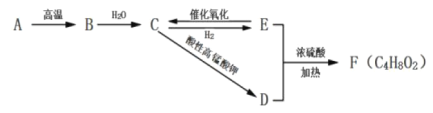
(1)B的分子式为____________。
(2)有机物E中含氧官能团的名称是____________。
(3)![]() 属于羧酸的同分异构体有____________种。
属于羧酸的同分异构体有____________种。
(4)下列说法正确的是___________。
A.有机物E与钠反应比水与钠反应要剧烈
B.有机物D、E、F可以用饱和碳酸钠溶液鉴别
C.有机物B、C、E均能使酸性高锰酸钾溶液退色
D.实验室制备F时,浓硫酸主要是吸水剂和催化剂
(5)写出E生成C的化学方程式___________。
(6)写出D和E生成F的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于四个“封管实验”![]() 夹持装置未画出、I2固体易升华
夹持装置未画出、I2固体易升华![]() 的说法正确的是( )
的说法正确的是( )

A.加热时,①中封管内固体消失
B.加热时,②中溶液变为无色,冷却后又变红
C.加热时,③中溶液变红,冷却后红色褪去,体现SO2的氧化性
D.加热又冷却的过程中,①④属于物理变化,②③属于化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的浓硝酸与足量铜在烧杯中充分反应,产生NO2、N2O4和NO的混合气体,这些气体若与1.12LO2(标准状况)混合后通入水中,则气体被水完全吸收。若继续向烧杯中加入5mol·L-1H2SO4溶液100mL,剩余的铜恰好被溶解,则Cu的总质量为( )
A.9.6gB.19.2gC.24gD.25.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的下列各组混合物完全燃烧生成CO2的质量由大到小是( )
①C2H6 C3H8 ②C3H4 C3H6 ③C3H6 C2H4 ④C4H10 C3H8 ⑤C2H2 C3H4
A. ⑤②③④①B. ②③⑤④①C. ①②③④⑤D. ⑤②③①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①Ca(ClO)2的名称为____________;
②磁铁矿主要成分的化学式为____________。
(2)请按要求完成相应的方程式:
①金属镁在二氧化碳中燃烧的化学方程式____________。
②铜与浓硫酸混合加热的化学方程式____________。
③用离子方程式说明用磨合玻璃塞的试剂瓶不可装NaOH溶液的原因:____________。
④用FeCl3溶液与铜反应制作印刷电路板的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空。
(1)100ml0.1mol/L的Na2SO4溶液中所含Na+的数目为___。
(2)同温同压下,同体积的甲烷和二氧化碳分子数之比为___,密度之比为___。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为__,R的相对原子质量为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com