
【题目】A是天然气的主要成分,以A为原料可以得到B、C、D、E、F其转化关系如下图所示,已知烃B是相同状态下氢气密度的13倍,C是有刺激性气味的液体,F具有芳香气味,B、C、D、E具有相同的碳原子数。
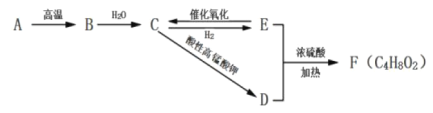
(1)B的分子式为____________。
(2)有机物E中含氧官能团的名称是____________。
(3)![]() 属于羧酸的同分异构体有____________种。
属于羧酸的同分异构体有____________种。
(4)下列说法正确的是___________。
A.有机物E与钠反应比水与钠反应要剧烈
B.有机物D、E、F可以用饱和碳酸钠溶液鉴别
C.有机物B、C、E均能使酸性高锰酸钾溶液退色
D.实验室制备F时,浓硫酸主要是吸水剂和催化剂
(5)写出E生成C的化学方程式___________。
(6)写出D和E生成F的化学方程式___________。
【答案】![]() 羟基 2 BCD
羟基 2 BCD 
![]()
【解析】
A是天然气的主要成分,则A为CH4;已知烃B是相同状态下氢气密度的13倍,则B的摩尔质量为:![]() ,B为CH≡CH; F是在浓硫酸并加热条件得到的具有芳香气味物质,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH、C为CH3CHO。
,B为CH≡CH; F是在浓硫酸并加热条件得到的具有芳香气味物质,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH、C为CH3CHO。
(1) A是天然气的主要成分,则A为CH4;已知烃B是相同状态下氢气密度的13倍,则B的摩尔质量为:![]() ,B为CH≡CH ,B的分子式为
,B为CH≡CH ,B的分子式为 ![]() ,故答案为:
,故答案为:![]() ;
;
(2) F是在浓硫酸并加热条件得到的具有芳香气味物质,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH,有机物E中含氧官能团的名称是羟基,故答案为:羟基;
(3)![]() 属于羧酸的同分异构体可用取代基法判断,结构简式改为
属于羧酸的同分异构体可用取代基法判断,结构简式改为![]() ,由于丙基有2种情况,故
,由于丙基有2种情况,故![]() 属于羧酸的同分异构体有2种;
属于羧酸的同分异构体有2种;
(4)下列说法正确的是。
A.E为CH3CH2OH,水与钠反应比乙醇与钠反应要剧烈,A错误;
B.D为CH3COOH、E为CH3CH2OH、F为CH3COOC2H5,有机物D、E、F三者遇到饱和碳酸钠溶液现象分别为:出现气泡、互溶、分层,可以鉴别三者,B正确;
C.有机物B为CH≡CH、C为CH3CHO、E 为CH3CH2OH,三者均能使酸性高锰酸钾溶液退色,C正确;
D.实验室制备CH3COOC2H5时,浓硫酸作用主要是吸水剂和催化剂,D正确;
故本题答案为:BCD;
(5)写出E生成C的化学方程式。
(6) CH3COOH与CH3CH2OH在浓硫酸做催化剂的条件下生成CH3COOC2H5的化学方程式为:![]()


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是

A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氟气混合在黑暗处即可爆炸并放出大量的热。在反应过程中,断裂![]() 中的化学键消耗的能量为
中的化学键消耗的能量为![]() ,断裂
,断裂![]() 中的化学键消耗的能量为
中的化学键消耗的能量为![]() ,形成
,形成![]() 中的化学键释放的能量为
中的化学键释放的能量为![]() ,下列关系式中,一定正确的是( )
,下列关系式中,一定正确的是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分,扇面的18折相当于中学化学常见长式元素周期表的18列,1、2、3、4相当于周期,针对表中所给元素,对照中学化学常见长式元素周期表,回答下列问题:
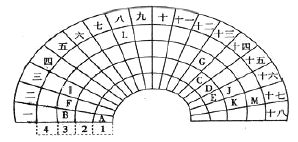
(1)表中金属性最强的元素在长式元素周期表中的位置是___________,该元素单质与水反应的化学方程式为______________。
(2)表中最高价氧化物对应的水化物酸性最强的是__________(填酸的化学式)。
(3)元素F与K形成化合物的电子式为__________。
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式_________。
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如下图所示。步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
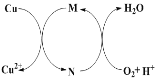
下列有关说法正确的是
A. a、b、c 之间的关系式为:a=b+c
B. 图中M、N分别为Fe2+、Fe3+
C. 步骤1充分反应后,加入少量CuO是为了除去Fe3+
D. 若制备1 mol的CuCl2,理论上消耗11.2 LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
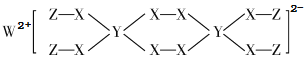
A.工业上通过电解熔融的WX来制得W
B.Z、X两元素形成的某种化合物可做消毒剂
C.Y的最高价氧化物对应水化物为强酸
D.该漂白剂中各元素均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种常见物质中均含有同一种元素,它们之间有如图所示的转化关系(部分反应物质已略去)。下列说法不正确的是
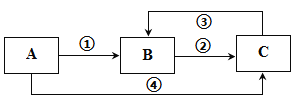
A. 若A是一种两性氧化物,则B的水溶液可呈酸性,C的水溶液可呈碱性
B. 若A为一种金属单质时,则反应①、②、③均可为化合反应,反应④可为置换反应
C. 若A、B、C是三种不同类别的固态物质,则B可以是工业上制取A、C的原料
D. 若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液pH<7,则将C通入A溶液中,pH值先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。

下列说法不正确的是
A. 异戊二烯所有碳原子可能共平面
B. 可用溴水鉴别M和对二甲苯
C. 对二甲苯的一氯代物有2种
D. M的某种同分异构体含有苯环且能与钠反应放出氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com