
【题目】有机化合物在人类生活和生产中必不可少,下列对有机化合物的叙述不正确的是
A.淀粉、蛋白质均属于高分子化合物,油脂不属于高分子化合物
B.乙醇的分子式为![]() ,常温下是一种无色液体,密度比水小
,常温下是一种无色液体,密度比水小
C.乙酸的结构简式是![]() ,能和水以任意比互溶,酸性比碳酸强
,能和水以任意比互溶,酸性比碳酸强
D.乙烯是重要的化工原料,能使溴水和酸性高锰酸钾溶液褪色,具有漂白作用
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中原子数相同的是( )
A.2LCO和2LN2
B.9gH2O和标准状况下11.2LCO2
C.标准状况下1molO2和22.4LH2O
D.0.2molNH3和4.48LHCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或装置正确的是
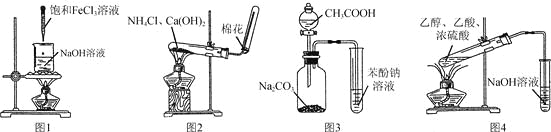
A.利用图1所示操作制备氢氧化铁胶体
B.利用图2所示装置制取NH3
C.利用图3所示装置证明H2CO3酸性强于苯酚
D.利用图4所示装置制备乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”(IYPT2019)。我国华东师范大学80后科学家姜雪峰教授被遴选为硫元素的代言人。其课题组运用“从无机硫向有机硫”转化的理念,构建起了“3S绿色硫化学”。下列有关S的说法正确的是( )
A.位于元素周期表中第三周期第VA族
B.硫元素原子结构示意图: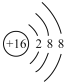
C.![]() S原子的中子数是32
S原子的中子数是32
D.有机化合物中可能含有硫元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业为人类解决粮食问题做出了巨大贡献.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )
A. N2、H2完全转化为NH3 B. N2、H2、NH3在容器中共存
C. 反应已达到化学平衡状态 D. N2、H2、NH3的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是
A.反应⑴和⑵均为氧化还原反应
B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移7mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇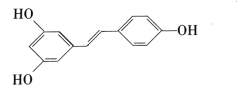 广泛存在于食物(如桑葚、花生,尤其是葡萄)中,它具有抗癌性。请回答下列问题。
广泛存在于食物(如桑葚、花生,尤其是葡萄)中,它具有抗癌性。请回答下列问题。
(1)白藜芦醇的分子式为_____,所含官能团的名称为_____;
(2)下列关于白藜芦醇的说法正确的是_____
A.可使酸性KMnO4溶液褪色
B.可与FeCl3溶液反应显紫色
C.可使溴的CCl4溶液褪色
D.可与NH4HCO3溶液反应产生气泡
E.属于醇类
F.不能发生酯化反应
(3)1mol该有机物最多能消耗____molNaOH,最多能消耗_____molBr2;
(4)1mol该有机物与H2加成时,最多消耗标准状况下的H2的体积为_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学利用如图所示装置探究二氧化硫气体的性质。

请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是__。
(2)当观察到②中溶液颜色变浅时,①中的现象是__。
(3)②中的溶液颜色变浅,说明二氧化硫具有的性质是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com