
【题目】碘化钠是一种白色结晶粉末,医疗上可用于甲状腺肿瘤防治剂、祛痰剂等。实验室用NaOH、单质碘和水合肼为原料制得,部分装置如下图所示。

实验步骤如下:
步骤①向三口烧瓶中加入8.2 gNaOH及30 mL水,搅拌冷却。
步骤②向制得的NaOH溶液中加入25.4 g单质碘,开动磁力搅拌器,保持6070℃至反应充分。
步骤③向步骤②所得溶液中加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得Nal溶液粗品和空气中常见的某气体。
步骤④向溶液③中加入1.0 g活性炭,煮沸半小时,然后将溶液与活性炭分离。
步骤⑤蒸发浓缩、结晶、过滤及干燥得产品24.3 g。
(1)步骤②温度不宜超过70℃的原因是__________;该步骤反应完全的现象是___________。
(2)步骤③N2 H4·H2O还原NaIO3的化学方程式为_______________。
(3)步骤④加入活性炭的目的是________;“将溶液与活性炭分离”的方法是__________。
(4)本次实验成品率为________。
【答案】 防止碘升华 无固体残留且溶液接近无色 3N2H4·H2O+2NaIO3=2NaI+3N2↑+9H2O 脱色(将多余的I2吸附除去) 趁热过滤 80.46%(81.0%也正确)
【解析】本题考查常见无机物质的制备实验的知识点。根据原料、反应原理、实验步骤可知:碘单质与NaOH溶液在6070℃反应生成NaIO和NaIO3,然后用N2H4·H2O(水合肼)将NaIO和NaIO3还原得到粗产物Nal,里面含有杂质碘单质,用活性炭吸附多余的碘单质进行脱色,趁热过滤,蒸发浓缩、结晶、过滤得到产品NaI。
(1)温度过高碘单质容易升华,影响产物的产率,答案为:防止碘升华;碘单质在水中溶解度很小,不能完全溶解,溶解的一部分溶液呈褐色,判断反应完全的标志是:无固体残留且溶液接近无色 。
(2)NaIO3与N2H4·H2O发生氧化还原反应色生成NaI和N2等产物,方程式为:3N2H4·H2O+2NaIO3=2NaI+3N2↑+9H2O
(3)实际反应中I2单质未完全反应,NaI中混有少量碘单质,导致NaI溶液显褐色,活性炭具有吸附性且不溶于水,可以吸附碘单质,对产物进行脱色处理;活性炭不溶于水,可在较高温度下使用过滤的方法除去多余的活性炭。答案为:脱色(将多余的I2吸附除去);趁热过滤
(4)反应物I2的物质的量为0.1mol,NaOH的物质的量为0.205mol,根据I2+2NaOH=NaI+NaIO+H2O,3I2+6NaOH=5NaI+NaIO3+3H2O,可知NaOH过量。根据I元素守恒,理论上应该得到NaI的物质的量为0.2mol,质量为0.2×150g=30g,剩余的NaOH的质量为0.205-0.1*2=0.005mol,质量为0.2g。成品率为 ![]() ×100%=80.46%。 或者作近似计算不考虑剩余的NaOH,则成品率为
×100%=80.46%。 或者作近似计算不考虑剩余的NaOH,则成品率为![]() ×100%=81%
×100%=81%


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )

①分子式为C15H12O7
②1 mol儿茶素A在一定条件下最多能与7 molH2加成
③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应,消耗金属钠和氢氧化钠的物质的量之比为1∶1
④1 mol儿茶素A与足量的浓溴水反应,最多消耗4 mol Br2
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁黑(Fe3O4)是常见的铁系颜料.一种制取铁黑的实验流程如下图所示:
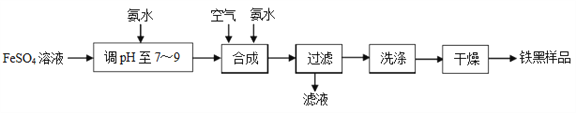
制取铁黑的反应原理可表示为Fe(OH)2+2Fe(OH)3![]() Fe(OH)2·2Fe(OH)3
Fe(OH)2·2Fe(OH)3![]() Fe3O4
Fe3O4
(1)加入氨水调pH至7~9时,发生反应的离子方程式为_______________。
(2)为了保证铁黑样品的质量,“合成”中需要控制的因素有______________(填三个)。
(3)铁黑产品中Fe3O4的含量是判断产品等级的依据之一。某铁黑样品中混有的杂质为FeO、Fe2O3中的一种。根据国标方法,进行的测定实验如下:
步骤1:称取1.908g样品置于锥形瓶中,加入足量盐酸,加热使之完全溶解。
步骤2:向锥形瓶中先加入足量的SnCl2溶液,将Fe3+全部转化为Fe2+,除去过量的Sn2+,再加入一定量的硫酸和磷酸,并滴加指示剂。
步骤3:再向锥形瓶中滴加0.08200mol·L-1K2Cr2O7溶液,发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
恰好完全反应时,共消耗50.00mL K2Cr2O7溶液。请计算样品中Fe3O4的质量分数_____________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.假说经过反复验证和修正,才发展成为科学的理论
B.模型一般可分为物体模型和思维模型
C.研究物质的性质常用观察、实验、分类、比较等方法
D.科学实验能解决化学学科的所有问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠的叙述中,正确的是( )
A. 钠是银白色金属,硬度很大
B. 将金属钠放在坩埚里用酒精灯加热,金属钠剧烈燃烧,产生黄色火焰,生成淡黄色固体氧化钠
C. 金属钠在空气中燃烧,生成过氧化钠
D. 金属钠的熔点很高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 将w g a%的NaCl溶液蒸发掉![]() g水,得到2a%的NaCl溶液
g水,得到2a%的NaCl溶液
B. 将1Lc mol/L的硫酸溶液用4L水稀释,稀释后溶液的物质的量浓度等于0.2c mol/L
C. 标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为
![]()
D. 将1.6 g CuSO4·5H2O晶体溶于水配成1L溶液,制得0.01 mol/L的CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~K有如下转化关系,E、H能与FeCl3溶液发生显色反应,I转化的产物K只有一种结构,且K能使溴的CCl4溶液褪色。
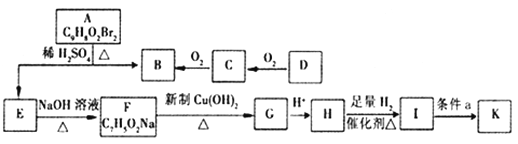
已知: D的质谱与核磁共振氢谱图如下:
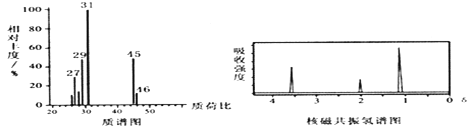
请回答下列问题:
(1)C中官能团的名称是______;H→I的反应类型是______。
(2)写出下列反应的化学方程式:
①F→G:____________。
②A与稀硫酸溶液共热的反应:____________。
(3)L是相对分子质量比H大14的同系物,L可能有______种。其中苯环上的一溴代物只有两种的L的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3﹣Na2O,O2﹣可以在其中自由移动.
下列有关叙述正确的是( )

A. 电极a的反应式为:CH4+4O2﹣﹣8e﹣=CO2+2H2O
B. 电极b是正极,O2﹣由电极a流向电极b
C. 瓦斯分析仪工作时,电池内电路中电子由电极 a流向电极b
D. 当固体电解质中有2 mol O2﹣通过时,外电路通过电子8 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com