
【题目】下列各物质中,含有极性键的原子晶体的是( )
A. 干冰 B. 石英 C. 烧碱 D. 晶体硅
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g)![]() SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________(填“增大” 、“不变”或“减小”);
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是___________mol/L;
(3)整个过程中,SO2的转化率由50%变为___________%,NO2的转化率由__________%变为___________%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将_______________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,能使电离平衡的是H2O![]() H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
A. 向水中加入NaHSO4溶液 B. 向水中加入Al2(SO4)3固体
C. 向水中加入Na2CO3溶液 D. 将水加热到100℃,使pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g)2SO3(g),平衡混合体系中 SO3的百分含量和温度的关系如图1所示,根据图1回答下列问题:
①2SO2(g)+O2(g)2SO3(g)的△H____0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是____.
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4mol 电子,同时消耗2mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)2NH3(g).图2表示在此反应过程中的能量的变化,图3表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图4表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.
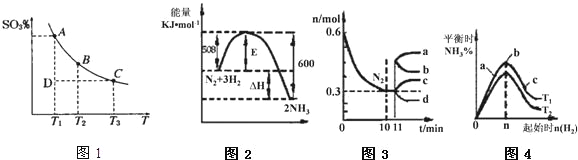
①该反应的平衡常数表达式为_____,升高温度,平衡常数______(填“增大”或“减小”或“不变”).
②由图2信息,计算0~10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为______(填“a”或“b”或“c”或“d”).
③图3a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是______点,温度T1______T2(填“>”或“=”或“<”).
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_____性,所得溶液中c(H+)﹣c(OH﹣)=_________________(填写表达式)(已知:H2SO3:Ka1=1.7×10﹣2,Ka2=6.0×10﹣8,NH3H2O:Kb=1.8×10﹣5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是重要的工业原料。
(1)标准状况下,将500L氨气溶与水形成1L氨水,则此氨水的物质的量浓度为______mol/L(保留三位有效数字),该氨水最多能吸收二氧化硫的体积为_________。
(2)氨的催化氧化是重要的工业生产,此反应将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为__________________。下列反应中的氨与氨催化氧化中的氨性质相同的是________________。
A.2Na+2NH3=2NaNH2+H2↑
B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O
D.HNO3+NH3=NH4NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电极的说法正确的是
A. 铜电极只能作正极 B. 电解精炼铜时,纯铜与电源正极相连
C. 原电池的负极得到电子 D. 电解池的阳极失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:则下列说法正确的是
①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1

A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要释放能量
D. 根据②推知反应H2(g) +1/2O2(g)=H2O(l):ΔH>-241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答问题:
(1)中和热的测定所需的玻璃仪器有:大小烧杯、量筒、温度计、 ;
已知:0.55 mol·L-1 HCl和0.50 mol·L-1的NaOH溶液各50 mL反应放出热量为1.42kJ,写出该反应的中和热的热化学方程式: 。
(2)101kpa时,1克乙醇(CH3CH2OH)液体完全燃烧生成稳定氧化物放出热量akJ,写出乙醇燃烧热的热化学方程式: 。
(3)已知H-H、O=O和O-H键的键能分别为436 kJ/mol、498 kJ/mol和463 kJ/mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
(4)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g ![]() CH3OH(g) ΔH=-90.7 kJ·mol-1
CH3OH(g) ΔH=-90.7 kJ·mol-1
2CH3OH(g ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g ![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为: 。
(5)① 25℃时,浓度均为0.1 mol/L的①氨水②氢氧化钠溶液③盐酸溶液④醋酸溶液,其c(H+)由大到小排列的顺序为: (用序号填空)。
② 95℃时,水中的H+的物质的量浓度为10-6 mol·L-1,若把0.01 mol的NaOH固体溶解于95℃水中配成1 L溶液,则溶液的pH为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.1 mol·L-1醋酸溶液10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大 ②c(CH3COOH)增大 ③CH3COO-数目增多 ④c(H+)增大
⑤导电性增强 ⑥![]() 增大 ⑦c(OH-)增大
增大 ⑦c(OH-)增大
A.①②③⑦ B.①③⑤⑥ C.①③⑥⑦ D.②④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com