
【题目】下列说法正确的是
A. 水解反应是吸热反应 B. 升高温度可以抑制盐类的水解
C. 正盐水溶液pH均为7 D. 硫酸钠水溶液pH小于7
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
属于该类的物质 | ② | ⑧⑨ |
(2)上述物质中属于非电解质的有_________;上述物质中能与盐酸反应的电解质有________(填序号)。
Ⅱ.(1)在 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O 的反应中,氧化剂是_________,还原产物是_________,氧化产物与还原产物的质量比是_________。
(2)在反应MnO2+4HCl=MnCl2+Cl2↑+2H2O中,每生成标准状况下4.48LCl2,转移的电子的物质的量为___________mol。
Ⅲ.Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程,据此回答下列问题:
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ _________+ ________![]() _________+ ________+H2O
_________+ ________+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据该反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
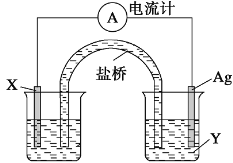
请回答下列问题:
(1) 电极X的材料是____________(写物质名称);电解质溶液Y是______________ (写化学式);
(2)银电极为电池的___________极,发生的电极反应为__________________;
X电极上发生的电极反应为_________________________________;
(3)外电路中的电子是从___________电极流向___________电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现往1L的容器中通入CO2、H2各2mol。在一定条件下让其发生反应:CO2+H2![]() CO+H2O,回答下列问题:
CO+H2O,回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的浓度为1mol·L-1。该条件下平衡常数K1=________。
(2)在(1)基础上,把体系的温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知平衡时c(H2O)=______________(保留2位有效数字)。
(3)该可逆反应的正反应为________反应(填“吸热”或“放热”)。
(4)在(1)基础上,压缩容器体积至0.5L。该条件下的平衡常数为K3。则K3________(填“大于”、“等于”或“小于”)K1,理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是

A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023
B. 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7
C. 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
D. 一定条件下反应N2+3H22NH3达到平衡时,3v正(H2)=2v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,可用离子方程式H++OH-= H2O表示的是
A.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
B.Mg(OH)2+2HCl==MgCl2+2H2O
C.NaOH+NaHCO3==Na2CO3+H2O
D.NaOH+HNO3==NaNO3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com