
【题目】下列实验操作能达到实验目的的是
A. 常温常压下,用铁和浓硫酸制取SO2气体
B. 用酸性高锰酸钾溶液鉴别环己烷和甲苯
C. 用饱和碳酸氢钠溶液除去O2中混有的少量HCl气体
D. 用分液漏斗分离苯和四氯化碳
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]X、Y、Z、W是前四周期中常见的四种元素。X的基态原子核外电子共占据5个原子轨道,其中能量最高的能级上的电子有3种运动状态;Y能形成最强的无机含氧酸,Z的单质是前36号元素中最活泼的金属单质,W的一种核素的质量数是56,中子数是30。
(1)W的稳定价态离子的核外电子排布式为_________,Y、Z、W电负性由大到小的顺序为___________(填元素符号)。
(2)X与同周期相邻的另外两种元素相比其第一电离能最大,原因是_____________________X和与X同族的另外两种前四周期元素的简单氢化物的沸点由低到高的顺序为_______________,试解释其原因__________________
(3)XY3的中心原子轨道杂化类型为_________
(4)已知WY3的沸点为319 ℃,熔点为306 ℃,则WY3的晶体类型为____________Z的重要化合物Z2O2中存在的化学键类型有_______________
A.离子键 B.极性共价键 C.非极性共价键 D.π 键
(5)若Z的晶胞为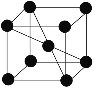 ,Z离子的半径为d cm,则Z单质的密度为_______。
,Z离子的半径为d cm,则Z单质的密度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
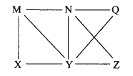
A. N一定是HCl(aq) B. X可能为Al或Cl2
C. Y一定为NaOH(aq) D. Q、Z中的一种必定为Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol·L-1、体积均为V0的MOH和ROH分别加水稀释至体积V,pH随lg![]() 的变化如图所示,下列叙述错误的是
的变化如图所示,下列叙述错误的是
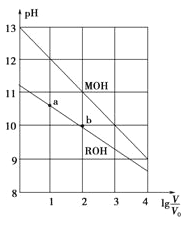
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是( )
A. 实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓)![]() Mn2++2Cl﹣+Cl2↑+2H2O
Mn2++2Cl﹣+Cl2↑+2H2O
B. Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C. 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42﹣+Ba2++2OH﹣=2H2O+BaSO4↓
D. 向次氯酸钠溶液中通入SO2:2ClO+SO2+H2O=SO32-+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用)。
查阅资料知:氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2和HCl。
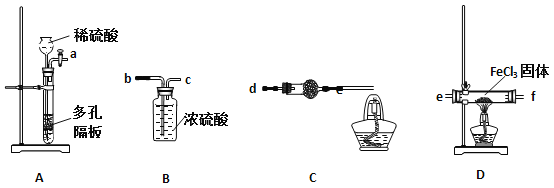
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法: 。
(2)气流从左至右,装置接口连接顺序是:
a→ ( )→( )→( )→( )→( )
(3)装置C中干燥管中所盛试剂为碱石灰,其作用是: 、
用上述方法制得的氯化亚铁中可能含有氯化铁,某同学设计了如下实验,测定样品中铁元素的质量分数x.请按要求回答下列问题:
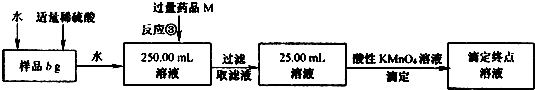
(4)反应③的离子方程式为__ ___.
(5)若3次平行滴定实验,平均消耗c mol/L KMnO4溶液的体积为d mL,则样品中铁元素的质量分数(化简代数式)x=_____________;若样品溶解仍使用盐酸而不改用稀硫酸,则所得样品中铁元素的质量分数将(填“偏大”、“偏小”或“无影响”)____ _________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 元素的电负性越大,其单质越稳定
B. 分子晶体中可能不存在共价键
C. 晶格能越大,形成的离子晶体越稳定
D. 金属晶体和离子晶体均具有延展性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,且为18电子微粒;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如图所示(某些条件已略去)。请用化学用语回答下列问题:

(1)A在元素周期表中的位置
A、B单质对应元素的简单离子半径由大到小的顺序为 。
(2)丙的电子式为 ,丁中所包含的化学键类型有 (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(3)甲和水反应生成戊和丙的化学方程式为 。
(4)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC)。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为 。
(5)已知另有物质己为中学常见黑色磁性氧化物,能够与A在一定条件下发生反应,实验测得与A反应的焓变(△H)和活化能(Ea)。下列能量关系图合理的是 (填写序号)。
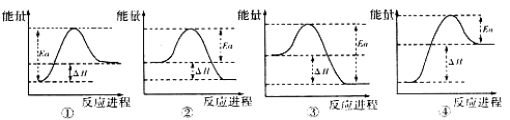
(6)资料显示物质己可用于除去地下水中的TcO4— (99Tc具有放射性)。在弱酸性条件下,物质己将TcO4— 转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用碳酸钡或硫酸钡做钡餐
B.药物能治疗疾病,故多吃点没关系
C.鸦片、吗啡、海洛因等毒品危害极大,没有任何益处
D.为了预防、治疗疾病,家庭应自备一些常用的非处方药,以供急用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com