
【题目】根据合成氨反应的能量变化示意图,下列有关说法正确的是( )
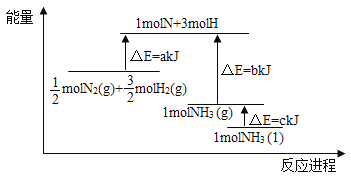
A. 若合成氨反应使用催化剂,反应放出的热量增多
B. 断裂0.5moIN2(g)和1.5molH2(g)中所有的化学键释放akJ热量
C. 2NH3(l)= N2(g)+3H2(g) △H=2(b+c-a) kJ/mol
D. N2(g)+3H2(g)=2NH3(g) △H=-2(a-b)kJ/mol
科目:高中化学 来源: 题型:
【题目】2005年法拉利公司发布的敞篷车(法拉利Superamerica),其玻璃车顶采用了先进的电致变色技术,即在原来玻璃材料基础上增加了有电致变色系统组成的五层膜材料(如图所示)。其工作原理是:在外接电源(外加电场)下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。下列有关说法中不正确的是( )
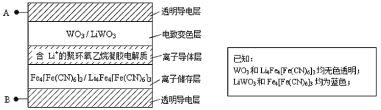
A.当A外接电源正极时,Li+脱离离子储存层
B.当A外接电源负极时,电致变色层发生反应为:WO3+Li++e-=LiWO3
C.当B外接电源正极时,膜的透过率降低,可以有效阻挡阳光
D.该电致变色系统在较长时间的使用过程中,离子导体层中Li+的量可保持基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化物是一类重要的化工原料,具有广泛的用途。完成下列填空:
(1)Na2S溶液中,水的电离程度会_________(填“增大”、 “减小”或“不变”);微热该溶液, pH 会_________(填“增大”、 “减小”或“不变”)。
(2)Na2S 溶液中各离子浓度由大到小的顺序为: ___________________________________。
(3)向 Na2S 和 Na2SO3 的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
__ Na2S+ __ Na2SO3+__ H2SO4→__ Na2SO4+__ S↓+ __ H2O
①配平上述化学方程式,标出电子转移的方向和数目______。
②反应中被氧化的元素是______________。
(4)CuS和FeS都是难溶于水的固体,工业上可用 FeS 将废水中的 Cu2+转化为CuS除去,请结合相关原理进行解释:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH![]() 、Cl-、AlO
、Cl-、AlO![]() 。当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是
。当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是
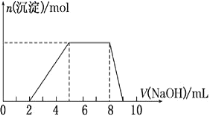
A.原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH![]()
B.反应最后形成的溶液中的溶质含AlCl3
C.原溶液中Al3+与NH![]() 的物质的量之比为1∶3
的物质的量之比为1∶3
D.原溶液中含有的阴离子是Cl-、AlO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列10种物质①熔融的氢氧化钠②蔗糖③纯净的盐酸④金属钠⑤硫酸⑥二氧化硫⑦硫粉⑧偏铝酸钠溶液⑨酒精溶液⑩液氨(注意:下面前三问的答案请填序号!)
(1)属于电解质的有__。
(2)属于非电解质的有__。
(3)上述状态下的电解质能导电的有__。
(4)偏铝酸钠溶液中通足量二氧化碳反应的离子方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是
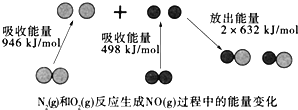
A. 该反应的热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180kJ·mol﹣1
B. 1mol N2(l)和NA个O2(l)反应生成2mol NO(g)时,吸收的能量为180kJ
C. 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量
D. 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下,分别测得反应2SO2(g)+O2(g)![]() 2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
A. υ(SO2)=4 mol·L-1·min-1B. υ(O2)=3 mol·L-1·min-1
C. υ(SO2)=0.1 mol·L-1·s-1D. υ(O2)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
元素 | 信息 |
Q | 地壳中含量第2的元素 |
W | 最高正化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色反应为紫色 |
Z | 原子结构示意图为 |
(1)Q在元素周期表中的位置是___________。
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是___________。(填化学式)
(3)金属性Y强于X,用原子结构解释原因:___________,失电子能力Y大于X。(用元素符号回答问题)
(4)下列对于Z及其化合物的推断中,正确的是___________(填序号)。
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用小轿车(燃油汽车)中的动力和能量与化学反应息息相关。
(1)用C8H18代表汽油分子,写出汽油完全燃烧的化学方程式_____。
(2)关于汽油在气缸中燃烧反应的叙述正确的是_____
A.汽油具有的总能量高于生成物二氧化碳和水具有的总能量
B.汽油燃烧过程中,化学能转化为热能
C.断裂汽油和氧气分子中化学键吸收的能量小于生成碳氧化物和水中化学键放出的能量
D.汽车尾气中含NO的原因是汽油中含有氮元素,燃烧后生成NO
(3)汽车中的电瓶为铅酸电池,Pb+PbO2 +2H2SO4![]() PbSO4+2H2O,已知PbSO4难溶于水,下列说法正确的是_____
PbSO4+2H2O,已知PbSO4难溶于水,下列说法正确的是_____
A. 放电时,负极的电极反应式为:Pb-2e-=Pb2+
B.放电时,正极得电子的物质是PbO2
C.放电时,理论上每消耗20.7g铅,外电路中转移的电子为0.4mol
D.充电是使放电时的氧化还原反应逆向进行
(4)研究氢氧燃料电池中,H2所在的电极为_____极(填“正”或“负”),电极反应式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com