
【题目】完成如下有关硫的化合物的问题。
(1)硫化物与充足的氧气反应会转化为SO2,写出硫化铝在充足的空气中灼烧的反应方程式________________________________________________。
(2)SO2作为一种化学性质活泼的物质,它能发生多种反应,请按照下表提示,从不同角度梳理SO2的化学性质,将化学方程式填在下表中。
SO2性质梳理 | 化学方程式 | |
物质 类别 | 酸性 氧化物 | SO2+H2O |
SO2+CaO=CaSO3 | ||
①______ | ||
S元素 价态 | S为 +4价 | ②______ |
SO2 +2H2S=3S+2H2O | ||
(3)在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成。
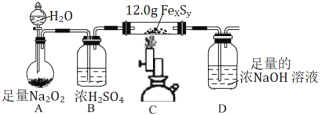
实验步骤:
步骤Ⅰ 如图连接装置,检查装置气密性,装入药品;
步骤Ⅱ 打开A的滴液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间;
步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
步骤Ⅴ 取25.00 mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66 g。
请回答:
①经测定,步骤Ⅳ所得溶液呈强碱性,其中含有的溶质除NaOH外,还可能有______(填化学式)。
②步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为__________。
③在C、D装置之间不需要防倒吸装置的理由是_____________________________。
④步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有________________。
⑤FexSy的化学式为______________。
【答案】2Al2S3+9O2 ![]() 2Al2O3+6SO2SO2+2NaOH=Na2SO3+H2OSO2+H2O2=H2SO4Na2SO3与Na2SO4继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收SO2中含不溶于NaOH溶液的O2250mL容量瓶、胶头滴管FeS2
2Al2O3+6SO2SO2+2NaOH=Na2SO3+H2OSO2+H2O2=H2SO4Na2SO3与Na2SO4继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收SO2中含不溶于NaOH溶液的O2250mL容量瓶、胶头滴管FeS2
【解析】
(1)硫化物与充足的氧气反应会转化为SO2,因此硫化铝在充足的空气中灼烧生成二氧化硫和氧化铝,反应的反应方程式为2Al2S3+9O2 ![]() 2Al2O3+6SO2。
2Al2O3+6SO2。
(2)二氧化硫作为一种酸性氧化物,能与碱反应生成盐和水,反应的方程式为SO2+2NaOH=Na2SO3+H2O;+4价的硫能被氧化为+6价,例如SO2+H2O2=H2SO4;
(3)①反应生成的二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,亚硫酸钠不稳定易被氧化为硫酸钠,则步骤Ⅳ所得溶液的溶质除NaOH外,还可能有Na2SO3与Na2SO4;
②过氧化钠与水反应生成氧气,则步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间的目的为继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收。
③由于SO2中含不溶于NaOH溶液的O2,因此在C、D装置之间不需要防倒吸装置;
④步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有250mL容量瓶、胶头滴管;
⑤4.66g沉淀是硫酸钡,物质的量是0.02mol,根据硫原子守恒可知S元素的物质的量是0.02mol,质量是0.02mol×32g/mol=0.64g;所以12g硫化物中Fe的质量是12g-0.64g×250mL/25mL=5.6g,物质的量是0.1mol,因此x:y=0.1:0.2=1:2,所以FexSy的化学式为FeS2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法,可以表明反应N2 + 3H2![]() 2NH3已达到平衡的标志是
2NH3已达到平衡的标志是
A. 1molN≡N键断裂的同时,有6molN-H键形成
B. 1molN≡N键断裂的同时,有3molH-H键断裂
C. 1molN≡N键断裂的同时,有3molH-H键形成
D. 1molN≡N键断裂的同时,有2molN-H键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙基丹皮酚肟胺基醇醚衍生物(H)具有很好的抗血小板聚集活性,是良好的心脑血管疾病的治疗药物。
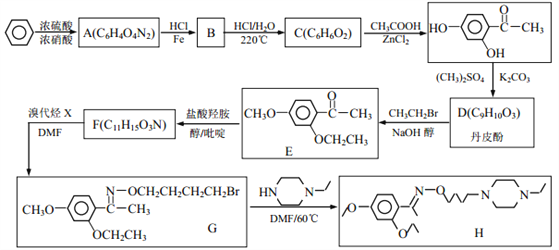
已知:①![]()
②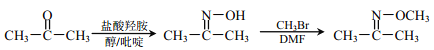
③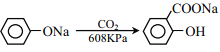
请回答:
(1)E中含有的官能团名称为_________;
(2)丹皮酚的结构简式为_________;
(3)下列说法不正确的是(___)
A.乙基丹皮酚肟胺基醇醚衍生物 H 的分子式为 C21H34O3N3
B.物质B 可能溶于水,且能与盐酸反应生成有机盐
C. D→E 和 G→H 的反应类型均为取代反应
D.物质 C 能使浓溴水褪色,而且 1mol C 消耗 2molBr2
(4)写出 F→G 的化学方程式_________。
(5)写出满足下列条件 F 的所有同分异构体的结构简式_________。
①能发生银镜反应;1molF 与 2molNaOH恰好反应。
②1H-NMR 谱显示分子中含有 5 种氢原子; IR 谱显示有-NH2,且与苯环直接相连。
(6)阿司匹林也具有抑止血小板凝聚的作用。结合题给信息,请以硝基苯和乙酸酐为原料设计合理的路线制备阿司匹林(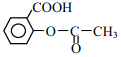 )。(用流程图表示,无机试剂任选)______。
)。(用流程图表示,无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是
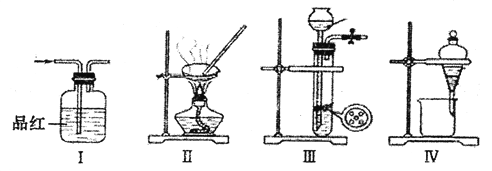
A. 将装置I中通入C12和SO2的混合气体,然后加热褪色后的溶液,据溶液是否变红来证明SO2的是否存在
B. 用装置Ⅱ来蒸发浓缩CuSO4溶液,并通过冷却结晶、过滤的方法获得胆矾晶体
C. 用浓氨水和块状固体NaOH在装置III中作用,来快速制取NH3
D. 用装置IV来分离乙醇萃取碘水后的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①MgSO4,②Ba(NO3)2,③NaOH,④CuCl2,⑤KCl五种溶液,不加任何其他试剂,可鉴别且鉴别的先后顺序也正确的是( )
A.④③②①⑤B.④⑤③②①C.④③①②⑤D.④②③①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是

A. 0-t1时,原电池的负极是铜片
B. 0-t1时,正极的电极反应式是2H++2e-=H2↑
C. t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应
D. tl时刻后,电子从铝经过导线流向铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同化学元素所组成的化合物,以下说法不正确的是( )
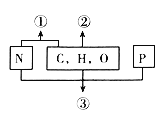
A. 若①是某种大分子的基本组成单位,则①是氨基酸
B. 若②是生命活动的主要能源物质,则②是糖类
C. 若②是细胞中的储能物质,则②一定是脂肪
D. 若③是携带遗传信息的大分子物质,则③一定是核酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com