
����Ŀ��ij�¶�ʱ��Ag2SO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ�����¶��£�����˵����ȷ����
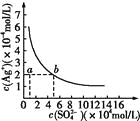
A. ���д���SO42-����Һ�п϶�������Ag+
B. 0.02 mol��L-1��AgNO3��Һ��0.02 mol��L-1��Na2SO4��Һ�������ϲ������ɳ���
C. Ag2SO4���ܶȻ�����(Ksp)Ϊ1��10-3
D. a���ʾAg2SO4�IJ�������Һ,��������ʹ��Һ��a��䵽b��
���𰸡�B
�����������������A��Ag2SO4��ˮ�г����ܽ�ƽ��Ϊ��Ag2SO4��s��2Ag+��aq��+SO42-��aq�����ܽ�Ϊ������̣���Һ��һ������Ag+��A����B��0.02mol/L��AgNO3��Һ��0.2mol/L��Na2SO4��Һ�������ϣ�c��SO42-��=0.1mol/Lʱ��c��Ag+��=0.01mol/L��c2��Ag+����c��SO42-��=1��10-5��ksp���������ɳ�����B��ȷ��C����ͼ���֪����c��SO42-��=5��10-2mol/Lʱ��c��Ag+��=2��10-2mol/L����ksp=[c��Ag+��] 2��[c��SO42-��]=2��10-5��C����D����������ʱ����Һ��Ag+��SO42-Ũ�ȶ�����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
��H2(g)��![]() O2(g)��H2O(l)����H����285.8 kJ��mol-1
O2(g)��H2O(l)����H����285.8 kJ��mol-1
��H2(g)��![]() O2(g)��H2O(g)����H����241.8 kJ��mol-1
O2(g)��H2O(g)����H����241.8 kJ��mol-1
��C(s)��![]() O2(g)��CO(g)����H����110.5 kJ��mol-1
O2(g)��CO(g)����H����110.5 kJ��mol-1
��C(s)��O2(g)��CO2(g)����H����393.5 kJ��mol-1��
�ش��������⣺
��1��H2��ȼ����Ϊ____________��C��ȼ����Ϊ____________��
��2��ȼ��10 g H2����Һ̬ˮ���ų�������Ϊ____________��
��3��д��COȼ�յ��Ȼ�ѧ����ʽ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
��1L0.1mol/LNH4NO3��Һ�е�ԭ����С��0.2NA
���ñ�����ζ�NaOH��Һ����Ũ��ʱ����ʽ�ζ���������ˮϴ�Ӻ�û�ñ�������ϴ��ֱ��װ������ζ�������ļ�ҺŨ��ƫ��
��pH��ȵ�������Һ��a��CH3COONa b��C6H5ONa c��NaHCO3d��NaOH��(��֪���ԣ�C6H5OH<H2CO3)����Һ���ʵ���Ũ����С����˳��Ϊ��d ��b ��c ��a
�ܸ�����ʴʱ���ܷ�����������Ӧ��2H2O+O2+4e-=4OH-
�ݵ�ⱥ��MgCl2��Һʱ����ⷴӦʽΪ��2H2O+2Cl-![]() Cl2��+H2��+2OH-
Cl2��+H2��+2OH-
���ں����������п�鱣����Dz��ܸ�ʴ�Dz�����������������������
������ʹ������泥�����������ǿ����ľ�����̬���ʲ��ܻ��ʩ��
A. �٢ڢݢ� B. �٢ۢ��� C. �ۢܢ��� D. �ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��ӦaA��g��+bB��g��![]() cC��g����H="Q" ���ܱ������н��У��ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£����������B����������w��B���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��
cC��g����H="Q" ���ܱ������н��У��ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£����������B����������w��B���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��

A. T1��T2��P1��P2��a+b��c��Q��0
B. T1��T2��P1��P2��a+b��c��Q��0
C. T1��T2��P1��P2��a+b��c��Q��0
D. T1��T2��P1��P2��a+b��c��Q��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ը��������Һ���𣬶���������ˮ������� ( )
A. �������ϩ B. 1��3һ����ϩ�Ͷ�ϩ
C. �����ұ� D. ���ͱ���ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪ��������У�����ͭ��������ᣨHN3�����ɵ�ԭ��أ��ܷ�Ӧ����ʽΪ�� 2Cu+2Cl- +HN3+3H+��2CuCl(s)+N2��+NH4+�����������������
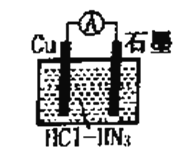
A. ���ӵ�����ΪCu��![]() ��ʯī
��ʯī
B. �����ĵ缫��ӦʽΪCu+Cl�D�De����CuCl(s)
C. ��Ӧһ��ʱ�����������Һ��pH��С
D. ��״���£�����224mL N2ʱ��ͭת�Ƶĵ�����Ϊ0.02NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȶ�ϵ������������Ư����ҵ���������ָ�ꡣ
��.������ͼװ�ã�ʡ�Լ���װ�ã���̽��Ư�۵��ȷֽ���������ʾ�������ڳ�ʪ�����е�Ư���������ɵ����������O2������Cl2��

��1�����ȸ���Ư����Ʒ���۲쵽B���д�����ɫ���ݲ������������Ʒֽ�Ĺ��������һ����________��
��2�����Ⱦ����ڳ�ʪ�����е�Ư����Ʒ���۲쵽B��Ҳ�����ݲ�����
��B�з�����Ӧ�����ӷ���ʽΪ_______��
�ڴ���ַ�Ӧ�Ͽ�����A��B����Ƥ�ܣ�ֹͣ���ȣ���ȴ������B�в��ͨ��ʵ��֤������ʱ�������������ɡ������ʵ�鷽����_________��
��. �ⶨƯ�����ȵİٷֺ���������Ʒ����Ԫ������������Ʒ�������ı�ֵ����ʵ�鲽�����£�
��ȷ��ȡ5.000 gƯ����Ʒ����ϸ��������ˮ�ܽⲢ��ȴ��ϡ����500 mL��
����ȡ25.00 mL��������Һ����ƿ�У�����pH��������������3% H2O2ˮ��Һ�����������ٲ������ݡ���������K2CrO4��Һ��Ϊָʾ������0.1000mol/L AgNO3����Һ�ζ����յ㡣���ʵ�飬�������AgNO3����Һƽ�����Ϊ25.00 mL������֪��Ksp(AgCl����ɫ)��1.56��10��10��Ksp(Ag2Cr2O4��ש��ɫ)��9.0��10��12��
��3��������У��ܽ⡢ϡ�͵Ĺ������õIJ����������ձ�����������____�� ____��
��4������H2O2ˮ��Һ�����������ٲ������ݣ�Ŀ����______�������ӷ���ʽ��ʾ����
��5���ζ��յ��������_______��
��6����Ư�����ȵİٷֺ���Ϊ__________��
��7�����в����������Ȱٷֺ����ⶨ���ƫ�ߵ���______��
A��ָʾ��K2CrO4����������
B���ڵζ��յ��ȡ�ζ��̶ܿ�ʱ�����ӱ�ҺҺ��
C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ�����ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����������ȡ��ˮ�е������ ( )
A. �ѻ����� B. ���ױ� C. �ƾ� D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӵ��������Ṥ���У�������Ӧ��450�����д��������½��У�
2SO 2��g����O2��g��![]() 2SO3��g������H=��190KJ��mol����
2SO3��g������H=��190KJ��mol����
��1)��һ���̶��ݻ�Ϊ5L���ܱ������г���0.20 mol SO2��0.10molO2������Ӻ�ﵽƽ�⣬��������к�SO38g����V(O2)= mol��L��1��min��1�������ʱ��ѧƽ�ⳣ��K1= ��
��2�����¶Ȳ��䣬����ͨ��0.20mol SO2��0.10mol SO3����ƽ���ƶ�������ԭ���� ����ƽ���ѧƽ�ⳣ��ΪK2����K1��K2֮��Ĺ�ϵΪ ���� ��>������<����=������
��3������ֻ�ܱ�����A��B��A�ܱ��ֺ��ݣ�B�ܱ��ֺ�ѹ����ʼʱ���ݻ���ȵ�A��B�зֱ�ͨ�������Ϊ2��1�ĵ�����SO2��O2��ʹ֮������Ӧ������>��=��<�����ң�����С�����䣩��
���ﵽƽ������Ҫ��ʱ�䣺t(A) t(B)
��ƽ��ʱ��SO2��ת���ʣ�a(A) a(B)
���ﵽƽ��ʱ�����������зֱ�ͨ�������Ar����B�еĻ�ѧƽ���� ��Ӧ�����ƶ���A�еĻ�ѧ��Ӧ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com