
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+![]() O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为____________;C的燃烧热为____________。
(2)燃烧10 g H2生成液态水,放出的热量为____________。
(3)写出CO燃烧的热化学方程式__________________________________。
【答案】 285.8 kJ·mol-1 393.5 kJ·mol-1 1429kJ CO(g)+ ![]() O2(g)=CO2(g) ΔH=-283.5 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.5 kJ·mol-1
【解析】(1)燃烧热是指在25℃,101 kPa时,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量为1mol,产物必须是稳定氧化物。根据燃烧热的定义,1mol H2燃烧生成液态水更稳定,所以①H2(g)+![]() O2 (g)=H2O(l);△H=﹣285.8 kJ·mol-1为H2燃烧热的化学方程式,所以H2的燃烧热为:285kJmol﹣1;1mol碳完全燃烧生成CO2时放出的热量为碳的燃烧热,④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol﹣1为碳燃烧热的化学方程式,所以碳的燃烧热为:393.5 kJ·mol-1;故答案为:285.8 kJ·mol-1;393.5 kJ·mol-1;
O2 (g)=H2O(l);△H=﹣285.8 kJ·mol-1为H2燃烧热的化学方程式,所以H2的燃烧热为:285kJmol﹣1;1mol碳完全燃烧生成CO2时放出的热量为碳的燃烧热,④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol﹣1为碳燃烧热的化学方程式,所以碳的燃烧热为:393.5 kJ·mol-1;故答案为:285.8 kJ·mol-1;393.5 kJ·mol-1;
(2)根据方程式①可知每燃烧1molH2生成H2O(l),放出热量285.8kJ,1molH2质量为2g,所以燃烧10g H2生成液态水,放出的热量为285.8kJ ×5=1429kJ。
(3)CO燃烧的化学方程式为CO(g)+ ![]() O2(g)=CO2(g),根据盖斯定律,将④﹣③即可得:CO(g)+
O2(g)=CO2(g),根据盖斯定律,将④﹣③即可得:CO(g)+ ![]() O2(g)=CO2(g) △H=-393.5kJ/mol-(-110.5 kJ/mol)= -283.5 kJ·mol-1。故答案为:CO(g)+
O2(g)=CO2(g) △H=-393.5kJ/mol-(-110.5 kJ/mol)= -283.5 kJ·mol-1。故答案为:CO(g)+ ![]() O2(g)=CO2(g) ΔH=-283.5 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.5 kJ·mol-1


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作的描述中,正确的是( )
A.从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶
B.用稀盐酸洗涤盛放过石灰水的试剂瓶
C.酒精灯不慎碰倒起火时可用水扑灭
D.各放一张质量相同的滤纸于天平的托盘上,将NaOH固体放在左盘纸上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:
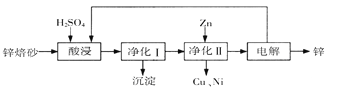
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为
(2)净化I操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式
②250C时,pH=3的溶液中,c (Fe3+)= mol/L(已知25℃,![]() 。
。
③净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是 。
(3)若没有净化II操作,则对锌的制备带来的影响是 。
(4)本流程中可以循环利用的物质除锌外还有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中,有广泛应用,它的工作原理如下:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2.下列叙述正确的是
Cd(OH)2+2Ni(OH)2.下列叙述正确的是
A. 该电池放电的时候,负极附近pH增大
B. 放电时每转移2mol电子,有2mol NiO(OH)被氧化
C. 充电时,阳极反应式是Ni(OH)2-e-+OH-=NiO(OH)+H2O
D. 充电时,Cd电极接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下某容积不变的密闭容器中,可逆反应C(s)+H2O(g)![]() CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
A. 体系的压强不再发生变化 B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时生成n mol H2 D. 1 mol H—H键断裂的同时断裂2 mol H-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃的沸点是:甲烷-164℃,乙烷-89℃,丁烷-1℃,戊烷+36℃,根据上述数据判断,丙烷的沸点可能是( )
A、低于-89℃ B、约为-42℃ C、高于-1℃ D、高于+36℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度 ②浓度 ③容量 ④压强⑤刻度线 ⑥酸式或碱式这六项中的( )
A.②④⑥
B.③⑤⑥
C.①②④
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述正确的是( )

A. 装置①工业上可用于生产金属钠,电解过程中石墨电极产生金属。
B. 装置②中阳极产生的气体可以使湿润的淀粉碘化钾试纸变蓝。
C. 装置③中的离子交换膜允许阳离子、阴离子和小分子水通过。
D. 装置④的待镀铁制品应与电源正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是
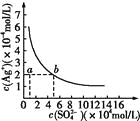
A. 含有大量SO42-的溶液中肯定不存在Ag+
B. 0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
C. Ag2SO4的溶度积常数(Ksp)为1×10-3
D. a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com