
【题目】下列烷烃的沸点是:甲烷-164℃,乙烷-89℃,丁烷-1℃,戊烷+36℃,根据上述数据判断,丙烷的沸点可能是( )
A、低于-89℃ B、约为-42℃ C、高于-1℃ D、高于+36℃
科目:高中化学 来源: 题型:
【题目】为实现下列实验目的,下表提供的主要仪器和所用试剂合理的是( )
选项 | 实验目的 | 主要仪器 | 所用试剂 |
A | 提纯混有MgCl2杂质的AlCl3溶液 | 烧杯、分液漏斗、胶头滴管、铁架台 | 待提纯的AlCl3溶液、NaOH溶液 |
B | 检验NH4Cl固体中的阳离子 | 试管、酒精灯 | NH4Cl固体、红色石蕊试纸、蒸馏水 |
C | 实验室制取CO2 | 试管、带导管的橡胶塞 | 大理石、稀硫酸 |
D | 测定FeSO4溶液的浓度 | 酸式滴定管、锥形瓶、 烧杯 | 0.100 mol·L-1 KMnO4标准溶液、FeSO4溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月18日中共中央国务院公开致电祝贺南海北部神狐海域进行的“可燃冰”试采成功。“可燃冰”是天然气水合物,外形像冰,在常温常压下迅速分解释放出甲烷,被称为未来新能源。
(1)“可燃冰”作为能源的优点是__________(回答一条即可)。
(2)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷,氧气和水蒸气,发生的主要化学反应如下:
反应过程 | 化学方程式 | 焓变△H(kJ.mol-l) | 活化能E.(kJ.mol-1) |
甲烷氧化 | CH4(g)+O2(g) | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸气重整 | CH4(g)+H2O(g) | +206.2 | 240.1 |
CH4(g)+2H2O(g) | +158.6 | 243.9 |
回答下列问题:
①在初始阶段,甲烷蒸汽重整的反应速率______(填“大于”“小于”或“等于”)甲烷氧化的反应速率。
②反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
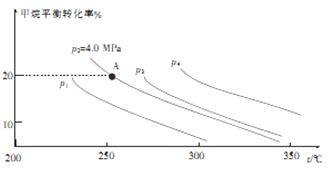
该反应在图中A点的平衡常数Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),图中压强(p1、p2、p3、p4)由大到小的顺序为___________。
③从能量角度分析,甲烷自热重整方法的先进之处在于___________。
④如果进料中氧气量过大,最终会导致H2物质量分数降底,原因是__________。
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和开境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。
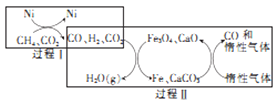
①过程II中第二步反应的化学方程式为_____________。
②只有过程I投料比![]() _______,过程II中催化剂组成才会保持不变。
_______,过程II中催化剂组成才会保持不变。
③该技术总反应的热化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如下:
海藻![]() 海藻灰
海藻灰![]() 海藻灰悬浊液
海藻灰悬浊液![]()

(1)写出提取碘的过程中有关实验操作的名称:①______;③________。
(2)提取碘的过程中可供选择的有机溶剂是(____)
A.汽油、酒精 B.四氯化碳、汽油 C.醋酸、酒精
(3)为完成以上①、③两步操作,实验室里有烧杯、玻璃棒、铁架台、烧瓶、导管、酒精灯,尚缺少的玻璃仪器是____________________________________。
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图所示的实验装置中的错误之处:①______,②________,③________,④________。

(5)为便于控制蒸馏时的温度,操作时使用水浴加热,最后晶体碘在________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+![]() O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为____________;C的燃烧热为____________。
(2)燃烧10 g H2生成液态水,放出的热量为____________。
(3)写出CO燃烧的热化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的离子积:25℃时Kw=1×10﹣14,100℃时Kw=1×10﹣12。试回答以下问题.
(1)25℃时,某Na2SO4溶液中c(SO42﹣)=5×10﹣4 molL﹣1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH﹣)=_________.
(2)在100℃时,测得某溶液pH=7,该溶液显_________(填“酸”、“碱”或“中”)性.
(3)将100℃温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合,若所得混合液pH=2,则a:b=________.
(4)某温度时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=________。
①该温度下( T ℃),将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=____________。
②该温度下(T ℃),1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学与科研、生产、生活相关的说法不正确的是( )
A.84消毒液能消杀新冠病毒,它也具有漂白性
B.常用铝槽车装运浓硫酸及浓硝酸是因为它们和铝不发生化学反应
C.锂离子电池是新一代可充电的绿色电池
D.电力是污染最小的一种二次能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为盐酸介质中,金属铜与氢叠氮酸(HN3)构成的原电池,总反应方程式为: 2Cu+2Cl- +HN3+3H+=2CuCl(s)+N2↑+NH4+。下列叙述错误的是
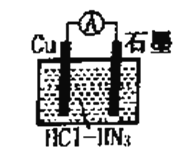
A. 电子的流向为Cu→![]() →石墨
→石墨
B. 负极的电极反应式为Cu+Cl――e-=CuCl(s)
C. 反应一段时间后正极区溶液的pH减小
D. 标准状况下,生成224mL N2时,铜转移的电子数为0.02NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com