
【题目】一定温度下某容积不变的密闭容器中,可逆反应C(s)+H2O(g)![]() CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
CO(g)+H2(g)可建立平衡状态。下列状态中不能确定该反应已达到平衡状态的是( )
A. 体系的压强不再发生变化 B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时生成n mol H2 D. 1 mol H—H键断裂的同时断裂2 mol H-O键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A. 向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中![]() 减小
减小
B. 将CH3COONa溶液从20 ℃升温至30 ℃,溶液中![]() 增大
增大
C. 在pH=8的NaB溶液中:c(Na+)﹣c(B﹣)=9.9×10﹣8mol![]() L﹣1
L﹣1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列操作中,所使用的仪器能够达到目的是( )
A.用5mL量筒准确量取4.55mL水
B.称量4.5g纯碱时,将纯碱放在称量纸上置于托盘天平的右盘,将砝码放在托盘天平的左盘
C.过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
D.萃取操作时,选择萃取剂的密度可以比水大也可以比水小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( ) ①1mol O2的质量是32gmol﹣1;②H2的摩尔质量是2g;③1mol H+的质量是1g;④对原子而言,摩尔质量就是相对原子质量.
A.①②③
B.③④
C.③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验、现象及有关结论不正确的是
选项 | A | B | C | D |
实验 |
|
|
|
|
现象 | 加热铝箔,铝箔熔化却不滴落 | 石蜡油分解产生的气体能使试管中溴的四氯化碳溶液褪色 | 食盐水浸泡过的铁钉放入试管中,一段时间后,导管口形成一段水柱 | 向蔗糖中加人浓硫酸时,蔗糖变黑,体积膨胀 |
结论 | 氧化铝的熔点比铝的高 | 石蜡油的分解产物中含不饱和烃 | 铁钉发生吸氧腐蚀 | 浓硫酸具有吸水性和强氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+![]() O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为____________;C的燃烧热为____________。
(2)燃烧10 g H2生成液态水,放出的热量为____________。
(3)写出CO燃烧的热化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用480mL、0.5mol/L的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)实验需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有________________________;
(2)计算:98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为__________,配制本次实验需要的稀硫酸需用量筒量取上述98%的浓H2SO4___________________ mL
(3)配制过程:①用量筒量取所需的浓硫酸
②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦将配制好的溶液转移至试剂瓶中待用。
上述配置溶液的步骤存在缺失,缺少的步骤是_____________________,应放在步骤_____之前进行(填“序号”)。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”).
①所用的浓硫酸长时间放置在密封不好的容器中_________;
②量取浓硫酸所用量筒有蒸馏水_________;
③定容时,俯视液面_________;
④用量筒量取浓硫酸时仰视液面___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是一种二元弱酸,可用作还原剂、络合剂、掩蔽剂、沉淀剂。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。
回答下列问题:
(1)甲组的同学利用电石(主要成分CaC2,少量CaS及Ca3P2等)并用下图装置制取C2H2[反应原理为:CaC2+2H2O![]() Ca(OH)2+C2H2(g) △H<0,反应剧烈]:
Ca(OH)2+C2H2(g) △H<0,反应剧烈]:
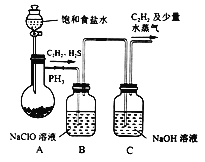
① 装置A用饱和食盐水代替水并缓慢滴入烧瓶中,其目的是__________。
② 装置B中,NaClO将H2S、PH3氧化为硫酸及磷酸,本身还原为NaCl,其中H2S被氧化的离子方程式为________。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化乙炔制取H2C2O4·2H2O。制备装置如下:
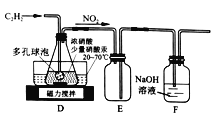
①装置D多孔球泡的作用是_________;装置E的作用是________。
②D中生成H2C2O4的化学方程式为_______。
③从装置D得到产品,还需经过浓缩结晶、________(填操作名称)洗涤及干燥。
(3)丙组设计了测定乙组产品在H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:精确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,在加入少量稀硫酸,然后用cmol/L酸性KMnO4标准溶液进入滴定,滴至溶液显微红色;共消耗标准溶液VmL。
①滴定时,KMnO4标准溶液盛放在__________滴定管中(填“酸式”或“碱式”)。
②滴定时KMnO4被还原Mn2+,其反应的离子方程式为_____,滴定过程中发现褪色速率先慢后逐渐加快,其主要原因是__________。
③产品中H2C2O4·2H2O的质量分数为_________(列出含m、c、v的表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com