
【题目】下列图示与对应的叙述相符的是

A. 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B. 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,且CH3COOH溶液的pH:a>b
C. 图丙表示加入催化剂,化学反应的焓变减小
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) ![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的H<0
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列各关系式中能说明反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
A. 3v正(N2)=v正(H2) B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3) D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.Na在足量O2中燃烧,消耗lmol O2时转移的电子数是4×6.02×1023
B.盐酸和醋酸的混合溶液pH=1,该溶液中c(H+) =0.1 mol/L
C.1 L 0.1 mol/L NH4Cl溶液中的NH![]() 数是0.1×6.02×1023
数是0.1×6.02×1023
D.标准状况下2.24 L Cl2中含有0.2 mol 共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z的离子具有相同的核外电子排布,离子半径Y大于Z,Y与Z可形成常见的离子化合物,原子半径X大于Z,则下列说法中不正确的是![]()
A.原子序数一定是![]()
B.X、Z两种元素的单质的沸点一定是![]()
C.Z的最高价氧化物一定能溶于X、Y的最高价氧化物的水化物
D.工业上获得X、Z单质的方法主要是电解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,下列叙述正确的是![]()
A.![]() 的
的![]() 与
与![]() 混合溶液中
混合溶液中![]()
B.![]() 的可乐中
的可乐中![]() 是
是![]() 的柠檬水中
的柠檬水中![]() 的10倍
的10倍
C.AgCl在![]()
![]() 溶液和
溶液和![]() NaCl溶液中的溶解度相同
NaCl溶液中的溶解度相同
D.![]() 溶液加水稀释至100mL,pH和
溶液加水稀释至100mL,pH和![]() 均减小
均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某密闭容器中存在如下反应A(g)+xB(g) ![]() 2C(g),反应过程中有关量值变化如下图所示,下列说法中错误的是( )
2C(g),反应过程中有关量值变化如下图所示,下列说法中错误的是( )
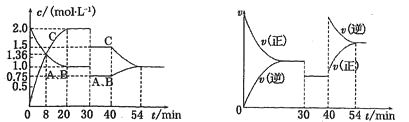
A.30 min时扩大了容器的容积
B.首次平衡时的K=4
C.40 min时增大了压强
D.8 min前A的平均反应速率为0.8 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯是一种难溶于水,密度大于水的无色油状液体,具有茉莉花气味,可用做调香剂。
(一)以乙烯,甲苯为原料,合成乙苯甲酯的路线如图所示。

(1)写出由乙烯制备A的化学方程式______。
(2)写出生成乙酸苯甲酯的化学方程式______。
(3)C到苯甲醇的反应类型______。
(二)制备乙酸苯甲酯的流程如图:
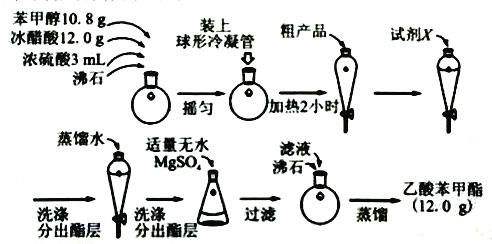
(4)球形冷凝管的作用为______。
(5)试剂X可为______。
A.氢氧化钠溶液 B.碳酸钠溶液 C.乙醇 D.氯化钠溶液
(6)分出酯层时应收集______层液体(填“上”或“下”)
(7)无水MgSO4的作用为______。
(8)本实验所得乙酸苯甲酯的产率为______。(已知:相对分子量:苯甲醇:108;乙酸:60;乙酸苯甲酯:150)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业上以制作印刷电路的废液![]() 含
含![]() 、
、![]() 、
、![]() 、
、![]() 生产CuCl的流程:
生产CuCl的流程:
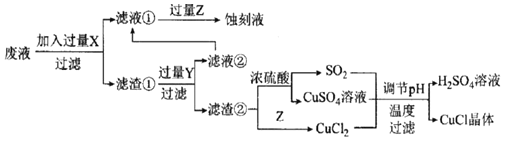
已知:CuCl是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化为绿色,见光分解变成褐色。
请回答下列问题:
(1)流程中的滤渣①与Y反应和X与Y反应相比,单位时间内得到的气体多,其原因为______。
(2)滤液②需要加过量Z,检验Z过量的方法是______。
(3)写出生成CuCl的离子方程式:______。
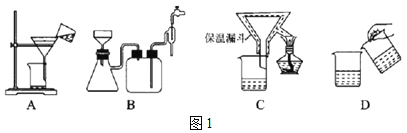
(4)为了提高CuCl产品的纯度,流程中的“过滤”操作适宜用下列装置![]() 图
图![]() 中的______
中的______![]() 填选项字母
填选项字母![]() ,过滤后,洗涤CuCl的试剂宜选用______
,过滤后,洗涤CuCl的试剂宜选用______![]() 填“无水乙醇”或“稀硫酸”
填“无水乙醇”或“稀硫酸”![]()
![]() 加入饱和NaCl溶液中会部分溶解生成
加入饱和NaCl溶液中会部分溶解生成![]() ,在一定温度下建立两个平衡:
,在一定温度下建立两个平衡:
I.CuCl![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。
(5)分析![]() 、
、![]() 和
和![]() 、K的数学关系,在图2中画出
、K的数学关系,在图2中画出![]() 、
、![]() 的关系曲线________(要求至少标出一个坐标点)
的关系曲线________(要求至少标出一个坐标点)
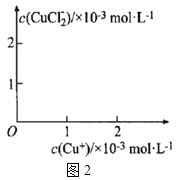
(6)氯化亚铜的定量分析:
①称取样品![]() 于250mL锥形瓶中,加入10mL过量的
于250mL锥形瓶中,加入10mL过量的![]() 溶液,不断摇动:
溶液,不断摇动:
②待样品溶解后,加入20mL蒸馏水和2滴指示剂;
③立即用![]() 硫酸铈标准溶液滴定至绿色为终点;
硫酸铈标准溶液滴定至绿色为终点;
④重复三次,消耗硫酸铈溶液的平均体积为![]() 。
。
上述相应化学反应为![]() 、
、![]() ,则样品中CuCl的纯度为______
,则样品中CuCl的纯度为______![]() 保留三位有效数字
保留三位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.氢氧燃料电池的能量转换形式仅为化学能转化为电能
B.一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率
C.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+
D.在一密闭容器中发生2SO2+O2![]() 2SO3反应,增大压强,平衡会正向移动,
2SO3反应,增大压强,平衡会正向移动,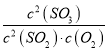 的值增大
的值增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com