
【题目】利用生活中或实验室中的常用物品,根据氧化还原反应知识和电化学知识,自己动手设计一个原电池.请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑
(2)实验用品:电极(__、__)、稀硫酸、__、__耳机(或电流计).
(3)①按如图所示装置连接好实验仪器,这时可以听见耳机发出“嚓嚓……”的声音。其原因是在原电池中化学能转化为__,在耳机中__又转化为声波这种能量。
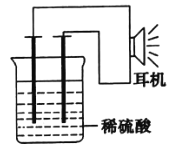
②在该原电池内中,Fe在___极发生了___反应,H+在___极发生了___反应。
【答案】铁钉(或铁条等) 铜钉(或其他的惰性电极,如铅笔芯等) 烧杯 导线 电能 电能 负 氧化 正 还原
【解析】
根据Fe+2H+═Fe2++H2↑知,铁失电子被氧化,则Fe作原电池负极,不如铁活泼的金属或导电的非金属作原电池正极,电解质溶液为弱氧化性酸溶液,结合原电池构成条件及能量转化方式分析解答。
(2)由形成原电池的条件可知,需要铁为负极,正极为铜钉(其他的惰性电极如铅笔 芯、铂等都可以),硫酸为电解质溶液,还需要烧杯、导线等,故答案为:铁钉或铁条;铜钉(其他的惰性电极如铅笔芯、铂等都可以);烧杯、导线;
(4)①在原电池中,由化学能转化为电能,在耳机中又由电能转化为声音这种能量,故答案为:电能;电能;
②如果将装置中的耳机改为电流计,则电流表指针发生偏转,形成原电池反应,铁为负极,发生氧化反应,电极方程式为Fe-2e-=Fe2+,正极发生还原反应,电极方程式为2H++2e-=H2↑,铁钉应该连接电流计的负极,铜钉连接电流计的正极,故答案为:负;氧化;正;还原。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】某温度下,0.200 molL-1的HA溶液与0.200 molL-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是
微粒 | X | Y | Na+ | A- |
浓度/(mol·L-1) | 8.00 | 2.50 | 0.100 | 9.92 |
A. 0.1mol·L-1HA溶液的pH=1 B. 该温度下Kw=1.0![]() 10-14
10-14
C. 微粒X表示OH-,Y表示H+ D. 混合溶液中:n(A-)+n(X)=n(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验兴趣小组按下图装置实验后,所记录内容合理的是( )
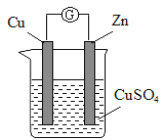
实验 记录 | ① Cu为正极,Zn为负极; ② Zn质量减少,Cu质量增加; ③ SO ④ 电子流方向是:由Zn经导线流入Cu片; ⑤ Zn电极发生还原反应; ⑥ 正极反应式:Cu2+ + 2e- = Cu |
A.②③④ B.①②④⑥ C.①②④⑤ D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 的一元酸HA,溶液的pH的变化曲线如图所示, 不正确的是
的一元酸HA,溶液的pH的变化曲线如图所示, 不正确的是
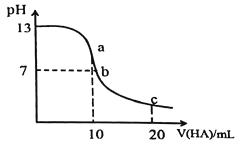
A.a点时,溶液中存在![]()
B.b点时,![]()
C.c点时,溶液中存在![]()
D.水的电离程度:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
(1)某有机物的结构简式如图。该有机物分子是___(填“极性”或“非极性”)分子,该有机物分子中电负性最大的原子为___。
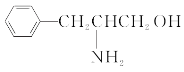
(2)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 25℃下时,NH3·H2O kb=1.77×10-5;H2CO3 ka1=4.30×10-7、ka2=5.61×10-11。 25℃时有关NH4HCO3溶液的说法中正确的是
A. 呈弱酸性
B. c(OH-)+c(NH3·H2O)=c(H+)+c(H2CO3)
C. 滴入NaOH 溶液发生反应:NH4++OH-=NH3·H2O和HCO3-+OH-=H2O+CO32-
D. 滴入NaOH溶液,则![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸钠(NaH2PO2)常用作化学镀剂、食品及工业锅炉水添加剂、抗氧剂。实验室可用如图所示装置制取一定量的次磷酸钠。已知PH3是一种无色、有毒且能自燃的气体。

回答下列问题:
(1)装烧碱溶液的仪器名称是___,已知NaH2PO2与盐酸反应但不能与NaOH溶液反应,则次磷酸(H3PO2)是___元弱酸。
(2)实验开始时,首先要打开K1,通入一段时间N2,其目的是___,为尽可能避免PH3造成的空气污染,拆卸装置前还要进行的一项操作是___,a中反应的化学方程式为___。
(3)装置C中物质反应后生成了NaCl、NaH2PO2,通过___的方法可分离出NaH2PO2固体(已知NaH2PO2在25℃时溶解度为100g,100℃时溶解度为667g)。
(4)产品纯度测定:取产品mg,将其溶于水配成250mL溶液,再用___(填“酸式”或“碱式”)滴定管取25.00mL溶液于锥形瓶中,然后用0.01mol·L-1的KMnO4标准溶液滴定(氧化产物是PO43-),达到滴定终点时消耗V1mLKMnO4标准溶液,滴定终点的现象是___,产品纯度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用。
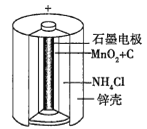
(1)锌锰干电池是应用最普遍的电池之一,如图为锌锰干电池的构造示意图,锌锰干电池的负极材料是________(填物质名称),负极发生的电极反应为_____________。若反应消耗32.5 g负极材料,则电池中转移电子的数目为________。
(2)目前常用的镍镉(Ni-Cd)可充电电池的总反应式可表示为Cd+2NiO(OH)![]() 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
①该电池可以在酸性条件下进行充、放电
②该电池放电时,负极的电极反应式为Cd-2e-+2OH-=Cd(OH)2
③该电池放电时,Cd极的质量减少
④该电池放电时,化学能转变为电能
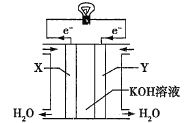
(3)如图为氢氧燃料电池的构造示意图,电解质溶液是KOH溶液。则X极为电池的________(填“正”或“负”)极,X极的电极反应式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com