
| A、1种 | B、2种 | C、3种 | D、4种 |


科目:高中化学 来源: 题型:
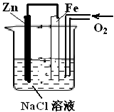
| A、锌极附近滴入酚酞,溶液呈红色 |
| B、铁极发生的电极反应为:2H2O+O2+4e═4OH- |
| C、铁极发生吸氧腐蚀生成锈蚀 |
| D、溶液中的OH-离子向铁极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B、V=224 |
| C、样品中CuO的质量为2.0g |
| D、样品中Fe元素的质量为1.07g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 | B、3 | C、5 | D、多于5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaBr,NaI |
| B、NaCl,NaBr |
| C、NaCl |
| D、NaCl,I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:HF<HCl<HBr |
| B、微粒半径:O2->Mg2+>Cl- |
| C、第一电离能:Si>Al>Mg |
| D、电负性:Si>Al>Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
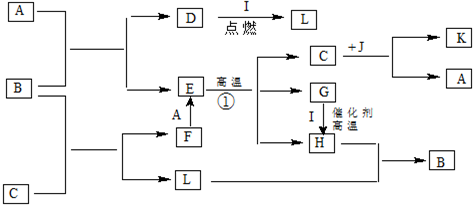
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com