
【题目】下列对有机物的描述正确的是
A. 组成为C6H14的烷烃中仅能由1种单炔烃加氢而制得的结构有2种
B. 立方烷( ![]() )燃烧的现象与乙烷燃烧的现象相同
)燃烧的现象与乙烷燃烧的现象相同
C. ![]() 分子中所有原子不可能处于同一平面
分子中所有原子不可能处于同一平面
D. 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,HX溶液、HY溶液、HY和NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是

A. HX、HY均为一元强酸
B. 溶液中水的电离程度:a = b < c
C. 常温下,HY的电离常数Ka约为1.0×10-4
D. c点溶液:c(Na+)>c(Y-)>c(HY) >c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣[主要成分为 Ca(OH)2 和 CaCO3]为原料制备 KClO3 的流程如下:

下列说法正确的是
A. 打浆步骤,将电石渣配制成溶液
B. 氯化步骤,发生的主要反应 2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
C. 转化步骤,发生复分解反应,将所得溶液蒸发结晶过滤得 KClO3 晶体
D. KClO3 晶体中可能混有 KCl、KClO 等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(一) 现代铝的精炼研究方向是减低能耗。如图 :室温下通过电解在阴极沉积纯铝,A1Br3 在苯(简写 ArH)中可以生成[A12Br5ArH]+和 Br-。

(1)阳极的材料________;
(2)写出阴极沉积铝的电极方程式__________________________________________;
(二)邻硝基苯甲酸是重要的医院中间体,最新合成方法是邻硝基甲苯和高锰酸钾在相转移催化剂季铵盐(Q+X-)氧化、酸化合成,其原理如下:

相转移催化原理如下:

有关物质的物理性质如下表:
物质 | 邻硝基苯甲酸 | 高锰酸钾 | 苄基三乙基氯化铵(C6H5-CH2CH2)N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵(C4H9)4NBr | NH4Cl |
水 | 难溶 | 易溶 | 可溶 | 任意比互溶溶 | 可溶 | 易溶 |
有机物 | 易溶 | 难溶 | 易溶 | 易溶 | 易溶 | 难溶 |
下列说法不合理的是________;
A.相转移催化剂作用主要决定于 Q+的物理化学性质
B.反应中为了防止温度剧烈升高,投料应该分批加入
C.Q+X-是通过增大反应接触面积提高反应速率
D.增大压强可以提高邻硝基甲苯氧化的反应限度
E.工业使用季铵盐(Q+X-)可以提高邻硝基苯甲酸产率
(2)四丁基溴化铵(C4H9)4NBr 萃取水中的高锰酸钾的方程式为:KMnO4(aq) +Q+X-(aq) →Q+ MnO4- (aq) +KX(aq),写出平衡常数 k 的表达式________________;设n(Q+X-):n(邻硝基甲苯)=x,理论证明当 x=5%邻硝基甲酸产率 y 得到最大值,请画出 y 随 x 变化的示意图________________ 。
(3)实验表明,当温度 100℃、反应时间 2.5h,n(KMnO4): n(邻硝基甲苯)=3:1,催化剂用量相同,Q+X-反应的催化效果如下:
相转移催化剂 | 苄基三乙基氯化铵 (C6H5-CH2CH2) N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵 (C4H9)4NBr |
产率% | 46.7 | 20.0 | 53.1 |
苄基三乙基氯化铵比四丁基溴化铵催化效果差的原因_____________________________;工业生产不用聚乙二醇做催化剂的主要原因____________________________________ ;
(4)(C4H9)4NBr 为催化剂,邻硝基甲苯和高锰酸钾反应,测得溶液酸碱性对产率、反应时间影响如图 ,下列推测合理的是________。

A.溶液碱性强产率降低是因为季铵盐发生水解反应
B.pH=2 高锰酸钾一定发生副反应
C.选择 pH=7、适当升温可以提高产率
D.工业可以选择浓硝酸替代高锰酸钾做氧化剂,减缓对设备的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核磁共振谱表明普鲁卡因 J(C13H20N2O2)中苯环上只有两类氢,它的合成路线如下:

请回答下列问题:
(1)物质 C 的名称是________________;F→G 反应类型是___________________;
(2)铁粉需要活化的理由是______________________________________________;
(3)已知普鲁卡因的阳离子(代号:BH+)的电离常数 Ka= 1×10-9。请计算在 pH=7 时,盐酸普普卡因溶液里的 B 和 BH+的浓度比________;
(4)写出 D→E 的化学方程式________________________________________________;
(5)K 是比 D 多一个碳原子的同系物,写出符合下列条件的 K 的所有同分异构体的结构简式___________;
①属于芳香族化合物
②能与碳酸氢钠溶液反应
③H-NMR 谱显示有 5 种氢原子
(6)参照上述合成路线和信息,用物质 C、二甲苯、HOCH2CH2N(C2H5)2 为原料(其他无机试剂任选)合成盐酸普鲁卡因。(已知:二甲苯和水易形成共沸混合物)_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯的物质与人们的生活密切相关。已知氯元素常见的化合价有-1、0、+1、+3、+5、+7六种,其不同价态的物质间可相互转化。回答下列问题:
(1)氯原子的原子结构示意图___;氯离子的电子式___。
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是____(写名称),漂粉精的主要有效成分是___(写化学式)。
(3)实验室制取氯化氢的化学方程式____。
(4)工业上将含有氯气的尾气通过___进行处理,在处理时发生的反应中氯气作为____。
a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。已知:HNO2既有氧化性又有还原性;AgNO2微溶于水,能溶于硝酸:AgNO2+HNO3= AgNO3+ HNO2。
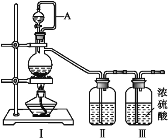
(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl2
① 写出利用装置Ⅰ制备氯气的离子反应方程式:_________。
② 利用上述装置制备NO时,Ⅱ中盛装物质为_________(写化学式)。
(2)利用以下装置在常温常压下制备ClNO
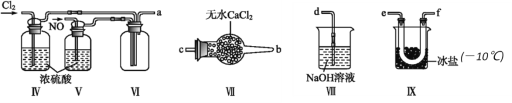
① 装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
② 为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为_________。
③ 装置Ⅸ的作用是_____________。
④ 装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾气,可将尾气与______________(气体)同时通入NaOH溶液中。
⑤ 王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2,该反应的化学方程式为______________________________________。
⑥ 写出验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2的实验步骤:取少量反应后的溶液于试管中,______________________________________________________。(限选试剂如下:AgNO3溶液,稀硝酸,KMnO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积均为100mL浓度均为1molL的 NaClO、NaOH、CH3COONa的三种溶液中通入CO2,测得各溶液中n(HCO3-)的变化如下:

下列分析正确的是
A. CO2通入 NaClO溶液的反应:2ClO-+CO2+H2O=CO32-+2HClO
B. CO2通入 CH3COONa溶液的反应:CO2+H2O+ CH3COO-=HCO3-+ CH3COOH
C. 通入n(CO2)=0.06mol,NaOH溶液的反应:2OH-+CO2=CO32-+H2O
D. 通入n(CO2)=0.06mol,三种溶液中:n(HCO3-)+n(CO32-)+n(H2CO3)=0.06mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O==2Cu+2Li++2OH-,下列说法不正确的是

A. 放电时,正极的电极反应式为Cu2O+H2O+2e-=2OH-+2Cu
B. 放电时,电子透过固体电解质向Li极移动
C. 通空气时,铜电极被腐蚀,表面产生Cu2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com