


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、4 v(NH3)=5v(O2) |
| B、6 v(O2)=5v(H2O) |
| C、4v(NH3)=6 v(H2O) |
| D、v(O2)=4v(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
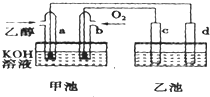 如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题
如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有盐类物质生成 |
| B、有酯类物质生成 |
| C、有醇类物质生成 |
| D、有酸类物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.
第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com