

| Fe3+ | Cu2+ | Cr3+ | |
| ��ʼ����pH | 2.1 | 4.7 | 4.3 |
| ��ȫ����pH | 3.2 | 6.7 | a |
���� �������м���ϡ���ᣬ������ӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O��CuO+H2SO4=CuSO4+H2O��Cr2O3+3H2SO4=Cr2��SO4��3+3H2O��Ȼ����˵õ�����I����Һ����Һ������ΪFe2��SO4��3��Cr2��SO4��3��CuSO4������Һ�м���Ca��OH��2����������ҺpH����������ͼ����Һ�к���Cr3+��Cu2+������ Fe3+��˵������II�к���Fe��OH��3�����������������Գ���II�ɷ�ΪFe��OH��3��CaSO4��ҪʹCr3+��Cu2+��������Fe3+���������������������ɳ�����ҪpHֵ֪����Һ��pH��ΧΪ3.2-4.3֮�䣻����Һ�м���NaHSO3�����������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��HSO3-+H+=SO2��+H2O�����˵õ�Cu2O������Һ�м���NaOH��������ҺpH��������ӦCr3++3OH-=Cr��OH��3������ҺX�к���NaOH��Na2SO4���ݴ˷������
��� �⣺�������м���ϡ���ᣬ������ӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O��CuO+H2SO4=CuSO4+H2O��Cr2O3+3H2SO4=Cr2��SO4��3+3H2O��Ȼ����˵õ�����I����Һ����Һ������ΪFe2��SO4��3��Cr2��SO4��3��CuSO4������Һ�м���Ca��OH��2����������ҺpH����������ͼ����Һ�к���Cr3+��Cu2+������ Fe3+��˵������II�к���Fe��OH��3�����������������Գ���II�ɷ�ΪFe��OH��3��CaSO4��ҪʹCr3+��Cu2+��������Fe3+���������������������ɳ�����ҪpHֵ֪����Һ��pH��ΧΪ3.2-4.3֮�䣻����Һ�м���NaHSO3�����������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��HSO3-+H+=SO2��+H2O�����˵õ�Cu2O������Һ�м���NaOH��������ҺpH��������ӦCr3++3OH-=Cr��OH��3������ҺX�к���NaOH��Na2SO4��
��1���ٸ���ͼ����֪��������ȫ����pHΪ3.2��Cr3+��ʼ������pHΪ4.3�������ڳ��������У���Ҫ��ȥFe3+��CaSO4���ֲ���ʹ��Cr3+��������ز������ټ���ʯ�������pH��3.2��4.3֮�䣬����Fe3+�������軯����Һ����Һ�Ƿ��죬�ʴ�Ϊ��3.2�� ȡ������Һ����KSCN��Һ��������죬��˵��Fe3+�ѳ������ڽ���Һ���ȵ�80�棬��ͼ2��֪��80��ʱCaSO4���ܽ��Խ�С������Ҫ���ȹ��˿��Գ�ȥCaSO4���ʴ�Ϊ�����ȹ��ˣ�
��2������������Ӿ���ǿ�Ļ�ԭ�ԣ��ܺ�ͭ����֮�䷢����Ӧ��������������Լ�������ͭ�������ķ�ӦΪ��2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+���ʴ�Ϊ��2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��
��3��������Ũ�ȡ�1��10-5 mol•L-1��Ϊ������ȫ����ҪʹCr3+��ȫ������Ҫ����c��OH-����$\root{3}{\frac{Ksp}{c��C{r}^{3+}��}}$=$\root{3}{\frac{6.31��1{0}^{-31}}{1��1{0}^{-5}}}$=4.0��10-9 mol•L-1���ʴ�Ϊ��4.0��10-9 mol•L-1��
���� ���⿼�����ʵķ�����ᴿ�ۺ�Ӧ�ã�Ϊ�߿���Ƶ�㣬�漰��������ܽ�ƽ�⡢����ʵ�������֪ʶ�㣬���ؿ�����������㼰ʵ�������������Ϥ����ͼ���漰�ķ�Ӧ�������������ѵ����ܶȻ��������㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵķ���Ƕ������������䷽�еġ�������Ρ���Ϊ�� | |
| B�� | ���ù��̷����ķ�ӦΪ������ԭ��Ӧ | |
| C�� | ���ù��̷����ķ�Ӧ�У���Ӧ����������Ϊ����� | |
| D�� | ��Ӧ�����ӷ���ʽΪ2Al3++3CO32-�T2Al��OH��3��+3CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
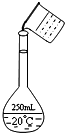 ʵ�����ù���NaOH����0.5mol/L��NaOH��Һ500mL����������������Ʒ�У����ձ� ��100mL��Ͳ ������ƿ ��ҩ�� �ݲ����� ��������ƽ�������룩
ʵ�����ù���NaOH����0.5mol/L��NaOH��Һ500mL����������������Ʒ�У����ձ� ��100mL��Ͳ ������ƿ ��ҩ�� �ݲ����� ��������ƽ�������룩�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij���ʲ�������ʣ������ڷǵ���� | |
| B�� | SO3����ˮ�ɵ��磬SO3���ڵ���� | |
| C�� | �ܵ�����������ڵ���ʣ�NaCl���ڵ���ʣ�NaCl����ɵ��� | |
| D�� | ��֪������������״̬���ܵ��磬��������������״̬���ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
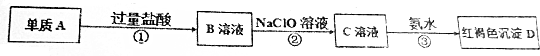
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
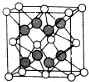 �±���������Ԫ�ص������Ϣ������������Ϣ��գ�
�±���������Ԫ�ص������Ϣ������������Ϣ��գ�| Ԫ�� | �����Ϣ |
| T | ��̬ԭ��2p�ܼ���3�������� |
| W | ��̬ԭ��p����ϳɶԵ���������δ�ɶԵ����� |
| X | �⻯�ﳣ���ڿ�ʴ���� |
| Y | ��̬ԭ�Ӻ�����ӷִ�6����ͬ�ܼ�����ÿ���ܼ��������� |
| Z | ԭ����������X��Y��ԭ������֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com