
����Ŀ����ͼ������ˮ������Ӧ��ʵ��װ�á���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ����(ʯ���������²��ϣ���ˮ��������Ӧ)�Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ���������ˮ������Ӧ��ʵ�顣
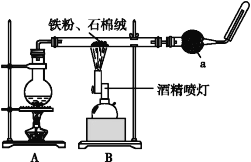
��1����ʵ�鷴Ӧ�ķ�Ӧ����ʽΪ��___��
��2������a��������___��
��3��ijͬѧΪ���о�һ��ʱ�������۵�ת���ʣ����������ʵ�飺ȷ����һ�����������۽��з�Ӧ��������Ӧ�����������������������۵�ת���ʡ�
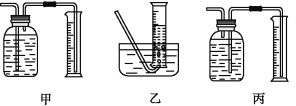
�ٸ�ͬѧӦ���ȵ�ȼ__(�A����B��)���ľƾ���(��ƾ����)�������������������ѡ����ͼ��___(��ס����ҡ�����)װ�á�
�ڳ�ȡ5.6g����������ʯ����ϣ�Ȼ����ȷ�Ӧһ��ʱ�䡣���������������ڱ�״����Ϊ0.896L�������۵�ת����Ϊ__����ת����=![]() ��
��
��4����Ӳ�ʲ������з�Ӧ��Ĺ�������ȫ��ȡ�������ձ��У����������������ܽⲢ���ˣ�Ϊ̽����Ӧ����Һ�п��ܵ������ӣ�С��ͬѧ��������ʵ�飬���㽫�±�����������
���� | ���� | ����(�����ӷ���ʽ��ʾ) | ���� |
��.ȡ�����μ�KSCN��Һ | ��Һ�����ɫ��Fe3+��KSCN��Һ��Ӧ�Ժ�ɫ�� | ��Fe3O4+8H+=Fe2++2Fe3++4H2O ��____ | ��.��Ӧ�����Һ��������Ϊ___ |
��.ȡ�����μ�NaOH��Һ | �տ�ʼ����������һ��ʱ����ȳ��ְ�ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ | ��___ ��Fe2++2OH��=Fe(OH)2������ɫ�� 4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
���𰸡�3Fe+4H2O��g��![]() Fe3O4+4H2 ����� A �� 30% Fe+2Fe3+=3Fe2+ OH��+H+=H2O H����Fe2��
Fe3O4+4H2 ����� A �� 30% Fe+2Fe3+=3Fe2+ OH��+H+=H2O H����Fe2��
��������
��A�ṩˮ��������B�з�Ӧ����ʵ�鷴Ӧ�ķ�Ӧ����ʽΪ3Fe+4H2O��g��![]() Fe3O4+4H2��
Fe3O4+4H2��
������a�������Ǹ���ܡ�
�����Ƚ�A���ƾ��Ƶ�ȼ����ˮ������������װ�ã��ٵ�ȼB���ƾ��ƣ�����ˮ���ⶨ���������
����ȡ5.6g���ۼ��������ʵ���Ϊ0.1mol�����������������ڱ�״����Ϊ0.896L�����ʵ���Ϊ0.04mol������3Fe+4H2O��g��![]() Fe3O4+4H2�����������ʵ���Ϊ0.03mol���ټ������۵�ת����Ϊ��
Fe3O4+4H2�����������ʵ���Ϊ0.03mol���ټ������۵�ת����Ϊ��
����Һ�����ɫ��Fe3+��KSCN��Һ��Ӧ�Ժ�ɫ����˵����Һ�е�������������Ӧ�������������ӣ�Fe+2Fe3+=3Fe2+�������������ƣ��տ�ʼ����������˵��������кͷ�Ӧ�����ӷ�ӦΪOH��+H+ = H2O���Ӷ�˵����Ӧ�����Һ�������ӡ�
��A�ṩˮ��������B�з�Ӧ����ʵ�鷴Ӧ�ķ�Ӧ����ʽΪ3Fe+4H2O��g��![]() Fe3O4+4H2���ʴ�Ϊ��3Fe+4H2O��g��
Fe3O4+4H2���ʴ�Ϊ��3Fe+4H2O��g��![]() Fe3O4+4H2��
Fe3O4+4H2��
������a�������Ǹ���ܣ��ʴ�Ϊ������ܡ�
�����Ƚ�A���ƾ��Ƶ�ȼ����ˮ������������װ�ã��ٵ�ȼB���ƾ��ƣ�����ˮ���ⶨ�����������˲�����ѡ����ͼ�м�װ�ã��ʴ�Ϊ��A���ס�
����ȡ5.6g���ۼ��������ʵ���Ϊ0.1mol�����������������ڱ�״����Ϊ0.896L�����ʵ���Ϊ0.04mol������3Fe+4H2O��g��![]() Fe3O4+4H2�����������ʵ���Ϊ0.03mol�������۵�ת����Ϊ
Fe3O4+4H2�����������ʵ���Ϊ0.03mol�������۵�ת����Ϊ![]() ���ʴ�Ϊ��30%��
���ʴ�Ϊ��30%��
����Һ�����ɫ��Fe3+��KSCN��Һ��Ӧ�Ժ�ɫ����˵����Һ�е�������������Ӧ�������������ӣ�Fe+2Fe3+=3Fe2+�������������ƣ��տ�ʼ����������˵��������кͷ�Ӧ�����ӷ�ӦΪOH��+H+ = H2O���Ӷ�˵����Ӧ�����Һ��������ΪH����Fe2�����ʴ�Ϊ��Fe+2Fe3+=3Fe2+��OH��+H+ = H2O��H����Fe2����


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ��ʵ������ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�ã�
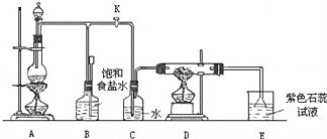
��1��A����������װ�ã����з�Ӧ�Ļ�ѧ����ʽΪ_____��
��2��ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ƾ��ƣ�������Eװ�á�Cl2ͨ��Cƿ���ٽ���D��Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl����д��D�з�Ӧ�Ļ�ѧ����ʽ��_____��װ��C��������_____��
��3����E������ɫʯ����Һ����ɫ����ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ����ԭ����_____��
��4������E���ձ�����Һ��Ϊ����ʯ��ˮ����Ӧ��������Ϊ_____��ѡ���ţ���
A.�а�ɫ�������� B.������ C.�����ɰ�ɫ�����������ɫ������ʧ
��5��D����Ӧ��Ϻر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A������Cl2��������ʱB�е�������_____��B��������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը�����������Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2������FeS2�ͽ��������Σ�Ϊԭ�ϣ����������������Fe3O4�IJ��ֹ����������£�
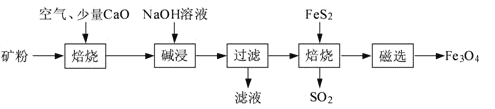
��1���������������ʯ��Ŀ����______��
��2������ʱ����������ԭ��Ӧ��______FeS2+______O2![]() ______Fe2O3+______SO2������ƽ�÷���ʽ��
______Fe2O3+______SO2������ƽ�÷���ʽ��
��3�����ʱ������Ӧ�Ļ�ѧ����ʽΪ______��
��4�����˺�����Һ��ͨ�������CO2���壬��Ӧ�����ӷ���ʽΪ______��
��5�������ˡ��õ��������к��д�����Fe2O3��Fe2O3��FeS2��Ϻ���ȱ�������±�������Fe3O4��SO2����������ȫ��Ӧ���ĵ�n��FeS2����n��Fe2O3��=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������Fe��FeO��Fe3O4�Ļ�����м���100mL2mol/L�����ᣬǡ��ʹ�������ȫ�ܽ⣬�ų�224mL����״���������壬������Һ�м���KSCN��Һ��Ѫ��ɫ���֡�����������CO�ڸ����»�ԭ��ͬ�����Ĵ˻����ܵõ����������ǣ� ��
A. 11.2gB. 5.6gC. 2.8gD. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���������ʵ��װ��(ͼ�мг�װ��ʡ��)�ⶨ�Ʊ���CaCO3��ĩ�Ĵ���(��Ʒ�����ʲ����ᷴӦ����Ӧǰװ���е�CO2��ȫ���ų�)������˵��������ǣ� ��
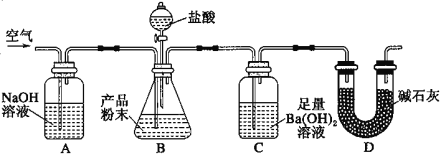
A.����ͨ������������ǽ���Ӧ������װ���в�����CO2ȫ�����뵽Cװ���б�����
B.Aװ�ú�Dװ�ö���Ϊ�˷�ֹ�����е�CO2�������C װ�ö��������
C.��CaCO3��Ʒ������Ϊx����C ��ȡ���ij���ϴ������������Ϊy����CaCO3�Ĵ���Ϊ![]()
D.Ϊ�˷�ֹB ������ӷ��������ţ�������B��Cװ���м��һ��װ�б���̼��������Һ��ϴ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų�������������(NOx)��CO2��SO2�����壬������Ⱦ�������Է���������������̼����������ʵ����ɫ�������������á�
I.��������֪��H2����ֵΪ142.9 kJ/g(��ֵ�DZ�ʾ��λ����ȼ����ȫȼ��ʱ���ų�������)��
N2(g) + 2O2(g)==2NO2(g) ��H= +133 kJ/mol
H2O(g)==H2O(l) ��H=- 44 kJ/mol
���������£�H2��ԭNO2����ˮ���������������ʵ��Ȼ�ѧ����ʽ__________________��
��.��̼����2L�ܱ������м���2 mol CO2��6 mol H2�����ʵ��Ĵ��������£�������ӦCO2(g)+3H2(g) ![]() CH3OH(l) + H2O(l)��
CH3OH(l) + H2O(l)��
(1)�ٸ÷�Ӧ�Է����е�������_________________(���������������������������¶�������������������˵���˷�Ӧ�ﵽƽ��״̬����________________________��
a.��������ƽ��ʽ�����ֲ���
b.CO2��H2������������ֲ���
c.CO2��H2��ת�������
d.���������ܶȱ��ֲ���
e.1 mol CO2���ɵ�ͬʱ��3 mol H-H������
(2)�ı��¶ȣ�ʹ��ӦCO2(g)+3H2(g) ![]() CH3OH(g) + H2O(g) ��H<0�е��������ʶ�Ϊ��̬����ʼ�¶������ͬ(T1�桢2L.�ܱ�����)����Ӧ�����в������ݼ��±���
CH3OH(g) + H2O(g) ��H<0�е��������ʶ�Ϊ��̬����ʼ�¶������ͬ(T1�桢2L.�ܱ�����)����Ӧ�����в������ݼ��±���
��Ӧʱ�� | CO2 (mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
��ӦI ���º��� | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
��ӦII���Ⱥ��� | 0 min | 0 | 0 | 2 | 2 |
�ٴﵽƽ��ʱ����ӦI��II�Աȣ�ƽ�ⳣ��K( I ) ______K(II)(����>����<������=������ͬ����ƽ��ʱCH3OH��Ũ��c(I)_______c(II)��
�ڶԷ�ӦI��ǰ10 min�ڵ�ƽ����Ӧ����v(CH3OH) =________�����������������£���30 minʱֻ�ı��¶�ΪT2�棬��ʱH2�����ʵ���Ϊ3.2 mol����T1_____T2(������>����<������=��)����30 minʱֻ���������ٳ���1 mol CO2(g)��1mol H2O(g)����ƽ��______�ƶ�(����������������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Ԫ�ؼ��仯�����˵����ȷ����
A.��ƿ��Ʊ����ᾭ��������S![]() SO3
SO3![]() H2SO4
H2SO4
B.�����������еĽ��������ﷴӦ����Ԫ���Ե��ʵ���ʽ����������
C.��ȼú�м���ʯ��ʯ�ɼ���SO2�ŷţ������ķ�ӦΪ2CaCO3��2SO2��O2![]() 2CO2��2CaSO4
2CO2��2CaSO4
D.����Һ�м���BaCl2��Һ��μ����ᣬ����������������İ�ɫ����������Һ�غ�SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ͼΪ�ⶨ�к��ȵ�ʵ��װ��ͼ����ش��������⣺
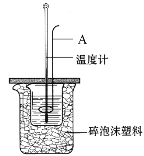
������A������Ϊ___��
�������0.50mol��L-1��������������ƹ������ʵ�飬��ʵ��������������к���������ֵ��___(�ƫ����ƫС�����䡱)
(2)���ڷ��֣�H2S�Ǽ�NO��CO֮��ĵ�����������ϵ�����źŷ��ӣ������в���������źŴ��ݡ�����Ѫ�ܼ����Ѫѹ�Ĺ��ܡ���ͼ��ͨ���Ȼ�ѧѭ���ڽϵ��¶�����ˮ������ֽ��Ʊ������ķ�Ӧϵͳԭ����

�ٸ�����ͼ����д��ϵͳ(II)��������Ȼ�ѧ����ʽ___��
��ϵͳ(I)��ϵͳ(II)��ȣ��Ƶõ���H2�����������ٵ���__������I������II������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ���м���һ���������ۣ���Һ©���м���һ�����Ũ��Ϊ12 mol��L��1�����ᣬ���ȴ�Һ©���Ļ�����ʹ���ַ�Ӧ��
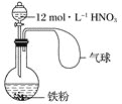
����������![]() ���� Fe3������H������ NO���� NO2���ڸ�װ����һ���������ڵ�(����)
���� Fe3������H������ NO���� NO2���ڸ�װ����һ���������ڵ�(����)
A.��B.�٢�C.�ڢܢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com