
ΓΨΧβΡΩΓΩ”–ΜζΈο![]() ÷ΜΚ§”–
÷ΜΚ§”–![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() »ΐ÷÷‘ΣΥΊΘ§≥Θ”ΟΉς”–ΜζΚœ≥…ΒΡ÷–ΦδΧεΓΘ
»ΐ÷÷‘ΣΥΊΘ§≥Θ”ΟΉς”–ΜζΚœ≥…ΒΡ÷–ΦδΧεΓΘ![]() ΗΟ”–ΜζΈο‘ΎΉψΝΩ
ΗΟ”–ΜζΈο‘ΎΉψΝΩ![]() ÷–≥δΖ÷»Φ…’…ζ≥…
÷–≥δΖ÷»Φ…’…ζ≥…![]()
![]() ΚΆ
ΚΆ![]()
![]() Θ§÷ ΤΉΆΦ±μΟςΤδœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ84Θ§Ζ÷ΈωΤδΚλΆβΙβΤΉΆΦΩ…÷Σ
Θ§÷ ΤΉΆΦ±μΟςΤδœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ84Θ§Ζ÷ΈωΤδΚλΆβΙβΤΉΆΦΩ…÷Σ![]() Ζ÷Ή”÷–Κ§”–
Ζ÷Ή”÷–Κ§”–![]() ΦϋΚΆΈΜ”ΎΕΥΒψ¥ΠΒΡ
ΦϋΚΆΈΜ”ΎΕΥΒψ¥ΠΒΡ![]() ΦϋΘ§ΚΥ¥≈Ι≤’ώ«βΤΉ…œ”–»ΐΉιΖεΘ§ΖεΟφΜΐ÷°±»ΈΣ
ΦϋΘ§ΚΥ¥≈Ι≤’ώ«βΤΉ…œ”–»ΐΉιΖεΘ§ΖεΟφΜΐ÷°±»ΈΣ![]() ΓΘ
ΓΘ
(1)![]() ΒΡΖ÷Ή” Ϋ «______ΓΘ
ΒΡΖ÷Ή” Ϋ «______ΓΘ
(2)![]() ΒΡΫαΙΙΦρ Ϋ «______ΓΘ
ΒΡΫαΙΙΦρ Ϋ «______ΓΘ
(3)œ¬Ν–Έο÷ ÷–Θ§“ΜΕ®ΧθΦΰœ¬Ρή”κ![]() ΖΔ…ζΖ¥”ΠΒΡ «______Θ®Χν–ρΚ≈Θ©ΓΘ
ΖΔ…ζΖ¥”ΠΒΡ «______Θ®Χν–ρΚ≈Θ©ΓΘ
AΘ°![]() BΘ°
BΘ°![]()
CΘ°Υα–‘![]() »ή“Κ DΘ°
»ή“Κ DΘ°![]() ΒΡ
ΒΡ![]() »ή“Κ
»ή“Κ
(4)”–ΜζΈο![]() «
«![]() ΒΡΆ§Ζ÷“λΙΙΧεΘ§
ΒΡΆ§Ζ÷“λΙΙΧεΘ§![]()
![]() ΉνΕύΩ…”κ
ΉνΕύΩ…”κ![]()
![]() Άξ»ΪΦ”≥…ΓΘ“―÷Σ
Άξ»ΪΦ”≥…ΓΘ“―÷Σ![]() ÷–Υυ”–ΧΦ‘≠Ή”‘ΎΆ§“ΜΗωΤΫΟφ…œΘ§«“ΟΜ”–Υ≥Ζ¥“λΙΙœ÷œσΘ§‘ρ
÷–Υυ”–ΧΦ‘≠Ή”‘ΎΆ§“ΜΗωΤΫΟφ…œΘ§«“ΟΜ”–Υ≥Ζ¥“λΙΙœ÷œσΘ§‘ρ![]() ΒΡΫαΙΙΦρ ΫΈΣ______ΓΘ
ΒΡΫαΙΙΦρ ΫΈΣ______ΓΘ
ΓΨ¥πΑΗΓΩ![]()
 ABCD
ABCD 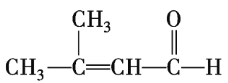
ΓΨΫβΈωΓΩ
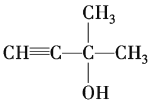
ΗυΨί”–ΜζΈο»Φ…’Ζ®ΦΤΥψ‘ΣΥΊ‘≠Ή”±»άΐΘ§ΚΥ¥≈Ι≤’ώ«βΤΉœ‘ Ψ”–ΜζΈο÷–«βΜΖΨ≥”–3÷÷Θ§ΖεΟφΜΐ±μ ΨΆ§ΜΖΨ≥«β‘≠Ή”ΒΡΗω ΐΘ§Ψί¥ΥΜΊ¥πΈ ΧβΓΘ
![]() ΗΟ”–ΜζΈοœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ84Θ§‘ΎΉψΝΩ
ΗΟ”–ΜζΈοœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ84Θ§‘ΎΉψΝΩ![]() ÷–≥δΖ÷»Φ…’…ζ≥…
÷–≥δΖ÷»Φ…’…ζ≥…![]()
![]() ΚΆ
ΚΆ![]()
![]() Θ§Φ¥nΘ®”–ΜζΈοΘ©ΘΚnΘ®C‘≠Ή”Θ©ΘΚnΘ®H‘≠Ή”Θ©=
Θ§Φ¥nΘ®”–ΜζΈοΘ©ΘΚnΘ®C‘≠Ή”Θ©ΘΚnΘ®H‘≠Ή”Θ©=![]() =1ΘΚ5ΘΚ8ΘΜΗυΨίΈο÷ œύΕ‘‘≠Ή”÷ ΝΩΩ…÷ΣΘ§Ζ÷Ή”÷–Κ§”–1Ηω―θ‘≠Ή”Θ§Φ¥Ζ÷Ή” ΫΈΣC5H8OΘΜΤδΚλΆβΙβΤΉΆΦΩ…÷ΣΘ§
=1ΘΚ5ΘΚ8ΘΜΗυΨίΈο÷ œύΕ‘‘≠Ή”÷ ΝΩΩ…÷ΣΘ§Ζ÷Ή”÷–Κ§”–1Ηω―θ‘≠Ή”Θ§Φ¥Ζ÷Ή” ΫΈΣC5H8OΘΜΤδΚλΆβΙβΤΉΆΦΩ…÷ΣΘ§![]() Ζ÷Ή”÷–Κ§”–
Ζ÷Ή”÷–Κ§”–![]() ΦϋΚΆΈΜ”ΎΕΥΒψ¥ΠΒΡ
ΦϋΚΆΈΜ”ΎΕΥΒψ¥ΠΒΡ![]() ΦϋΘ§ΚΥ¥≈Ι≤’ώ«βΤΉ…œ”–»ΐΉιΖεΘ§ΖεΟφΜΐ÷°±»ΈΣ
ΦϋΘ§ΚΥ¥≈Ι≤’ώ«βΤΉ…œ”–»ΐΉιΖεΘ§ΖεΟφΜΐ÷°±»ΈΣ![]() Θ§Φ¥ΫαΙΙ÷–Κ§”–2ΗωΦΉΜυΘ§ΫαΙΙΦρ ΫΈΣ
Θ§Φ¥ΫαΙΙ÷–Κ§”–2ΗωΦΉΜυΘ§ΫαΙΙΦρ ΫΈΣ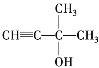 ΓΘ
ΓΘ
(1)Ψί“‘…œΖ÷ΈωΩ…÷ΣΘΚ![]() ΒΡΖ÷Ή” Ϋ «C5H8OΘΜ
ΒΡΖ÷Ή” Ϋ «C5H8OΘΜ
(2)![]() ΒΡΫαΙΙΦρ Ϋ «
ΒΡΫαΙΙΦρ Ϋ « ΘΜ
ΘΜ
(3)”–ΜζΈοA÷–ΙΌΡήΆ≈ΫαΙΙ”–ΧΦΧΦ»ΐΦϋΘ§τ«ΜυΘ§Ι ΡήΖΔ…ζ«βΤχΚΆ“ΚδεΒΡΦ”≥…Ζ¥”ΠΘ§”κΥα–‘ΗΏΟΧΥαΦΊΒΡ―θΜ·Ζ¥”ΠΘ§”κΒΞ÷ ΡΤΖΔ…ζΒΡ÷ΟΜΜΖ¥”ΠΘ§¥πΑΗΈΣABCDΓΘ
(4)”–ΜζΈο![]() «
«![]() ΒΡΆ§Ζ÷“λΙΙΧεΘ§
ΒΡΆ§Ζ÷“λΙΙΧεΘ§![]()
![]() ΉνΕύΩ…”κ
ΉνΕύΩ…”κ![]()
![]() Άξ»ΪΦ”≥…Θ§Φ¥÷ΜΚ§”–“ΜΗω≤Μ±ΞΚΆΧΦΧΦΥΪΦϋΓΘ“―÷Σ
Άξ»ΪΦ”≥…Θ§Φ¥÷ΜΚ§”–“ΜΗω≤Μ±ΞΚΆΧΦΧΦΥΪΦϋΓΘ“―÷Σ![]() ÷–Υυ”–ΧΦ‘≠Ή”‘ΎΆ§“ΜΗωΤΫΟφ…œΘ§«“ΟΜ”–Υ≥Ζ¥“λΙΙœ÷œσΘ§‘ρBΒΡΚ§―θΙΌΡήΆ≈ΈΣ»©ΜυΘ§
÷–Υυ”–ΧΦ‘≠Ή”‘ΎΆ§“ΜΗωΤΫΟφ…œΘ§«“ΟΜ”–Υ≥Ζ¥“λΙΙœ÷œσΘ§‘ρBΒΡΚ§―θΙΌΡήΆ≈ΈΣ»©ΜυΘ§![]() ΒΡΫαΙΙΦρ ΫΈΣ
ΒΡΫαΙΙΦρ ΫΈΣ![]() ΓΘ
ΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “‘Ύ’τΝσ…’ΤΩ÷–Φ”NaBrΓΔ ΝΩΥ°ΓΔ95%ΒΡ““¥ΦΚΆ≈®ΝρΥαΘ§”ΟΨΤΨΪΒΤΕ‘…’ΤΩΈΔ»»Θ§±ΏΖ¥”Π±Ώ’τΝσΘ§’τ≥ωΒΡδε““Άι”ΟΥ°œ¬ ’Φ·Ζ®ΜώΒΟΓΘΤδ÷–Ω…ΡήΖΔ…ζΒΡΗ±Ζ¥”Π”–ΘΚ2HBr+H2SO4Θ®≈®Θ©ΓζBr2+SO2![]() +2H2O
+2H2O
Άξ≥…œ¬Ν–ΧνΩ’ΘΚ
Θ®1Θ©÷Τ±Ηδε““ΆιΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ_________ΓΔ_______ΓΘ
Θ®2Θ©Ζ¥”Π÷–Φ”»κ…ΌΝΩΥ°≤ΜΡή≤ζ…ζΒΡΉς”Ο «__________Θ®―ΓΧν±ύΚ≈Θ©
A Ζά÷Ιδε““Άι±Μ≈®ΝρΥα―θΜ· B Φθ…ΌδεΜ·«βΒΡΜ”ΖΔ
C ΙΖ¥”ΠΜλΚœΈοΖ÷≤ψ D »ήΫβδεΜ·ΡΤ
Θ®3Θ©ΈΣΝΥ±Θ÷Λ»ίΤςΨυ‘» ή»»ΚΆΩΊ÷ΤΚψΈ¬Θ§Φ”»»ΖΫΖ®ΉνΚΟ≤…”Ο________ΓΘ
Θ®4Θ©≤…”Ο±ΏΖ¥”Π±Ώ’τΝσΒΡ≤ΌΉς…ηΦΤΘ§Τδ÷ς“ΣΡΩΒΡ «_________ΓΘ
Θ®5Θ©δε““ΆιΩ…”ΟΥ°œ¬ ’Φ·Ζ®ΜώΒΟΒΡ“άΨί «___________ΓΘ
Θ®6Θ©œ¬Ν–ΉΑ÷Ο‘Ύ Β―ι÷–Φ»ΡήΈϋ ’HBrΤχΧεΘ§”÷ΡήΖά÷Ι“ΚΧεΒΙΈϋΒΡ «__________Θ®―ΓΧν±ύΚ≈Θ©
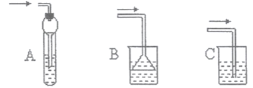
Θ®7Θ©¥÷≤ζΤΖ”ΟΥ°œ¥Β”Κσ”–Μζ≤ψ»‘≥ ΚλΉΊ…ΪΘ§”ϊ≥ΐ»ΞΗΟ‘”÷ Θ§Ω…Φ”»κΒΡ ‘ΦΝΈΣ________Θ®―ΓΧν±ύΚ≈Θ©
A ΒβΜ·ΦΊ»ή“Κ B ―«ΝρΥαΡΤ»ή“Κ C «β―θΜ·ΡΤ»ή“Κ
Θ®8Θ©“‘œ¬≤Ϋ÷ηΘ§Ω…”Ο”ΎΦλ―ιδε““Άι÷–δε‘ΣΥΊΘ§Τδ’ΐ»ΖΒΡ≤ΌΉςΥ≥–ρ «ΘΚ»Γ…ΌΝΩδε““ΆιΘ§»ΜΚσ_______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΨυ»ΐΦΉ±Ϋ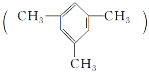 «“Μ÷÷“Ή»ΦΓΔ≤Μ»ή”ΎΥ°ΓΔ±»Υ°ΟήΕ»–ΓΒΡ”–ΕΨ“ΚΧεΘ§ «÷Ί“ΣΒΡ”–ΜζΜ·ΙΛ‘≠ΝœΘ§”Ο”Ύ÷Τ±ΗΚœ≥… ς÷§ΓΔΩΙ―θΜ·ΦΝΒ»ΓΘ
«“Μ÷÷“Ή»ΦΓΔ≤Μ»ή”ΎΥ°ΓΔ±»Υ°ΟήΕ»–ΓΒΡ”–ΕΨ“ΚΧεΘ§ «÷Ί“ΣΒΡ”–ΜζΜ·ΙΛ‘≠ΝœΘ§”Ο”Ύ÷Τ±ΗΚœ≥… ς÷§ΓΔΩΙ―θΜ·ΦΝΒ»ΓΘ
(1)Ψυ»ΐΦΉ±Ϋ τ”Ύ±ΫΒΡΆ§œΒΈοΘ§―ÔϓΜ÷÷ ‘ΦΝ«χ±π±ΫΚΆΨυ»ΐΦΉ±ΫΘΚ________________ΓΘ
(2)Ψυ»ΐΦΉ±ΫΖ÷Ή”÷–ΒΡ“ΜΗωH‘≠Ή”±ΜCl‘≠Ή”»Γ¥ζΘ§ΥυΒΟ≤ζΈο”–________÷÷ΓΘ
(3)œ¬Ν– τ”Ύ±ΫΒΡΆ§œΒΈοΒΡ «________(ΧνΉ÷ΡΗ)ΓΘ
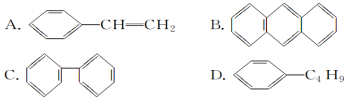
(4)œ¬Ν–Έο÷ ÷–Θ§ΡήΖΔ…ζΦ”≥…Ζ¥”ΠΘ§“≤ΡήΖΔ…ζ»Γ¥ζΖ¥”ΠΘ§Ά§ ±Ρή ΙδεΥ°“ρΦ”≥…Ζ¥”ΠΕχΆ …ΪΘ§ΜΙΡή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΒΡ «________(ΧνΉ÷ΡΗ)ΓΘ
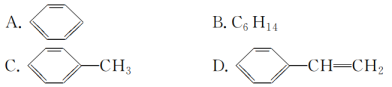
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œΩ…”ΟΗτΡΛΒγΫβ≤έΒγΫβ ≥―ΈΥ°ΒΡΖΫΖ®ά¥÷Τ»ΓNaOHΓΔCl2ΚΆH2Θ§≤Δ“‘ΥϋΟ«ΈΣ‘≠Νœ…ζ≤ζ“ΜœΒΝ–Μ·ΙΛ≤ζΤΖΘ§»γ¥Έ¬»ΥαΡΤΒ»ΓΘΗυΨίΧβ“βΆξ≥…œ¬Ν–ΦΤΥψΘΚ
(1)Ρ≥¬»Φν≥ß≤βΒΟΡ≥ΉιΒγΫβ≤έΒΡ―τΦΪΟΩ–Γ ±≤ζ…ζΤχΧε485.92m3(’έΥψΒΫ±ξΉΦΉ¥ΩωΘ§œ¬Ά§)Θ§Κœ________________molΘΜ≤β÷ΣΤδ÷–Cl2ΒΡΧεΜΐΖ÷ ΐΈΣ0.985(‘”÷ ΈΣO2)Θ§‘ρΗΟΤχΧεΒΡΟήΕ»ΈΣ________________ΘΜ“θΦΪ≤ζ…ζNaOH_________mol(±ΘΝτΥΡΈΜ”––ß ΐΉ÷Θ§œ¬Ά§)ΓΘ
(2)œ¬±μΧαΙ©ΝΥΝΫΦΪ»ή“Κ≈®Ε»ΒΡ±δΜ· ΐΨί(“θ―τΝΫΗωΦΪ«χΒΡΈοΝœ≤ΜΝςΆ®Θ§Κω¬‘Τδ÷–»ή“ΚΒΡΧεΜΐ±δΜ·)ΓΘ
“θΦΪΘΚNaOH»ή“Κ÷ ΝΩΖ÷ ΐ | ―τΦΪΘΚNaCl»ή“Κ≈®Ε»(g/L) | |
ΫχΝœ“Κ | 0.30 | 310 |
ΒγΫβΚσ | 0.32 | 210 |
»τΡ≥ΗωΒγΫβ≤έΟΩ–Γ ±ΫχNaOH»ή“Κ52.000 kgΘ§ΒΟΒΫΦν»ή“Κ≥θ≤ζΤΖ90.416 kgΘ§‘ρ―τΦΪ«χΟΩ–Γ ±Φ”»κNaCl»ή“Κ_______________m3ΓΘ»ΓΦν»ή“Κ≥θ≤ζΤΖ÷–ΒΡ40% Φ”»κ“ΜΕ®ΝΩ¥ΩΥ°Θ§¥οΒΫ“θΦΪΫχΝœ“ΚΒΡ≈®Ε»“Σ«σΘ§‘ρ–η“ΣΦ”»κ¥ΩΥ°_________________LΓΘ
(3)≤ζΤΖ÷°“Μ----Τ·Υ°(NaClO»ή“Κ)ΨΏ”–ΝΦΚΟΒΡœϊΕΨΓΔΤ·ΑΉΡήΝΠΓΘ‘Ύ÷ΤΤ·Υ°Ιΐ≥Χ÷–»Γ1L»ή“ΚΘ§≤βΒΟpH=12(Κω¬‘Υ°Ϋβ)Θ§NaClOΚ§ΝΩΈΣ0.3725gΓΘ‘Ύ“ΜΕ®ΧθΦΰœ¬Θ§ΫΪΗΟ»ή“Κ÷Τ≥…ΨßΧεΘ§÷ ΝΩΉνΕύΈΣ1.335gΓΘΆ®ΙΐΝ– ΫΦΤΥψΘ§–¥≥ωΗΟΨßΧεΒΡΜ·―ß Ϋ_________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ![]() Ρ≥”–ΜζΈο
Ρ≥”–ΜζΈο![]() ”κΉψΝΩΒΡ―θΤχ≥δΖ÷Ζ¥”ΠΚσΘ§ΫΪΥυΒΟΤχΧε≤ζΈο“ά¥ΈΆ®Ιΐ Δ”–≈®ΝρΥαΚΆΦν ·Μ“ΒΡΉΑ÷ΟΘ§ΝΫΉΑ÷ΟΖ÷±π‘ω÷Ί
”κΉψΝΩΒΡ―θΤχ≥δΖ÷Ζ¥”ΠΚσΘ§ΫΪΥυΒΟΤχΧε≤ζΈο“ά¥ΈΆ®Ιΐ Δ”–≈®ΝρΥαΚΆΦν ·Μ“ΒΡΉΑ÷ΟΘ§ΝΫΉΑ÷ΟΖ÷±π‘ω÷Ί![]() ΓΔ
ΓΔ![]() ΘΜΆ§Έ¬Ά§―Ιœ¬Θ§
ΘΜΆ§Έ¬Ά§―Ιœ¬Θ§![]() ’τΤχΒΡΟήΕ» «
’τΤχΒΡΟήΕ» «![]() ΒΡ37±ΕΓΘ‘ρΡήΙΜ”κΡΤΖ¥”ΠΖ≈≥ω
ΒΡ37±ΕΓΘ‘ρΡήΙΜ”κΡΤΖ¥”ΠΖ≈≥ω![]() ΒΡ
ΒΡ![]() ΒΡΫαΙΙ”–Θ®≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ©Θ® Θ©
ΒΡΫαΙΙ”–Θ®≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ©Θ® Θ©
A.6÷÷B.5÷÷C.4÷÷D.3÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥÷ΜΚ§ΧζΓΔ―θΝΫ÷÷‘ΣΥΊΒΡ―υΤΖAΘ§ΗΏΈ¬ ±”κΉψΝΩΒΡCO≥δΖ÷Ζ¥”ΠΘ§…ζ≥…ΒΡΤχΧε±ΜΉψΝΩ≥Έ«ε ·Μ“Υ°Έϋ ’Θ§≤βΒΟ≥ΝΒμΒΡ÷ ΝΩ”κ‘≠―υΤΖA÷ ΝΩœύΒ»ΓΘ»γΙϊA÷–÷ΜΚ§ΝΫ÷÷Έο÷ Θ§‘ρA÷–“ΜΕ®Κ§”–(ΓΓΓΓ)
A. FeO B. Fe2O3 C. Fe3O4 D. Fe
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ1-δεΕΓΆιΘ®ΟήΕ»1.2758 g/mLΘ© «÷Ί“ΣΒΡ”–ΜζΚœ≥…÷–ΦδΧεΦΑ”–Μζ»ήΦΝΘ§Ω…“‘‘Ύ Β―ι “άο”ΟδεΜ·ΡΤΓΔ≈®ΝρΥαΚΆ1-ΕΓ¥ΦΈΣ‘≠ΝœΘ§Ψ≠Ιΐ»γΆΦΝυ≤Ϋ÷ΤΒΟΓΘ
Άξ≥…œ¬Ν–ΧνΩ’ΘΚ
Θ®1Θ©Ά®Ιΐ≤Ϋ÷ηΔΎΜώΒΟ¥÷≤ζΤΖΘ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «___ΓΘ¥Υ ±≤ζΤΖΆυΆυ≥ ΚλΉΊ…ΪΘ§‘≠“ρ «____ΓΘ Β―ι “άο”–œ¬Ν–≥Θ”Ο ‘ΦΝΘ§«κΗυΨί Β―ι–η“ΣΈΣ”κ≤Ϋ÷ηΔήœύΙΊΒΡΘ®2Θ©Θ®3Θ©–ΓΧβ―Γ‘ώ ‘ΦΝΘ§≤Δ”Ο ‘ΦΝ±ύΚ≈ΧνΩ’ΘΚ
aΘ°NaOH»ή“Κ bΘ°NaHCO3»ή“Κ cΘ°NaHSO3 »ή“Κ dΘ°NaBr»ή“Κ
Θ®2Θ©≤ζΤΖΒΡΚλΉΊ…ΪΩ…”Ο___≥ΐ»ΞΘ®Χν–¥ ‘ΦΝ±ύΚ≈Θ©Θ§œύ”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___ΓΘ
Θ®3Θ©―Γ”Ο≈®ΝρΥαœ¥»ΞΈ¥Ζ¥”ΠΒΡ1-ΕΓ¥ΦΚΆ”–ΜζΗ±≤ζΈοΘ§»ΜΚσ≥ΐΥαΓΘΉν “ΥΒΡ≥ΐΥα ‘ΦΝ «__Θ®Χν–¥ ‘ΦΝ±ύΚ≈Θ©ΓΘ
Θ®4Θ©”Ο≈®ΝρΥαΘ®ΟήΕ»1.84g/mLΘ©œ¥Β” ±Θ§≤…”Ο___Θ®Χν–¥“«ΤςΟϊ≥ΤΘ©Ζ÷άκ≥ω___Θ®Χν–¥ΓΑ…œΓ±ΜρΓΑœ¬Γ±Θ©≤ψ≤ζΈοΓΘ
Θ®5Θ©Φλ―ι≤ζΈο÷–Κ§”–δε‘ΣΥΊΒΡ Β―ιΖΫΖ® «____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬±μΝ–≥ωΝΥ‘ΣΥΊ÷ήΤΎ±μ÷–«Α20Κ≈‘ΣΥΊ÷–Ρ≥–©‘ΣΥΊ–‘÷ ΒΡ“Μ–© ΐΨίΘΚ
–‘÷ ‘ΣΥΊ | ‘≠Ή”ΑκΨΕΘ® | ΉνΗΏΦέΧ§ | ΉνΒΆΦέΧ§ |
ΔΌ | 1.02 |
|
|
ΔΎ | 2.27 |
| ΓΣ |
Δέ | 0.74 | ΓΣ |
|
Δή | 1.43 |
| ΓΣ |
Δί | 0.77 |
|
|
Δό | 1.10 |
|
|
ΔΏ | 0.99 |
|
|
Δύ | 1.86 |
| ΓΣ |
Δα | 0.75 |
|
|
Δβ | 1.17 |
|
|
‘ΜΊ¥πœ¬Ν–Έ ΧβΓΘ
Θ®1Θ©“‘…œ10÷÷‘ΣΥΊ÷–Θ§ΒΎ“ΜΒγάκΡήΉν–ΓΒΡ «______Θ®Χν–ρΚ≈Θ©ΓΘ
Θ®2Θ©…œ ωΔίΓΔΔόΓΔΔΏ»ΐ÷÷‘ΣΥΊ÷–ΒΡΡ≥ΝΫ÷÷‘ΣΥΊ–Έ≥…ΒΡΜ·ΚœΈο÷–Θ§ΟΩ“ΜΗω‘≠Ή”ΕΦ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΒΡΈο÷ ”–______Θ®ΧνΖ÷Ή” ΫΘ§ΝΫ÷÷Φ¥Ω…Θ©ΓΘ‘ΣΥΊΔαΚΆΔβ–Έ≥…ΒΡΜ·ΚœΈοΒΡΜ·―ß ΫΈΣ______ΘΜ‘ΣΥΊΔΌΒΡ‘≠Ή”ΦέΒγΉ”≈≈≤Φ Ϋ «______ΓΘ
Θ®3Θ©ΔΌΓΔΔόΓΔΔΏΓΔΔβΥΡ÷÷‘ΣΥΊΒΡΦρΒΞ«βΜ·ΈοΒΡΈ»Ε®–‘”…«ΩΒΫ»θΒΡΥ≥–ρ «______Θ®ΧνΜ·―ß ΫΘ©ΓΘ
Θ®4Θ©ΔέΚΆΔαΝΫ‘ΣΥΊœύ±»Θ§Ζ«Ϋπ τ–‘Ϋœ»θΒΡ «______Θ®ΧνΟϊ≥ΤΘ©Θ§Ω…“‘―ι÷ΛΗΟΫα¬έΒΡ «______Θ®Χν–ρΚ≈Θ©ΓΘ
AΘ°ΤχΧ§«βΜ·ΈοΒΡΜ”ΖΔ–‘
BΘ°ΒΞ÷ Ζ÷Ή”÷–ΒΡΦϋΡή
CΘ°ΝΫ‘ΣΥΊΒΡΒγΗΚ–‘
DΘ°Κ§―θΥαΒΡΥα–‘
EΘ°ΉνΦρΒΞ«βΜ·ΈοΒΡΈ»Ε®–‘
FΘ°ΝΫΒΞ÷ ‘ΎΉ‘»ΜΫγ÷–ΒΡ¥φ‘Ύ–Έ Ϋ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥―–ΨΩ–ΓΉιΫΪ¥ΩΨΜΒΡSO2ΤχΧεΆ®»κ0.1molL©¹1ΒΡBaΘ®NO3Θ©2»ή“Κ÷–Θ§ΒΟΒΫΝΥBaSO4≥ΝΒμΓΘΈΣΧΫΨΩ…œ ω»ή“Κ÷–ΚΈ÷÷ΈΔΝΘΡή―θΜ·Ά®»κΒΡSO2Θ§ΗΟ–ΓΉιΧα≥ωΝΥ»γœ¬ΦΌ…ηΘΚ
ΦΌ…η“ΜΘΚ»ή“Κ÷–ΒΡNO3-
ΦΌ…ηΕΰΘΚ»ή“Κ÷–»ήΫβΒΡO2ΘΜ
(1)―ι÷ΛΦΌ…η“Μ
ΗΟ–ΓΉι…ηΦΤ Β―ι―ι÷ΛΝΥΦΌ…η“ΜΘ§«κ‘Ύœ¬±μΩ’ΑΉ¥ΠΧν–¥œύΙΊ Β―ιœ÷œσΘ°
Β―ι≤Ϋ÷η | Β―ιœ÷œσ | Ϋα¬έ |
Β―ι1ΘΚ‘Ύ Δ”–≤ΜΚ§O2ΒΡ25mL0.1molL©¹1BaCl2»ή“ΚΒΡ…’±≠÷–Θ§ΜΚ¬ΐΆ®»κ¥ΩΨΜΒΡSO2ΤχΧε | _______ | ΦΌ…η“Μ≥…ΝΔ |
Β―ι2ΘΚ‘Ύ Δ”–≤ΜΚ§O2ΒΡ25mL0.1molL©¹1Ba(NO3)2»ή“ΚΒΡ…’±≠÷–Θ§ΜΚ¬ΐΆ®»κ¥ΩΨΜΒΡSO2ΤχΧε | ________ |
ΈΣ…ν»κ―–ΨΩΗΟΖ¥”ΠΘ§ΗΟ–ΓΉιΜΙ≤βΒΟ…œ ωΝΫΗω Β―ι÷–»ή“ΚpHΥφΆ®»κSO2ΧεΜΐΒΡ±δΜ·«ζœΏ»γΆΦΓΘ Β―ι1÷–»ή“ΚpH±δ–ΓΒΡ‘≠“ρ «____________ΘΜV1 ±Θ§ Β―ι2÷–»ή“ΚpH–Γ”Ύ Β―ι1ΒΡ‘≠“ρ «__________ΓΘΘ®”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΘ©
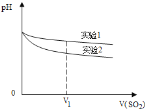
(2)―ι÷ΛΦΌ…ηΕΰ
«κ…ηΦΤ Β―ι―ι÷ΛΦΌ…ηΕΰΘ§–¥≥ω Β―ι≤Ϋ÷ηΓΔ‘ΛΤΎœ÷œσΚΆΫα¬έΘΚ
Β―ι≤Ϋ÷η | Β―ιœ÷œσ | Ϋα¬έ |
__________________ | ______________ | ΦΌ…ηΕΰ≥…ΝΔ |
(3)»τΦΌ…ηΕΰ≥…ΝΔΘ§«κ‘Λ≤βΘΚ‘ΎœύΆ§ΧθΦΰœ¬Θ§Ζ÷±π”ΟΉψΝΩΒΡO2ΚΆKNO3―θΜ·œύΆ§ΒΡH2SO3»ή“ΚΘ®»ή“ΚΧεΜΐ±δΜ·Κω¬‘≤ΜΦΤΘ©Θ§≥δΖ÷Ζ¥”ΠΚσΝΫ»ή“ΚΒΡpH«Α’Ώ_____________Θ®ΧνΓΑ¥σ”ΎΓ±ΜρΓΑ–Γ”ΎΓ±Θ©Κσ’ΏΘ§άμ”… «__________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com