
【题目】已知某化合物的晶体是由如图所示的最小结构单元密置堆积而成,下列关于该化合物叙述错误的是( )
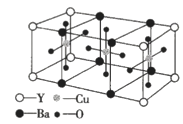
A.该化合物的化学式是YBa2Cu3O6
B.1mol该化合物中含有1molY
C.1mol该化合物中含有3molCu
D.1mol该化合物中含有2molBa
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为_____。
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为_____。
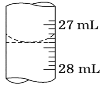
乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(4)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______(保留四位有效数字)。
(5)下列哪些操作会使测定结果偏高_____ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是第三周期部分元素的电离能数据,下列说法正确的是( )
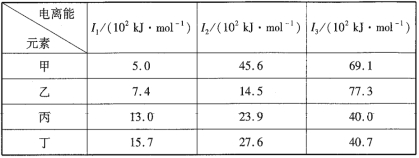
A.甲的金属性比乙弱B.乙的最高正化合价为+1
C.丙一定为非金属元素D.丁一定是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2007年诺贝尔化学奖授予埃特尔以表彰其对于合成氨反应机理的研究,氮气和氢气分子在催化剂表面的部分变化过程如图所示,下列说法不正确的是( )
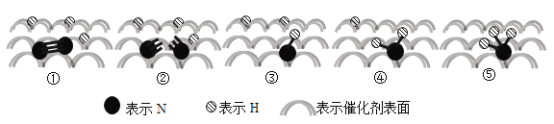
N2(g)+3H2(g)![]() 2NH3(g) △H = 92 kJ/mol
2NH3(g) △H = 92 kJ/mol
A.升高温度不能提高一段时间内NH3的产率
B.图①→②过程吸热,图②→③过程放热
C.N2在反应过程中三键均发生断裂
D.反应过程中存在NH、NH2等中间产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,1小时后观察到生铁明显锈蚀,由此得出的结论是
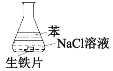
A.属于化学腐蚀
B.O2未参与反应
C.负极反应2Fe-6e+3H2O→Fe2O3+6H+
D.正极反应O2+4e- +2H2O→4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中进行如下反应:X(g)+3Y(g)![]() 2Z(g),X、Y、Z起始浓度分别是0.2mo1/L、0.6mol/L、0.4mol/L,当达到平衡时,下列数据可能正确的是
2Z(g),X、Y、Z起始浓度分别是0.2mo1/L、0.6mol/L、0.4mol/L,当达到平衡时,下列数据可能正确的是
A. X为0.25mol/L,Z为0.5mol/L B. Y为1.2mo1/L
C. X为0.3mol/L,Z为0.3mol/L D. Z为0.6mo1/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A.等物质的量的乙烯与乙醇完全燃烧消耗氧气的物质的量相等
B.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.苯乙烯和甲苯分子内所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如下:
该有机分子的核磁共振氢谱图如下(单位是ppm):
![]()
化学位移5
下列关于该有机物的叙述正确的是
A. 该有机物属于芳香族化合物
B. 键线式中的Et代表的基团为-CH3
C. 该有机物不同化学环境的氢原子有8种
D. 该有机物在氢氧化钠醇溶液加热的情况下能发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
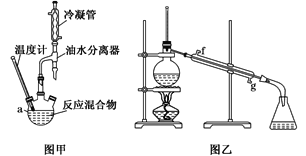
【题目】丙烯酸甲酯是一种重要的化工原料,实验室制备丙烯酸甲酯的反应、装置示意图和有关数据如下:
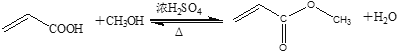
沸点(℃) | 溶解性 | 毒性 | |
丙烯酸 | 142 | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 65 | 与水互溶,易溶于有机溶剂 | 有毒 |
丙烯酸甲酯 | 80.5 | 难溶于水,易溶于有机溶剂 | 无毒 |
实验步骤:
①向三颈瓶中加入10.0g丙烯酸、6.0g甲醇、数滴浓硫酸和几粒沸石,缓慢加热。
②反应30min后,停止加热,反应液冷却后,分别用少量水、饱和碳酸氢钠溶液和水洗涤。
③取上层油状液体,用少量无水MgSO4干燥后蒸馏,收集70~90℃馏分。
回答下列问题:
(1)反应过程采用水浴加热,原因是___。
(2)图甲中油水分离器的作用是___。
(3)判断酯化反应达到平衡的现象为__。
(4)第一次水洗的主要目的是___。
(5)在洗涤、分液步骤中用到的主要玻璃仪器有烧杯、___。
(6)图乙所示装置中冷却水的进口为___(填字母)。
为分析产率,进行如下实验:将收集到的馏分平均分成五份,取出一份置于锥形瓶中,加入2.5mol/LKOH溶液10.00mL,加热使之完全水解;用酚酞作指示剂,向冷却后的溶液中滴加0.5mol/LHCl溶液,中和过量的KOH,共消耗盐酸20.00mL。
(7)本次制备实验的产率为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com