
����Ŀ��ij�������ۺϴ�����NH4+��ˮ��ҵ��������Ҫ��N2��CO2��SO2��NO��CO�������������ɷ֣���������������̣�
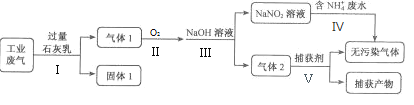
��֪����2NO2+2NaOH=NaNO3+NaNO2+H2O��NO+NO2+2NaOH=2NaNO2+H2O��
��1������1����Ҫ�ɷֳ�Ca(OH)2�⣬����__________ ��________ ���ѧʽ��;
��2�����������Ҫ��O2��Ӧ��_____����������������������������������ղ������������������________;
��3�������������NH4+��ˮʱ��������Ӧ�����ӷ���ʽΪ__________________;
��4��Ϊȷ���������NaNO3���ɣ�������Ӧ����NO��O2�����ʵ���֮��Ϊ_____����n(NO) :n(O2)=5:2��NaOH��Һ�����������������Һ��NaNO3��NaNO2�����ʵ���֮��Ϊ______________��
���𰸡�CaSO3 CaCO3 ���� CO NH4++ NO2- = N2+2H2O 4:1 3:7
��������
�������е����̣���ҵ����ͨ�������ʯ�����У�SO2��CO2��Ca(OH)2��Ӧ���ֱ�õ�CaSO3��CaCO3�������������1ΪCaSO3��CaCO3����������Ca(OH)2������1ΪN2��NO��CO��NO��������Ӧ����NO2��������Ϣ��֪��NO2������δ��Ӧ���NO�����ռ���Һ��Ӧ�������գ�����2ΪN2��CO��
��1���������е����̣���ҵ����ͨ�������ʯ�����У�����1����Ҫ�ɷֳ�Ca(OH)2�⣬����CaSO3��CaCO3������
��2��������������ԭ����O2������NO��ȫ������NO2������ͨ����Һ��õ������ƣ�����2ΪN2��CO����������Ⱦ������ΪN2���ʲ����������Ҫ��CO��
��3��NH4+��NO2-�ܹ��������з�Ӧ����N2�����ӷ���ʽΪNH4++ NO2- = N2+2H2O��
��4��NO+NO2+2NaOH=2NaNO2+H2O˵��n(NO)��n(NO2)Ϊ1��1ʱ����ȫתΪ�������ƣ���2NO+O2=2NO2����������2xmolNO2��������xmolO2��2xmolNO������n(NO)��n(NO2)Ϊ1��1��˵����Ӧʣ��2xmolNO�����ܼ�4xmolNO����ô������Ӧ����NO��O2�����ʵ���֮��Ϊ4��1��������2molO2��5molNO����ôNO��O2��Ӧ��õ�1molNO��4molNO2��1molNO��1molNO2ǡ����ȫ��Ӧ����2mol�������ƣ�ʣ��3molNO2�ͼ�Һ��Ӧ���䷽��ʽΪ2NO2+2NaOH=NaNO3+NaNO2+H2O�����ݼ�������ϵ��֪����1.5mol�����ƺ�1.5mol�������ƣ��ϼƹ�1.5mol�����ƺ�3.5mol�������ƣ�������������Һ��NaNO3��NaNO2�����ʵ���֮��Ϊ3��7��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е�����ָ����Һ��һ���ܴ����������(����)
A. c(FeCl3)��1.0 mol��L��1����Һ�У�HCO![]() ��Cl����H����Na��
��Cl����H����Na��
B. �����£���ˮ�������c(H��)��10��14mol��L��1��Һ�У�NH![]() ��K����CO
��K����CO![]() ��SO
��SO![]()
C. ��c(HCO![]() )��0.1 mol��L��1����Һ�У�NH
)��0.1 mol��L��1����Һ�У�NH![]() ��AlO
��AlO![]() ��Cl����NO
��Cl����NO![]()
D. �����£� 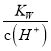 ��0.1 mol��L��1����Һ�У�K����NH3��H2O��SO
��0.1 mol��L��1����Һ�У�K����NH3��H2O��SO![]() ��NO
��NO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ի�����AΪԭ�Ϻϳɻ�����M����·����ͼ��ʾ��

��1��д��������B�к��������ŵ�����Ϊ________________��
��2���ٵķ�Ӧ����Ϊ________________��
��3��д��ͬʱ��������������E��һ��ͬ���칹��Ľṹ��ʽ_____________��
������FeCl3������ɫ��Ӧ�� �ڷ�������3�ֲ�ͬ��ѧ�������⣻
��4��E��Y��Ӧ����Mͬʱ�����ɼ״���д��Y(C5H8O4)�Ľṹ��ʽ__________________��
��5���Ա��ӡ��Ҵ���![]() Ϊ�л�ԭ�Ϻϳ�
Ϊ�л�ԭ�Ϻϳ� ��д���Ʊ��ĺϳ�·������ͼ (���Լ����ã��ϳ�·������ͼʾ�����������)______________��
��д���Ʊ��ĺϳ�·������ͼ (���Լ����ã��ϳ�·������ͼʾ�����������)______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ȷݡ�������һ��������ͭ�ۣ�������ܽ�19.2g (��֪����ֻ����ԭΪNO����)������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ�����з��������������

A. OA�β�������NO��AB�εķ�ӦΪFe+2Fe3+=3Fe2+��BC�β�������
B. ԭ�������SO42�����ʵ���Ϊ0.6 mol
C. �ڶ�����Һ����������ΪFeSO4
D. ȡ20mLԭ������ˮϡ����1L����Һ��c(H+)=0.2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������״���;����㷺��Խ��Խ�����̼ҵĹ�ע����ҵ�ϼ״��ĺϳ�;�����ֶ���������ʵ������ģ��״��ϳɷ�Ӧ,��2 L�ܱ������ڣ�400 ��ʱ������ӦCO(g)+2H2(g) ![]() CH3OH(g)����ϵ��n(CO)��ʱ��ı仯�����
CH3OH(g)����ϵ��n(CO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 5 |
n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

��1��ͼ�б�ʾCH3OH �ı仯��������_______��
��2�����д�ʩ������߷�Ӧ���ʵ���_________(������Ӧ��ĸ���)��
a.�����¶� b.������� c.����ѹǿ d.��ʱ�����CH3OH
��3������������˵����Ӧ�ﵽƽ��״̬����__________(������Ӧ��ĸ���)��
a.CO��H2��Ũ�ȱ��ֲ��� b.v(H2)=2 v(CO)
c.CO�����ʵ����������ֲ��� d.�����������ܶȱ��ֲ���
e.ÿ����1molCH3OH��ͬʱ��2molH-H������
��4��CH3OH��O2�ķ�Ӧ�ɽ���ѧ��ת��Ϊ���ܣ��乤��ԭ����ͼ��ʾ��ͼ��CH3OH��__________����A��B��ͨ�룬b���ĵ缫��Ӧʽ��__________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���(SnCl4)����ýȾ�����л��ϳ��ϵ��Ȼ�������ʵ�����Ʊ����Ȼ�����װ������ͼ(���ּг�װ������ȥ)����֪���ٽ���������ʱͨ�����������Ӧ���������Ȼ���������ˮ���Ȼ����۵�-33�棬�е�114.1�棻����ˮ���Ȼ�����ˮ�������ɰ�ɫ����������˵������ȷ����

A. �١��ڡ��ޡ��ߵ��Թ�������ʢװMnO2������ʳ��ˮ��ŨH2SO4��NaOH��Һ
B. ʵ��ʱ�μ�Ũ���ᷴӦһ��ʱ�䣬Ȼ���ٵ�ȼ�ܴ��ľƾ���
C. ��װ�������ռ�SnCl4����������ˮԡ��Ч������
D. �ޡ��������Թܿ�����һ��װ�м�ʯ�ҵĸ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ������c(Cl-)������
A. 50mL0.1mol��L-1AlCl3��Һ B. 100mL0.1 mol��L-1MgCl2��Һ
C. 150mL0.3 mol��L-1KClO3��Һ D. 200mL0.2 mol��L-1NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ��ѡ��3�����ʽṹ������]
��1��Fe3+�ĵ����Ų�ʽΪ___________________����֪��Fe3���Ļ�ѧ���ʱ�Fe2���ȶ������ԭ�ӽṹ�ĽǶȽ��н���____________________��
��2��Fe����CO�γ������Fe(CO)5��1 mol Fe(CO)5�к���________ mol�Ҽ���
��3����CO��Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ________ ��_______(����һ�֣��ѧʽ)��
��4��ij��������Cu�������ʾ���ϼ�Ϊ+1������γ�ͼ����ʾ�����ӡ��������к��л�ѧ����������____________________��������ţ�
A�����Լ� B�����Ӽ� C���Ǽ��Լ� D����λ��
��5�����Ȼ�ͭ��Һ��ͨ�������Ķ����������ɰ�ɫ����M�� M�ľ����ṹ��ͼ����ʾ��д���÷�Ӧ�����ӷ���ʽ��____________________��
��6����֪��������Ԫ����ɵĻ�����AΪ�������뵼�塣��֪������A�ľ����ṹ����ʯ���ƣ��侧���ṹ��ͼ����ʾ����д��������A�Ļ�ѧʽ___________���軯����A�ľ����߳�Ϊ![]() pm����ÿ�������þ�����������Ԫ�ص�����Ϊ______________g��NA��ʾ�����ӵ�������ֵ����
pm����ÿ�������þ�����������Ԫ�ص�����Ϊ______________g��NA��ʾ�����ӵ�������ֵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л������������˫���ϵ�̼ԭ��������ԭ��(��ԭ����)ֱ�ӽ�������µĻ�������ӵķ�Ӧ�Ǽӳɷ�Ӧ�����й�����ӳɷ�Ӧ�ص��ǣ� ��
A.�����������Ļ�������ڹ�����������ɫ��dz
B.��ϩ����ˮ�����ˮ����ɫ��ȥ
C.��ϩ��ˮ��һ�������·�Ӧ��ȡ�Ҵ�
D.��ϩ���Ȼ�����һ�������·�Ӧ��ȡ������һ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com