
| A、氮氧化合物与碳氢化合物经紫外线照射可发生反应形成有毒烟雾 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、雾霾中含有大量超标的主要物质是二氧化硫 |
| D、食盐中的Na+的焰色反应呈黄色,属于化学变化 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、乙醇与乙酸都存在碳氧双键 |
| B、油脂水解可得到氨基酸和甘油 |
| C、淀粉和纤维素水解最终产物都是葡萄糖 |
| D、卤代烃加入硝酸酸化的硝酸银溶液可根据生成的卤化银沉淀颜色检验卤原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种,若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入的物质的量之间的关系如图所示,下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种,若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入的物质的量之间的关系如图所示,下列说法正确的是( )| A、溶液中一定不含有CO32-,可能含有SO42-和NO3- |
| B、溶液中的阳离子只有H+、Mg2+、Al3+ |
| C、溶液中n(NH4+)=0.2mol |
| D、n(H+):n(Al3+):n(Mg2+)=1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 铵盐质量(g) | 浓硫酸增加的质量(g) |
| 第一次 | 9.05 | 1.7 |
| 第二次 | 18.10 | 1.7 |
| 第三次 | 27.15 | a |
| 第四次 | 36.20 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):
W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):2- 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、放出热量关系:a<b<196 |
| B、三个容器内反应的平衡常数:③>①>② |
| C、达平衡时SO3的体积分数:③>① |
| D、SO2的转化率:②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验 | 装置或仪器 |
| A | 分离乙酸乙酯中混有的乙酸 |  |
| B | 用已知浓度NaOH滴定未知浓度盐酸 |  |
| C | 从KI和I2的固体混合物中回收I2 |  |
| D | 配制100mL 0.100 0mol?L-1 NaOH溶液 | 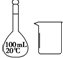 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验方案 | 现象 | 结论 |
| A |  | 向里推活塞时,长颈漏斗中有一段水柱,静止,水柱高度不变 | 该装置的气密性良好 |
| B |  | 脱脂棉燃烧 | Na2O2与水反应生成氢氧化钠和氧气 |
| C |  | 烧杯①的澄清石灰水先变浑浊 | NaHCO3比Na2CO3受热更易分解 |
| D | 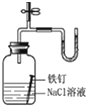 | U形管右端的液面高 | 铁钉发生吸氧腐蚀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 | ||
| B、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | ||
| C、某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、[Al(OH)4]-、SO42- | ||
D、常温下0.1 mol?L-1HA溶液的pH>1,0.1 mol?L-1BOH溶液中
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com