
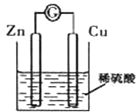
| A、铜为负极,产生气泡 |
| B、溶液变蓝色 |
| C、电子从锌极经导线流向铜极 |
| D、Zn、Cu 分别接外加电源的正、负极可在锌极镀上铜 |


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| A、仅有①② | B、仅有①③④⑤ |
| C、仅有①③⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、砷的+3价化合物的毒性强于+5价化合物 |
| B、砷原子最外层有3个电子 |
| C、砷化氢(AsH3)比NH3稳定 |
| D、砷酸(H3AsO4)的酸性强于磷酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有③ | B、②③ | C、③⑤ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次磷酸(H3PO2)是三元酸 |
| B、H3PO2中磷为+1价 |
| C、NaH2PO2溶液呈酸性 |
| D、次磷酸根离子为-3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 molAl与足量盐酸反应转移电子数为1NA |
| B、标准状况下,11.2L SO3所含的分子数为0.5NA |
| C、0.1molCH4所含的电子数为1NA |
| D、46gNO2和N2O4的混合物含有的分子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 3 |
| A、上式中的X为S4O62- |
| B、该反应中的还原剂为Fe2+和S2O32- |
| C、当生成1 mol Fe3O4时,转移电子的物质的量为4 mol |
| D、当3 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
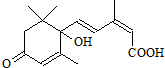
| A、其分子式为C15H22O4 |
| B、1mol该物质与NaOH溶液反应,最多消耗2mol NaOH |
| C、能发生加聚反应 |
| D、不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com