
【题目】叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。

(1)甲中含氧官能团是__________(填名称)。
(2)下列关于乙的说法正确的是________(填序号)。
a.分子中碳原子与氮原子的个数比是7∶5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________。
a.含有![]()
b.在稀硫酸中水解有乙酸生成
(4)写出丁在氢氧化钠溶液中水解的化学方程式。________
【答案】羧基 a、c ![]()
![]() +2NaOH → HOCH2CH(NH2)COONa+H2O+CH3COONa
+2NaOH → HOCH2CH(NH2)COONa+H2O+CH3COONa
【解析】
(1)甲含有氨基和羧基;
(2)a.该分子中C、N原子个数分别是7、5;
b.含有苯环的有机物属于芳香族化合物;
c.氨基能和酸反应、氯原子能和碱溶液反应;
d.该分子中含有N原子;
(3)丙的同分异构体丁中含有![]() 、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,据此判断丁的结构简式;
、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,据此判断丁的结构简式;
(4)丁为![]() ,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应。
,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应。
(1)甲含有氨基和羧基,含氧官能团为羧基;
(2)a.该分子中C、N原子个数分别是7、5,所以分子中碳原子与氮原子的个数比是7:5,a正确;
b.含有苯环的有机物属于芳香族化合物,该分子中没有苯环,所以不属于芳香族化合物,b错误;
c.氨基能和酸反应、氯原子能和碱溶液反应,所以该物质既能与盐酸又能与氢氧化钠溶液反应,c正确;
d.该分子中含有N原子,不属于苯酚的同系物,d错误;
故合理选项是ac;
(3)丙的同分异构体丁中含有、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,所以丁的结构简式为![]() ;
;
(4)丁为![]() ,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应,方程式为
,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应,方程式为![]() +2NaOH=HOCH2CH(NH2)COONa+H2O+CH3COONa。
+2NaOH=HOCH2CH(NH2)COONa+H2O+CH3COONa。


科目:高中化学 来源: 题型:
【题目】用下列有关实验装置进行的相应实验中,能达到实验目的的是
A.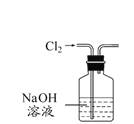 所示装置除去Cl2中含有的少量HCl
所示装置除去Cl2中含有的少量HCl
B.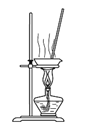 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 所示装置制取少量纯净的CO2气体
所示装置制取少量纯净的CO2气体
D.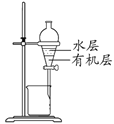 所示装置分离CCl4萃取碘水后已分层的有机层和水层
所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4)是重要的氨化剂,在潮湿的空气中能转化为碳酸铵,受热易分解、易被氧化。实验小组对氨基甲酸铵的性质进行了如下探究。请回答下列问题:
(1)氨基甲酸铵在潮湿的空气中转化为碳酸铵的化学方程式为____________________________。
(2)用下图装置探究氨基甲酸铵的分解产物(夹持装置略去,下同)。

①点燃A处的酒精灯之前,需先打开k,向装置中通入一段时间的N2,目的为_________________。
②仪器B的名称为_________________。
③装置D的作用为________________________________________________________。
④能证明分解产物中有NH3的现象为_________________________________________。
⑤试剂A用于检验分解产物中的CO2,该试剂的名称为_______________________。
(3)已知:CuO高温能分解为Cu2O和O2。若用上述装置和下列部分装置进一步检验分解产物中是否有CO,装置E后应依次连接_________________(按从左到右的连接顺序填选项字母)。
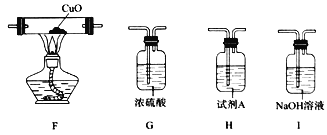
(4)通过实验得出结论:氨基甲酸铵受热分解为NH3和CO2。该反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据相关实验得出的结论正确的是
A. 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液
B. 已知I3-![]() I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
C. 将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯
D. 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤,可除去氯化镁溶液中少量氯化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。工业上,通过如下转化可制得KClO3晶体:![]()
(1) 与氯元素同族的短周期元素的原子核外电子排布式为______________________。
(2)上述转化过程中所涉及的短周期元素中,原子半径由大到小的顺序是______________。
(3)硫与氯同周期,写出一个能比较硫和氯非金属性强弱的化学反应方程式____________。硫单质不溶于水,易溶于CS2,则CS2分子的结构式为___________。
(4)电解氯化钠溶液可以得到NaClO3与H2。写出该反应的化学方程式,并标出电子转移的方向和数目_________________________________________________________________。
(5) II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体。该反应能够发生的原因是__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种天然黄铜矿主要成分为CuFeS2 (含SiO2),为了测定该黄铜矿的纯度,某同学设计了如图1实验:
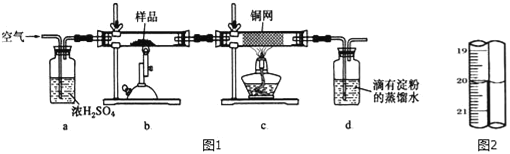
称取研细的黄铜矿样品1.150g煅烧,生成Cu、Fe2O3、FeO和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.01mo1/L标准碘溶液进行滴定,初读数为0.01mL,末读数如图2所示.
完成下列填空:
(1)实验中称量样品所需定量仪器为_____.
(2)装置c的作用是_____.
(3)上述反应结束后,仍需通一段时间的空气,其目的是_____.
(4)滴定时,标准碘溶液所耗体积为_____mL.用化学方程式表示滴定的原理:_____.
(5)计算该黄铜矿的纯度_____.
(6)工业上利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.选用提供的试剂,设计实验验证炉渣中含有FeO.提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液,所选试剂为_____.证明炉渣中含有FeO的实验现象为:_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 键角:BF3>CH4>H2O>NH3
B. CO2、HClO、HCHO分子中一定既有σ键又有π 键
C. 已知二茂铁(Fe(C5H5)2)熔点是173 ℃(在100 ℃时开始升华),沸点是249℃,不溶于水,易溶于苯等非极性溶剂。在二茂铁结构中,C5H5 -与Fe2+之间是以离子键相结合
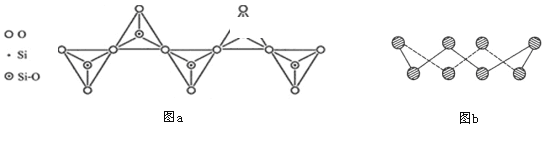
D. 在硅酸盐中,SiO44-四面体通过共用顶角氧离子形成一种无限长单链结构的多硅酸根如图a,其中Si原子的杂化方式与b图中S8单质中S原子的杂化方式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从植物中提取的天然化合物a-damascone,可用于制作“香水”,其结构为: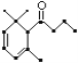 ,有关该化合物的下列说法不正确的是( )
,有关该化合物的下列说法不正确的是( )
A. 分子式为C13H20O
B. 1mo该化合物可与3molH2发生加成反应
C. 1mol该化合物完全燃烧消耗18 mol O2
D. 1mol该化合物最多与2mol溴单质加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com