
【题目】(1)在一体积为10 L的密闭容器中,通入一定量的CO和H2O,在850 ℃时发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图所示,则0~4 min的平均反应速率v(CO)=_____________ mol/(L·min)。
CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图所示,则0~4 min的平均反应速率v(CO)=_____________ mol/(L·min)。

(2)t℃(高于850 ℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①表中3~4 min时,反应处于_______________状态;c1数值_____________0.08 mol/L(填“大于”、“小于”或“等于”)。
②反应在4~5 min时,平衡向逆方向移动,可能的原因是____________(填字母,下同),表中5~6 min时,数值发生变化,可能的原因是________________。
a.增加水蒸气b.降低温度
c.使用催化剂d.增加氢气浓度
【答案】 0.03 化学平衡 大于 d a
【解析】本题主要考查化学平衡的移动。
(1)0~4 min的平均反应速率v(CO)=0.12/4mol/(L·min)=0.03mol/(L·min)。
(2)①表中3~4 min时,各物质浓度保持不变,所以反应处于化学平衡状态;850 ℃时,CO的平衡浓度是0.08mol/L,升温平衡左移,所以高于850 ℃时,c1数值大于0.08 mol/L。
②反应在4~5 min时,平衡向逆方向移动,可能的原因是d,原因:a.增加水蒸气,反应物浓度增大,平衡右移,不符合题意;b.降低温度,平衡右移,不符合题意;c.使用催化剂平衡不移动,不符合题意;d.增加氢气浓度,生成物浓度增大,平衡左移,符合题意。故选d。表中5~6 min时,数值发生变化,可能的原因是a。原因:a.增加水蒸气,由于c(H2O)增大,所以平衡右移,结果c(CO)减小,c(CO2)增大,符合题意;b.降低温度,使得平衡右移,结果c(H2O)减小,不符合题意;c.使用催化剂,平衡不移动,各成分浓度不变,不符合题意;d.增加氢气浓度,由于c(H2)增大,所以平衡左移,c(CO)增大,c(CO2)减小,不符合题意。故选a。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质分类正确的是
①混合物:盐酸、王水、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡
④同素异形体:C60、C70、金刚石、石墨.
A. ①③ B. ②④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是 ( )
A. 向Al2(SO4)3溶液中加入过量氨水:Al3+ + 4NH3·H2O == AlO2- + 4NH4+ + 2H2O
B. 酸性溶液中KIO3与KI反应:I- + IO3- + 6H+ == I2 + 3H2O
C. 碳酸钠与次氯酸反应:CO32- + 2HClO = 2ClO- + H2O + CO2↑
D. 碘化亚铁溶液与少量氯气反应:2I- + Cl2 = I2 + 2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
酸 | 碱 | 盐 | 氧化物 | |
A | H2SO4 | Na2CO3 | NaCl | SO2 |
B | CO2 | NaOH | NaCl | Na2CO3 |
C | HCl | NaOH | CaO | CH3COOH |
D | HNO3 | KOH | CaCO3 | CaO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的营养物质.某天然油脂A可发生下列反应:

已知:A的分子式为C57H106O6.1mol该天然油脂A经反应①可得到1molD、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C.经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1;
(1)写出B的分子式:________________________;
(2)写出反应①的反应类型:____________;C的名称(或俗称)是_________;
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程.下列有关说法不正确的是_______________;
a.氢化油又称人造奶油,通常又叫硬化油.
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病.
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂.
d.油脂的氢化与油脂的皂化都属于加成反应
(4)D和足量金属钠反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】血红蛋白(Hb)易与O2结合生成HbO2, CO吸入肺中发生反应:CO+HbO2![]() O2+HbCO,平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。假设空气中氧气的体积分数为20%。据此,下列结论错误的是
O2+HbCO,平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。假设空气中氧气的体积分数为20%。据此,下列结论错误的是
A. 当HbCO的浓度达到HbO2浓度的0.02倍时,反应达到平衡
B. 可以把CO中毒的病人放入高压氧仓中解毒
C. 血红蛋白结合CO的能力强于O2
D. 空气中CO的体积分数不能超过1.8×10-5,否则对人体有害
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液含有①NO3- ②HCO3- ③SO32- ④CO32- ⑤SO42- 等五种阴离子,向其中加入少量的过氧化钠固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)( )
A. ① B. ①⑤ C. ①④⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放显减少10%,二氧化碳(CO2)的排放量也要大幅减少。
(1)在恒温,容积为1L恒容中,硫可以发生如下较化,其反应过程和能量关系如图1所示(已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
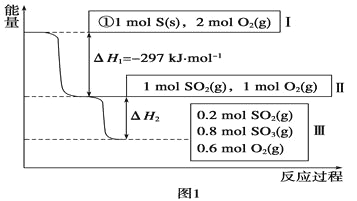
①写出能表示硫的燃烧热的热化学方程式:_________。,
②ΔH2=_________kJ·mol-1。
③在相同条件下,充入1molSO3和0.5mol的O2,则达到平衡时SO3的转化率为_______;此时该反应______(填“放出“或“吸收”)_______kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下40%~50%。
①CO2可转化成有机物实现碳循环。在休积为1L的密闭容器中,充入lmolCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3min到9min,v(H2)=_______mol/(L·min)
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3min到9min,v(H2)=_______mol/(L·min)
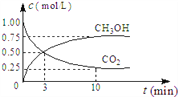
②为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有_______ (填编号)。
A.升高温度 B.缩小容器体积 C.再充入CO2气体 D.使用合适的催化剂
(3)工业上,CH3OH也可由CO2和H2合成。参考合成反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数。下列说法正确的是______________。
CH3OH(g)的平衡常数。下列说法正确的是______________。
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1molCO和0.2molH2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5MPa)和250℃,是因为此条件下,原料气转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com