
【题目】电导率可用于衡量电解质溶液导电能力的大小。向一定浓度的![]() 溶液中滴入某浓度的
溶液中滴入某浓度的![]() 溶液,其电导率随滴入的
溶液,其电导率随滴入的![]() 溶液体积的变化如图所示。下列说法不正确的是( )
溶液体积的变化如图所示。下列说法不正确的是( )
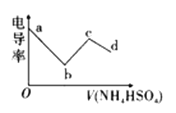
A. bc段的离子方程式为:![]()
B. c点溶液中:![]()
C. bc段之间存在某点,其溶液中:![]()
D. b点溶液存在三个平衡,且水的电离被抑制
【答案】B
【解析】
根据导电能力随滴入溶液体积的变化如图可知,b点时导电能力最弱,则n(NH4HSO4)=n[Ba(OH)2],该点溶液中发生的反应为NH4HSO4+Ba(OH)2=BaSO4↓+NH3·H2O+H2O,该点溶液中的溶质为NH3·H2O;c点时导电能力最强,n(NH4HSO4)=2n[Ba(OH)2],该点溶液中发生的反应为2NH4HSO4+Ba(OH)2=BaSO4↓+(NH4)2SO4+2H2O,该点溶液中溶质为 (NH4)2SO4,(NH4)2SO4是强酸弱碱盐;据此分析解答.
A、ab段电导率一直在下降,因此溶液中自由移动的离子浓度在减小,起始阶段,由于![]() 过量,所以发生的反应就是NH4HSO4+Ba(OH)2=BaSO4↓+NH3·H2O+H2O,
过量,所以发生的反应就是NH4HSO4+Ba(OH)2=BaSO4↓+NH3·H2O+H2O,![]() ,b点时溶液的溶质为
,b点时溶液的溶质为![]() ,bc段为
,bc段为![]() 和
和![]() 的反应,产物为
的反应,产物为![]() ,故A正确;
,故A正确;
B、从b点到c点,溶液的电导率在增大,此时![]() 过量,发生的反应为:
过量,发生的反应为:![]() ,溶液的溶质是
,溶液的溶质是![]() ,根据电荷守恒:
,根据电荷守恒:![]() ,因为
,因为![]() ,所以
,所以![]() ,故B错误;
,故B错误;
C、从b点到c点的过程中,溶液由碱性变为酸性,所以可为中性,因此根据电荷守恒,![]() ,故C正确;
,故C正确;
D、b点时溶液中存在着![]() 的电离平衡、
的电离平衡、![]() 的溶解平衡和水的电离平衡,
的溶解平衡和水的电离平衡,![]() 的存在抑制了水的电离,故D正确;
的存在抑制了水的电离,故D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.22.4LCO和CO2的混合气体中所含的碳原子数一定是NA
B.常温常压下,32gO2和32gO3所含氧原子数都是NA
C.48gO2所含的分子数为3NA
D.标准状况下36 g H2O中原子的数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法淡化海水的原理如图所示。已知海水中含![]() 等离子,电极为惰性电极。下列叙述正确的是
等离子,电极为惰性电极。下列叙述正确的是
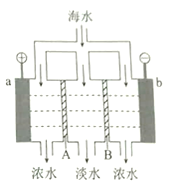
A. A是阳离子交换膜
B. 海水中阴离子移向b电极
C. a的电极反应为![]()
D. b极产生无色气体,出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据所给条件推出的结论不正确的是( )
选项 | 条件 | 结论 |
A | 在水溶液或熔融状态下可以导电的化合物,称为电解质 | 水中存在: |
B | 凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱 |
|
C | 联氨为二元弱碱,在水中的电离方式与氨相似 | 联氨与硫酸形成的酸式盐的化学式为: |
D | 发生化学反应时,接受电子对的物质为酸,提供电子对的物质为碱 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2 广泛用于造纸工业、污水处理等。工业上生产NaClO2 的工艺流程如下:
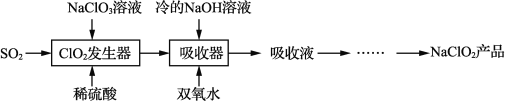
ClO2发生器中的反应为SO2 + 2NaClO3 + H2SO4 = 2ClO2↑+ 2NaHSO4
(1)NaClO3中Cl的化合价_______,上述反应中氧化剂是_______ ,被氧化的元素为_______。请用双线桥法表示该反应中电子转移的方向和数目SO2 + 2NaClO3 + H2SO4 = 2ClO2↑+ 2NaHSO4_______________________反应后,若产生0.6 mol气体,则电子转移的物质的量为 _______mol。
(2)吸收器中反应温度不能高于5℃的可能原因有 _______
(3)反应结束后,向ClO2发生器中通入一定量空气的目的是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯(![]() )可用于制备二茂铁(
)可用于制备二茂铁(![]() ,结构简式为
,结构简式为![]() ),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
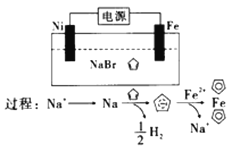
A. ![]() 为电解池的阳极
为电解池的阳极
B. 电解质溶液可以是![]() 的水溶液
的水溶液
C. 电解池的总反应方程式为:![]()
D. 电解质溶液中,当有![]() 的
的![]() 向
向![]() 电极移动时,同时在
电极移动时,同时在![]() 电极上产生了
电极上产生了![]() 的氢气
的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)质子数为17、中子数为20的原子可表示为________,Na+的结构示意图________。
(2)焰色反应是_______变化,将碳酸钠进行焰色反应,火焰呈________。
(3)漂白粉有效成分的化学式________,漂白粉发挥漂白作用的反应方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成C的溶液,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D。
(1)写出下列物质的化学式:B____________,E_____________。
(2)写出A→C的化学方程式,并标出电子转移的方向和数目:_______________
(3)写出C→D的离子方程式:________________________________。
(4)写出E→D的化学方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )
2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )

A. 反应开始时,B容器中化学反应速率快
B. A容器中X的转化率为40%,且比B容器中X的转化率小
C. 打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D. 打开K达新平衡后,升高B容器温度,A容器体积一定增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com