
【题目】如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )
2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )

A. 反应开始时,B容器中化学反应速率快
B. A容器中X的转化率为40%,且比B容器中X的转化率小
C. 打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D. 打开K达新平衡后,升高B容器温度,A容器体积一定增大
【答案】A
【解析】
A.起始VA=VB=aL,B中的物质的量大于A中的物质的量,即B装置中的浓度大于A装置中的浓度,所以反应开始时,B反应速率大于A反应速率,A正确;
B.等压、等温条件下,气体的体积之比大于气体的物质的量之比,达到平衡时,VA=1.2aL,所以平衡后混合气体的物质的量是2.4mol,设A物质反应了mmol。
X(g)+Y(g)![]() 2Z(g)+W(g)物质的量增多
2Z(g)+W(g)物质的量增多
1mol 1mol
mmol (2.4-2)mol=0.4mol
m=0.4,所以X物质的转化率=![]() =40%,而B装置是在等容条件下,反应向正反应方向移动时,使混合气体的物质的量增大,导致容器内气体压强增大,增大压强,平衡逆向移动,使物质X的转化率减小,所以A在物质X的转化率比B在X的转化率大,B错误;
=40%,而B装置是在等容条件下,反应向正反应方向移动时,使混合气体的物质的量增大,导致容器内气体压强增大,增大压强,平衡逆向移动,使物质X的转化率减小,所以A在物质X的转化率比B在X的转化率大,B错误;
C.当打开K时,整个装置是在等温、等压条件下反应,使整个装置中气体的压强与A装置中的初始压强相同时,A和B的体积之和为3aL,其中B占aL,则A占2aL;当等温等压条件下反应达到平衡状态时,混合气体的体积是原来的1.2倍,即混合气体的体积是3.6aL,其中B是aL,所以A是2.6aL,C错误;
D.不能确定该反应的正反应是放热反应还是吸热反应,所以升高温度,不能确定平衡移动方向,则A容器的容积可能增大,也可能减小,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】电导率可用于衡量电解质溶液导电能力的大小。向一定浓度的![]() 溶液中滴入某浓度的
溶液中滴入某浓度的![]() 溶液,其电导率随滴入的
溶液,其电导率随滴入的![]() 溶液体积的变化如图所示。下列说法不正确的是( )
溶液体积的变化如图所示。下列说法不正确的是( )
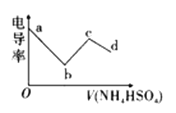
A. bc段的离子方程式为:![]()
B. c点溶液中:![]()
C. bc段之间存在某点,其溶液中:![]()
D. b点溶液存在三个平衡,且水的电离被抑制
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 与
与![]() 反应制备KI固体,装置如图所示。实验步骤:①检查装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得
反应制备KI固体,装置如图所示。实验步骤:①检查装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得![]() ;③打开K,通入
;③打开K,通入![]() 直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加热,充分逸出
直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加热,充分逸出![]() ;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可得成品。下列有关该实验的叙述错误的是( )
;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可得成品。下列有关该实验的叙述错误的是( )
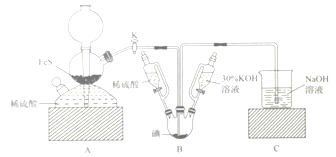
A. 步骤②可观察到固体溶解,溶液由棕黄色变为无色
B. 步骤③装置B中发生反应的离子方程式为![]()
C. 装置C中氢氧化钠溶液的作用是吸收硫化氢
D. 步骤⑤中一系列操作为过滤,洗涤,合并滤液和洗液,蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ba(OH)2 是一种强碱,可用于测定天然气中 CO2 的含量。
(1)CO2 的密度比空气______(填“大”或“小”)
(2)①称取5.25g 试样[含有 Ba(OH)2xH2O 和杂质]配成 100 mL 溶液,配制溶液中用到的仪器有天平、药匙、量筒、烧杯、玻璃棒、______、胶头滴管。用 15.00 mL 0.2 mol/L盐酸与上述 Ba(OH)2 溶液反应,消耗该 Ba(OH)2溶液 10.00 mL(杂质不与酸反应)
②另取5.25 g 试样加热至失去全部结晶水(杂质不分解),称得剩余固体质量为3.09 g, 求 Ba(OH)2xH2O中的 x=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A. 图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B. 图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C. 图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
D. 图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的衍生物A的化学式为C6H12O2,已知:

又知D不与Na2CO3反应,C和E均不能发生银镜反应,则A的结构可能有( )
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂废水中含5.00×10-3mol·L-1的![]() ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料![]() (
(![]() 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:
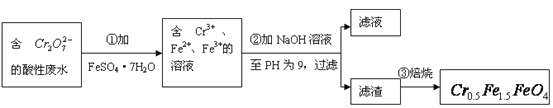
(1)第①步反应的离子方程式是_________________________________________________;
(2)第②步中用pH试纸测定溶液pH的操作是:
______________________________________________________________________________;
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有______________________;
(4)欲使1L该废水中的![]() 完全转化为
完全转化为![]() 。理论上需要加入__________g FeSO4·7H2O。
。理论上需要加入__________g FeSO4·7H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对电解质溶液作如下的归纳总结(均在常温下)。其中正确的是
A. pH=3的强酸溶液1mL,加水稀释至100mL后,溶液pH降低2个单位
B. 1L 0.50mol·L-1NH4Cl 溶液与2L 0.25mol·L-1NH4Cl 溶液含NH4+物质的量后者大
C. pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. pH=4、浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如下图所示,其中P端通入CO2。通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是

A. X、Y两端都必须用铁作电极
B. 不可以用NaOH溶液作为电解液
C. 阴极发生的反应是:2H2O+ 2e-= H2↑+ 2OH-
D. X端为电解池的阳极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com