
【题目】1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
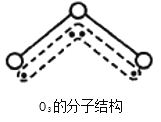
(1)选出下列分子与O3分子的结构最相似的的是___________。
A. H2O B.CO2 C.SO2 D.BeCl2
(2)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有___________对孤对电子。
(3)O3分子是_____________分子(填极性或非极性)。
(4)O3 能使淀粉碘化钾试纸变蓝2KI+O3+H2O===2KOH+I2+O2则氧化产物和还原产物的物质的量之比为____
【答案】 C 5 极性 1:2
【解析】试题分析:(1)根据臭氧分子结构进行分析;(2)根据孤对电子的概念及臭氧分子结构分析;(3)臭氧中的化学键都是非极性键;(4)根据氧化产物和还原产物的定义分析。
解析:(1)在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子称折线形,在三个氧原子之间还存在着一个垂直于分子平面的大π键,这个离域的π键是由中心的氧原子提供两个p电子、另外两个配位氧原子各提供一个p电子形成的,SO2分子呈“V”字形结构,其成键方式与O3类似,S原子sp2杂化,S原子和两侧的氧原子除以σ键结合以外,还形成一个三中心四电子的大π键,
故选C;
(2)中间的氧原子含有1对孤电子对,两边的各含有2对孤电子对,所以总共5对孤电子对;(3)由于臭氧分子中的化学键都是非极性键,所以臭氧分子属于非极性分子;
(4) 2KI+O3+H2O===2KOH+I2+O2,KI中碘元素化合价升高被氧化为碘单质,碘单质是氧化产物,O3中氧元素化合价降低,被还原为KOH,KOH是还原产物,所以氧化产物和还原产物的物质的量之比为1:2。


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】烃基异构化是当前环保的急切要求,正戊烷异构化为异戊烷的热化学方程式是: CH3CH2CH2CH2CH3![]() CH3CH(CH3)CH2CH3 △H=-7.1 kJ·mol-1
CH3CH(CH3)CH2CH3 △H=-7.1 kJ·mol-1
(1)正戊烷异构化反应选择的温度条件是____________。
(2)由于副反应较为复杂,提髙产率的最佳方法是____________。
(3)如果提高温度,反应速率___________,转化率___________(填“升高"“不变”或“降低” ),同时还会产生积炭现象,假如在反应物中掺入一定量水,则可以减弱这种现象,理由是___________(用化学方程式表示)。
(4)在573 K时,正戊烧转化率为54%,则此时平衡常数为___________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2 是一种高效安全的杀菌消毒剂。用氯化钠电解法生成ClO2的工艺原理示意图如下图, 发生器内电解生成ClO2。下列说法正确的是
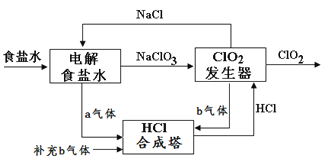
A. a气体是氯气,b气体是氢气
B. 氯化钠电解槽内每生成2 mol a气体,转移2mol e-
C. ClO2发生器中阴极的电极反应式为:2ClO3- + 12H+ + 10e-![]() Cl2↑ + 6H2O
Cl2↑ + 6H2O
D. 为使a、b气体恰好完全反应,理论上每生产1molClO2需要补充56L(标准状况)b气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置 如右下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1︰2,以下说法不正确的是

A. a极与电源的正极相连
B. 产物丙为硫酸溶液
C. 离子交换膜d为阳离子交换膜(允许阳离子通过)
D. a电极反应式为2H2O+2e-=2OH-+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素X的气态氢化物在高温下分解为固态的X单质和H2,分解反应前后气体的质量之比是17:1。下列有关叙述中错误的是
A. X的阴离子的电子排布式是1s22s22p63s23p6
B. X的最高价氧化物对应的水化物的酸性比砷酸强
C. X的最高价氧化物中,X的质量分数为50%
D. X的气态氢化物的水溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于CaF2的表述正确的是
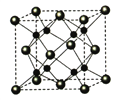
A. Ca2+与F-间仅存在静电吸引作用
B. F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
C. 阴阳离子比为2:1的物质,均与CaF2晶体构型相同
D. CaF2中的化学键为离子键,因此CaF2在晶体状态下能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0,下列叙述正确的是( )
H++OH- ΔH>0,下列叙述正确的是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量CH3COOH,平衡逆向移动,c(H+)降低
D. 将水加热,Kw增大,pH不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com