
【题目】【化学—选修5:有机化学基础】化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成:
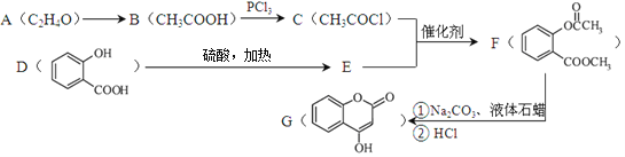
(1)G中含有的官能团名称为 。
(2)B→C的反应类型是 。
(3)1 mol D最多可与 mol H2加成。写出D→E的化学方程式 。
(4)写出同时满足下列条件的D的一种同分异构体的结构简式 。
A.能发生银镜反应
B.核磁共振氢谱只有4个峰
C.能与FeCl3溶液发生显色反应,水解时1 mol可消耗3 mol NaOH
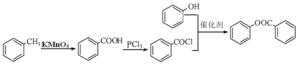
(5)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化。甲苯可被酸性高锰酸钾溶液氧化为苯甲酸。苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。合成路线流程图示例如
)是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。合成路线流程图示例如![]()
【答案】(1)羟基、酯基、碳碳双键(各1分,共3分)
(2)取代反应(2分)
(3)3;![]() (2分)
(2分)
(4)![]() (2分)
(2分)
(5)
【解析】
试题分析:(1)根据G的结构简式可知,分子中含有的官能团名称为羟基、酯基、碳碳双键;
(2)B→C是羧基中羟基被氯原子代替,是取代反应;
(3)苯环能与氢气加成,1 mol D最多可与3mol H2加成。根据F的结构简式可知D生成E是羧基与甲醇发生酯化反应,反应的化学方程式为![]() ;
;
(4)B为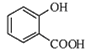 ,能满足如下条件A.能发生银镜反应,含有醛基,B.核磁共振氢谱只有4个峰,即有4组不同环境的氢原子,C.能与FeCl3溶液发生显色反应,有酚羟基,水解时1mol可消耗3molNaOH,含有酯基,综上所述,该物质应该为甲酸苯酚酯,结合核磁共振氢普,其结构简式为
,能满足如下条件A.能发生银镜反应,含有醛基,B.核磁共振氢谱只有4个峰,即有4组不同环境的氢原子,C.能与FeCl3溶液发生显色反应,有酚羟基,水解时1mol可消耗3molNaOH,含有酯基,综上所述,该物质应该为甲酸苯酚酯,结合核磁共振氢普,其结构简式为![]() ;
;
(5)甲苯可以被酸性高锰酸钾氧化为苯甲酸,所以苯甲酸由甲苯氧化得到,由于酚羟基一般不易直接与羧酸酯化,所以可以根据题目中的乙酰氯制备D的方法来制备本甲酸苯酚酯,即把苯甲酸转化为苯甲酰氯,然后再与苯酚反应得到,上述反应流程为 。
。


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】某氯化亚铁和氯化铁的混合物.现要测定其中铁元素的质量分数,按如图步骤进行实验: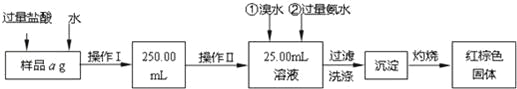
请根据以上流程,回答下列问题:
(1)样品溶解过程中加入少量浓盐酸的目的是什么?
操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有哪些仪器?
操作Ⅱ中可用的玻璃仪器是什么仪器?
(2)请写出加入氨水发生的离子反应方程式。
(3)沉淀洗涤的方法是什么?
(4)将沉淀物灼烧,冷却到室温,用天平称量其质量为b1g,再次灼烧并冷却至室温称量其质量为b2g,若b1﹣b2=0.3g,则接下来还应进行的操作是 .若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时每转移3mol电子,正极有1mol K2FeO4被氧化
B.充电时阳极反应为:Fe(OH)3﹣3e﹣+5 OH﹣═FeO42﹣+4H2O
C.放电时正极附近溶液的碱性增强
D.放电时负极反应为:Zn﹣2e﹣+2OH﹣═Zn(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是____________________。再由a向c中加2 mL蒸馏水,c中的实验现象是 ___________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是_____________。理由是_____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是
A.用溴水可以鉴别苯、CCl4、己烯
B.加浓溴水,然后过滤可除去苯中少量己烯
C.苯、溴水、铁粉混合制成溴苯
D.可用分液漏斗分离己烷和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化钙在2973 K时熔化,而NaCl在1074 K时熔化,二者的离子间距和晶体结构都类似,有关它们熔点差别较大的原因叙述不正确的是
A.氧化钙晶体中阴、阳离子所带电荷数多
B.氧化钙晶格能比氯化钠的晶格能大
C.两种晶体的晶胞结构类型不同
D.氧化钙、氯化钠的离子间距类似情况下,晶格能主要由阴、阳离子所带电荷数决定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ.NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-1
2CO(g)+O2(g)![]() 2 CO2(g) △H=-566.00kJ·mol-1
2 CO2(g) △H=-566.00kJ·mol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环。写出该反应的热化学方程式_________________。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0-15min)中NO的物质的量随时间变化的关系如右图所示。


①T℃时该化学反应的平衡常数K=_______________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将_______移动。(填“向左”、“向右”或“不)
②图中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是__________(填“a”或“b”)。
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是_______。
Ⅱ.SO2主要来源于煤的燃烧。燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)用纯碱溶液吸收SO2可将其转化为HSO3-。该反应的离子方程式是___________________。
(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_____________,阴极的电极反应式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,不正确的是( )
A. 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌
B. 试管、烧杯、烧瓶、蒸发皿、量筒都可以直接在火焰上加热
C. 可燃性气体点燃前必须验纯
D. 制备蒸馏水时,弃去开始馏出的部分液体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com